ГОСТ Р 52147-2003
Группа С19
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
БЕЛКОВО-ВИТАМИННО-МИНЕРАЛЬНЫЕ И АМИДО-ВИТАМИННО-МИНЕРАЛЬНЫЕ ДОБАВКИ
Методы определения содержания ретинола-ацетата (витамина А),
эргокальциферола (холекальциферола) (витамина D),
токоферола-ацетата (витамина Е)
Protein-vitamin-mineral and amide-vitamin-mineral additives.
Methods for the determination of retinol-acetate (vitamin A), argocalciferol
(holecalciferol) (vitamin D), tokoferol-acetate (vitamin E)
ОКС 65.120
ОКСТУ 9209
Дата введения 2005-01-01
Предисловие
1 РАЗРАБОТАН Открытым акционерным обществом "Всероссийский научно-исследовательский институт комбикормовой промышленности" (ОАО "ВНИИКП");
Всероссийским научно-исследовательским и технологическим институтом птицеводства (ВНИТИП);
Всероссийским научно-исследовательским институтом кормов им. В.Р.Вильямса (ВНИИК)
ВНЕСЕН Техническим комитетом по стандартизации ТК 4 "Комбикорма, белково-витаминные добавки, премиксы"
2 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 3 декабря 2003 г. N 342-ст
3 ВВЕДЕН ВПЕРВЫЕ
1 Область применения
1 Область применения
Настоящий стандарт распространяется на белково-витаминно-минеральные и амидо-витаминно-минеральные добавки и устанавливает хроматографические методы определения ретинола-ацетата (витамина А), эргокальциферола (холекальциферола) (витамина D), токоферола-ацетата (витамина Е)
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура средств защиты
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4147-74 Железо (III) хлорид 6-водный. Технические условия
ГОСТ 4166-76 Натрий сернокислый. Технические условия
ГОСТ 4517-87 Реактивы. Методы приготовления вспомогательных реактивов и растворов, применяемых при анализе
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование фарфоровые. Технические условия
ГОСТ 9736-91 Приборы электрические прямого преобразования для измерения неэлектрических величин. Общие технические требования и методы испытаний
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 19627-74 Гидрохинон (парадиоксибензол). Технические условия
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
ГОСТ 24363-80 Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29169-91 (ИСО 648-77) Посуда лабораторная стеклянная. Пипетки с одной отметкой
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
3 Определения
В настоящем стандарте применяют следующие термины с соответствующими определениями.
3.1 Содержание витамина А: Содержание ретинола-ацетата, определенное в соответствии с настоящим стандартом и выраженное в международных единицах в 1 кг испытуемой пробы (МЕ/кг). 1 ME витамина А соответствует 0,344 мкг ретинола-ацетата.
3.2 Содержание витамина Е: Содержание токоферола-ацетата, определенное в соответствии с настоящим стандартом и выраженное в миллиграммах в 1 кг (мг/кг) испытуемой пробы.
3.3 Содержание витамина D: Содержание эргокальциферола (витамина ) или холекальциферола (витамина
), определенное в соответствии с настоящим стандартом и выраженное в международных единицах в 1 кг испытуемой пробы (МЕ/кг). 1 ME витамина D соответствует 0,025 мкг эргокальциферола (холекальциферола).
4 Диапазоны измерений содержания витаминов и характеристики погрешности измерений
Диапазоны измерений содержания витаминов и характеристики погрешности измерений приведены в таблице 1.
Таблица 1
Наименование витамина и его единица измерения | Вид хроматографии | Диапазон измерений содержания витамина | Границы относительной погрешности, %, ( |
Витамин А, тыс. МЕ/кг | Колоночная | От 5,0 до 50 включ. | ±25 |
Св. 50 " 100 " | ±20 | ||
" 100 " 300 " | ±15 | ||
ВЭЖ | От 5,0 до 100 включ. | ±20 | |
Св. 100 " 300 " | ±15 | ||
Витамин Е, мк/кг | Колоночная | От 10 до 500 включ. | ±20 |
Св. 500 " 1000 " | ±15 | ||
ВЭЖ | От 10 до 100 включ. | ±20 | |
Св. 100 " 1000 " | ±15 | ||
Витамин D, тыс. МЕ/кг | ВЭЖ | От 5,0 до 20 включ. | ±20 |
Св. 20 " 50 " | ±15 |
5 Требования техники безопасности
5.1 При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования пожарной безопасности по ГОСТ 12.1.004 и ГОСТ 12.1.018 и электробезопасности при работе с электроустановками по ГОСТ 12.1.019, а также требования, изложенные в технической документации на фотоэлектроколориметр, спектрофотометр и хроматограф.
5.2 Помещение, в котором проводят измерения, должно быть снабжено приточно-вытяжной вентиляцией. Работу необходимо проводить в вытяжном шкафу.
5.3 При работе с газовыми баллонами необходимо руководствоваться НД [1].
6 Подготовка проб к испытанию
6.1 Отбор проб - по ГОСТ 13496.0.
6.2 Измельчение пробы
6.2.1 Оборудование:
мельница лабораторная электрическая, обеспечивающая измельчение пробы до прохода остатка через сито с отверстиями диаметром 1 мм;
сито с отверстиями диаметром 1 мм.
6.2.2 Из средней пробы исследуемого продукта методом квартования выделяют часть пробы массой не менее 100 г и измельчают на лабораторной мельнице до такого состояния, чтобы весь продукт проходил через сито с отверстиями диаметром 1 мм без остатка. Размолотую пробу тщательно перемешивают.
7 Определение содержания ретинола-ацетата (витамина А) и токоферола-ацетата (витамина Е) фотометрическим методом
Сущность метода заключается в омылении образца водно-спиртовым раствором гидроокиси калия, экстракции витаминов диэтиловым эфиром, разделении витаминов хроматографией на колонке с окисью алюминия и количественном определении витаминов фотометрическим методом.
7.1 Аппаратура, материалы и реактивы
Весы лабораторные высокого класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104.
Спектрофотометр типа СФ-26, СФ-46 со спектральным диапазоном работы 186-1100 нм, основной погрешностью измерений коэффициента пропускания не более 1%, градуировкой длин волн в ультрафиолетовой (УФ) области - не более 0,1 нм.
Фотоэлектроколориметр с пределом измерений оптической плотности от 0 до 2, основной погрешностью измерений не более 1% и светофильтром длиной волны =(520±25) нм.
Холодильник бытовой по ГОСТ 16317.
Баллон с азотом рабочим давлением от 40 до 60 кг/см (от 4 до 6 МПа) [1].
Испаритель ротационный диапазоном измерения рабочего давления от 7 до 760 мм рт.ст. (от 9·10 до 10·10
Па) или насос водоструйный по ГОСТ 25336.
Баня водяная с регулятором нагрева.
Термометр жидкостный по ГОСТ 28498.
Печь муфельная электрическая, обеспечивающая поддержание температуры от 0 до 800 °С с погрешностью ±10 °С по ГОСТ 9736.
Секундомер [2].
Чашки выпарительные фарфоровые диаметром 123 мм по ГОСТ 9147.
Щипцы для тиглей муфельные.
Лампа ультрафиолетовая со светофильтрами =260-350 нм.
Шкаф сушильный, обеспечивающий поддержание температуры от 0 °С до 110 °С с погрешностью ±2 °С [3].
Холодильники стеклянные лабораторные по ГОСТ 25336.
Колбы конические со шлифом -1-100(250)-24/29 по ГОСТ 25336.
Колбы мерные 1(2)-50(100, 200)-2 по ГОСТ 1770.
Воронки делительные вместимостью 250, 500 см по ГОСТ 25336.
Цилиндры мерные 1(2, 2а, 3, 4, 4а)-25(100, 250)-2 по ГОСТ 1770.
Воронки для фильтрования ВФ-1-56(75)ХС по ГОСТ 25336.
Пипетки с одной отметкой 1-2-0,5(1,2) по ГОСТ 29169.
Пипетки градуированные 1(2, 3, 5)-1(1а, 2, 2а)-2-0,5(1, 2, 5) по ГОСТ 29227.
Пробирки мерные с притертыми пробками П-1(2)-5(10)-0,1(0,2)ХС по ГОСТ 1770.
Склянки из темного стекла.
Колбы с тубусом вместимостью 250 см по ГОСТ 25336.
Колбы круглодонные К-1-100(250)-14/23(19/26) по ГОСТ 25336.
Колонки стеклянные для хроматографии размером 10х200 мм.
Эксикатор по ГОСТ 25336, заправленный хлористым кальцием, прокаленным при температуре 250-300 °С в течение 2 ч.
Бумага фильтровальная по ГОСТ 12026 или фильтры [4].
Вата обезжиренная, готовят по ГОСТ 4517.
Палочки деревянные.
Витамин Е фармакопейный [5].
Спирт этиловый абсолютированный [6] или приготовленный по ГОСТ 4517.
Железо хлорное, раствор массовой долей около 0,2% в абсолютированном этиловом спирте.
Калия гидроокись по ГОСТ 24363, раствор массовой долей 50%.
Натрий сернокислый по ГОСТ 4166, безводный.
Алюминия окись, безводная [7].
Эфир петролейный, фракция (40-70) °С, не содержащая ненасыщенные и ароматические углеводороды.
Эфир диэтиловый фармакопейный, не содержащий пероксидные соединения (испытание на отсутствие пероксидных соединений - по ГОСТ 4517).
Пирогаллол или гидрохинон по ГОСТ 19627.
Спирт этиловый ректификованный по ГОСТ Р 51652.-фенантролин или
,
-дипиридил, раствор массовой долей около 0,5% в абсолютированном этиловом спирте.
Кислота аскорбиновая [8].
Фенолфталеин [9], спиртовый раствор массовой долей 1%.
Вода дистиллированная по ГОСТ 6709.
Примечания
1 Допускается применение других средств измерений с метрологическими характеристиками и оборудования с техническими характеристиками, а также материалов и реактивов по качеству не ниже вышеуказанных.
2 Все реактивы должны быть квалификации х.ч. или ч.д.а.
7.2 Подготовка к испытанию
7.2.1 Приготовление раствора хлорного железа массовой долей около 0,2% в абсолютированном спирте.
Навеску реактива массой 0,2 г растворяют в 99,8 см абсолютированного этилового спирта.
Раствор хранят в холодильнике в склянке из темного стекла не более 7 сут.
7.2.2 Приготовление раствора -фенантролина или
,
-дипиридила массовой долей около 0,5% в абсолютированном этиловом спирте
Навеску реактива массой 0,500 г растворяют в 99,5 см абсолютированного этилового спирта.
Раствор хранят в холодильнике в склянке из темного стекла не более 7 сут.
7.2.3 Приготовление безводного сернокислого натрия
Реактив высушивают в сушильном шкафу при температуре (105±2) °С в течение 3 ч, хранят в склянке с притертой пробкой.
7.2.4 Приготовление окиси алюминия
Реактив прокаливают в муфельной печи при температуре (400±10) °С в течение 4 ч, охлаждают до комнатной температуры в эксикаторе. К 97 г реактива добавляют 3 см дистиллированной воды и тщательно перемешивают.
После отстаивания в течение не менее 3 ч реактив годен к использованию.
Реактив хранят в склянке с притертой пробкой.
7.2.5 Приготовление раствора -токоферола массовой концентрации 1 мг/см
Навеску токоферола-ацетата массой 0,1120 г в расчете на содержание чистого вещества помещают в круглодонную колбу со шлифом вместимостью 250 см добавляют от 100 до 200 мг аскорбиновой кислоты, 50 см
этилового спирта и 10 см
раствора гидроокиси калия массовой долей 50%. Колбу соединяют с обратным холодильником и нагревают в водяной бане при температуре (85±2) °С в течение 25 мин. Затем содержимое колбы быстро охлаждают под струей водопроводной воды до комнатной температуры, переносят в делительную воронку вместимостью 250 см
, приливают по 50 см
дистиллированной воды и диэтилового эфира, встряхивают и отстаивают до разделения слоев.
После расслаивания нижний водно-спиртовый слой сливают в коническую колбу, а эфирный слой оставляют в делительной воронке. В коническую колбу приливают 50 см диэтилового эфира, встряхивают, отстаивают и после расслаивания верхний эфирный слой присоединяют к эфирному экстракту в делительной воронке, а к водно-спиртовому слою в конической колбе снова приливают 50 см
диэтилового эфира и проводят экстракцию, как было указано выше. После расслаивания эфирный слой из конической колбы снова присоединяют к экстракту в делительной воронке.
Объединенные эфирные экстракты промывают дистиллированной водой порциями по 30 см до исчезновения розовой окраски промывных вод по реакции с фенолфталеином. Промытый экстракт переносят в коническую колбу вместимостью 250 см
, пропуская его через бумажный фильтр и слой безводного сернокислого натрия (10-15 г). После окончания фильтрации сернокислый натрий три раза промывают порциями (по 20-30 см
) диэтилового эфира. Эфир отгоняют в водяной бане при температуре не выше 50 °С в токе азота или под вакуумом, используя водоструйный насос или роторный испаритель.
К сухому остатку приливают 10-15 см абсолютированного этилового спирта, количественно переносят раствор в мерную колбу вместимостью 100 см
, доводят объем в колбе до метки этим же спиртом и тщательно перем
ешивают.
7.2.6 Приготовление раствора -токоферола массовой концентрации 20 мкг/см
1 см раствора
-токоферола массовой концентрации 1 мг/см
переносят в мерную колбу вместимостью 50 см
, доводят объем в колбе абсолютированным спиртом до метки и тщательно перемешивают.
В полученном растворе проверяют массовую концентрацию -токоферола и его чистоту, снимая спектр в пределах 260-310 нм на спектрофотометре в кювете толщиной поглощающего свет слоя 1 см относительно абсолютированного этилового спирта. Чистый
-токоферол имеет симметричный пик максимумом поглощения при длине волны 292 нм.
Массовую концентрацию -токоферола в растворе
, мкг/см
, вычисляют по формуле
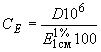 , (1)
, (1)
где - оптическая плотность раствора при длине волны 292 нм;
- коэффициент пересчета граммов в микрограммы;
- оптическая плотность раствора
-токоферола в абсолютированном этиловом спирте массовой концентрации 1 г в 100 см
при длине волны 292 нм и толщине поглощающего свет слоя 1 см (для
-токоферола
=75)
.
7.2.7 Построение градуировочного графика для определения токоферола-ацетата (витамина Е)
В пять мерных пробирок вместимостью по 5 см приливают 0,5; 1,0; 2,0; 3,0 и 4,0 см
раствора
-токоферола массовой концентрации 20 мкг/см
. В первые четыре пробирки добавляют 3,5; 3,0; 2,0 и 1,0 см
абсолютированного этилового спирта. Затем в пробирки добавляют по 0,5 см
раствора
-фенантролина и по 0,5 см
раствора хлорного железа, перемешивают. Ставят опытную пробу в темное место на 5 мин для развития окраски. По истечении времени измеряют оптические плотности испытуемых растворов в порядке возрастания их концентрации на фотоэлектроколориметре в кювете толщиной поглощающего свет слоя 10 мм при длине волны (520±25) нм относительно абсолютированного этилового спирта. Одновременно проводят контрольное испытание на реактивы без внесения
-токоферола.
По полученным данным строят градуировочный график, откладывая на оси ординат значения разности оптической плотности испытуемых растворов и контрольного раствора, на оси абсцисс - содержание -токоферола, мкг/5 см
(10, 20, 40, 60 и 80 мкг/
5 см)
7.2.8 Приготовление элюирующих растворов
7.2.8.1 Приготовление раствора I
В мерную колбу вместимостью 100 см вносят 6 см
диэтилового эфира и объем жидкости в колбе доводят до метки петролейным эфиром, перемешивают.
7.2.8.2 Приготовление раствора II
В мерную колбу вместимостью 100 см вносят 12 см
диэтилового эфира и объем жидкости в колбе доводят до метки петролейным эфиром, перемешивают.
7.2.8.3 Приготовление раствора III
В мерную колбу вместимостью 100 см вносят 30 см
диэтилового эфира и объем жидкости в колбе доводят до метки петролейным эфиром, перемешивают.
7.3 Проведение испытаний
Из-за высокой чувствительности витаминов к ультрафиолетовому свету и воздуху все процедуры, связанные с анализом, следует завершить в течение одного рабочего дня, избегая воздействия натурального и интенсивного флуоресцентного света.
7.3.1 Омыление и экстракция
Навеску исследуемого продукта массой 4,00-5,00 г помещают в круглодонную колбу со шлифом вместимостью 250 см, приливают 50 см
этилового спирта, 10 см
раствора гидроокиси калия массовой долей 50% и добавляют 40-50 мг пирогаллола или гидрохинона (на кончике скальпеля).
Колбу соединяют с обратным холодильником, помещают в водяную баню и нагревают при температуре (85±2) °С в течение 25 мин, периодически перемешивая содержимое колбы. После этого содержимое колбы охлаждают до комнатной температуры.
Затем в колбу приливают 20-25 см дистиллированной воды, 50 см
диэтилового эфира, перемешивают, жидкую часть сливают в делительную воронку вместимостью 500 см
, сохраняя осадок в колбе. Экстракцию витаминов диэтиловым эфиром проводят трижды по 7.2.5.
При образовании устойчивой эмульсии в делительную воронку добавляют 20 см этилового спирта.
В объединенный эфирный экстракт добавляют несколько кристаллов бутилокситолуола и промывают его дистиллированной водой порциями по 100 см до исчезновения розовой окраски промывных вод по реакции с фенолфталеином. Затем экстракт переносят в круглодонную колбу, пропуская его через бумажный фильтр со слоем безводного сернокислого натрия (30-50 г). Делительную воронку и фильтрующий материал промывают 40 см
диэтилового эфира. Эфир выпаривают досуха в водяной бане при температуре не выше 50 °С в токе азота или под вакуумом на ротационном испарителе. Сухой остаток растворяют в 4 см
петролейного эфира.
Примечание - Допускается для экстракции применять петролейный эфир.
7.3.2 Подготовка хроматографической колонки
В нижнюю часть колонки помещают кусочек ваты, затем активированную окись алюминия, уплотняя ее постукиванием по колонке деревянной палочкой до высоты сорбента 7 см. Сверху помещают слой безводного сернокислого натрия высотой 1 см.
В колбу с тубусом вставляют резиновую пробку, через сквозное отверстие которой проходит утонченный конец хроматографической колонки. Через колонку при вакууме, создаваемом с помощью водоструйного насоса пропускают петролейный эфир до полного смачивания слоя окиси алюминия (около 15 см).
Промывание колонки проводят со скоростью одна капля в секунду, не допуская при этом высыхания верха колонки и просасывания воздуха.
7.3.3 Хроматографическое разделение ретинола и -токоферола
4 см раствора экстракта испытуемого продукта, полученного по 7.3.1, помещают в колонку, подготовленную по 7.3.2, не допуская высыхания верха колонки. Промывают колонку 15 см
элюирующего раствора I. Эту фракцию отбрасывают.
-токоферол элюируют от 15 до 25 см
раствора II, контролируя продвижение витамина в УФ свете (
-токоферол имеет голубоватое свечение).
Элюат количественно переносят в коническую колбу вместимостью 50 см.
К колонке присоединяют другую колбу с тубусом и элюируют ретинол 30-35 см раствора III, также контролируя продвижение витамина в УФ-свете (ретинол имеет желто-зеленое свечение). Элюат количественно переносят в коническую колбу вместимостью 50 см
и выпаривают досуха в водяной бане при температуре не выше 50 °С в токе азота или под вакуумом.
Сухой остаток растворяют в 5-50 см абсолютированного этилового спирта в зависимости от предполагаемого содержания витамин
а А.
7.3.4 Оптическую плотность полученного раствора ретинола измеряют на спектрофотометре при длине волны 326 нм в кювете толщиной поглощающего свет слоя 10 мм относительно абсолютированного этилового спирта.
7.3.5 Проведение цветной реакции с раствором -токоферола
Собранный и перенесенный в коническую колбу элюат -токоферола выпаривают досуха на водяной бане при температуре не выше 50 °С в токе азота или под вакуумом. Остаток растворяют в 10 см
абсолютированного этилового спирта. Ориентируясь на рецептуру добавки, берут 0,2-3,5 см
раствора и переносят в кювету толщиной поглощающего свет слоя 10 мм или в мерную пробирку вместимостью 5 см
, добавляют соответственно от 3,8 до 0,5 см
абсолютированного этилового спирта, 0,5 см
раствора
-фенантролина и 0,5 см
раствора хлорного железа. Опытную пробу ставят в темное место на 5 мин для развития окраски. По истечении времени измеряют оптическую плотность испытуемого раствора на фотоэлектроколориметре при длине волны (520±25) нм относительно абсолютированного этилового спирта.
Одновременно проводят контрольное испытание на реактивы без внесения -токоферо
ла.
7.4 Обработка и оформление результатов
7.4.1 Содержание ретинола-ацетата , МЕ/кг, в испытуемой пробе вычисляют по формуле
![]() , (2)
, (2)
где 18,3 - массовая концентрация раствора ретинола в абсолютированном этиловом спирте, имеющего оптическую плотность, равную 1, при длине волны 326 нм и толщине поглощающего свет слоя 1 см, МЕ/см;
- объем элюата (5-50), см
;
- оптическая плотность раствора;
10 - коэффициент пересчета граммов в килограммы;
- масса навески, г;
1,15 - коэффициент пересчета ретинола в ретинол-ацетат.
7.4.2 Содержание токоферола-ацетата , мг/кг, в испытуемой пробе вычисляют по формуле
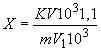 , (3)
, (3)
где - масса
-токоферола, найденная по градуировочному графику, мкг;
- объем раствора элюата (10), см
;
10 - коэффициенты пересчета микрограммов в миллиграммы и граммов в килограммы;
1,1 - коэффициент пересчета -токоферола в ацетатную форму;
- масса навески, г;
- объем раствора, взятый для проведения цветной реакции (0,2-3,5), с
м.
7.4.3 Результат вычисляют до третьей значащей цифры и округляют до двух значащих цифр.
7.4.4 При анализе каждой пробы выполняют два параллельных определения, начиная со взятия навески испытуемой пробы. Если расхождение между результатами параллельных определений не превышает допустимое ![]() , где
, где ,
и
- результат первого и второго параллельных определений и их среднеарифметическое значение соответственно, то среднеарифметическое значение принимают за результат анализа. В противном случае анализ повторяют.
Если расхождения между параллельными определениями вновь превышают регламентируемые допуски, выясняют и устраняют причины плохой сходимости результатов анализа.
Значения приведены в таблице 2.
Таблица 2
Наименование витамина и единица | Вид | Диапазон измерений массовой доли | Значение норматива контроля, %, | |
измерения | витамина | сходимости | воспро- | |
Витамин А, тыс. | Колоночная | От 5,0 до 50 включ. | 20 | 35 |
Св. 50 " 100 " | 15 | 25 | ||
" 100 " 300 " | 10 | 20 | ||
ВЭЖ | От 5,0 до 100 включ. | 15 | 25 | |
Св. 100 " 300 " | 10 | 20 | ||
Витамин Е, мг/кг | Колоночная | От 10 до 100 включ. | 15 | 30 |
Св. 100 " 500 " | 10 | 25 | ||
" 500 " 1000 " | 10 | 20 | ||
ВЭЖ | От 10 до 100 включ. | 12 | 28 | |
Св. 100 " 1000 " | 8 | 20 | ||
Витамин D, тыс. | ВЭЖ | От 5,0 до 20 включ. | 20 | 30 |
Св. 20 " 50 " | 12 | 22 |
По полученному результату анализа и значению относительной погрешности (таблица 1) рассчитывают абсолютную погрешность по формуле
![]() .
.
Результат анализа представляют в виде ![]() МЕ/кг или
МЕ/кг или ![]() мг/кг при
мг/кг при =0,95.
8 Определение содержания ретинола-ацетата (витамина А), эргокальциферола (холекальциферола) (витамина D), токоферола-ацетата (витамина Е) методом высокоэффективной жидкостной хроматографии (ВЭЖХ)
Сущность метода заключается в омылении образца водно-спиртовым раствором гидроокиси калия, экстракции витаминов диэтиловым эфиром с последующим определением витаминов на жидкостном хроматографе.
При содержании витамина D в испытуемом продукте менее 10 МЕ/г перед проведением высокоэффективной жидкостной хроматографии (ВЭЖХ) необходима очистка экстракта на колонке с окисью алюминия по 8.3.2. Анализ проводят из отдельно взятой навески массой 10 г.
8.1 Аппаратура, материалы и реактивы
Аппаратура, материалы и реактивы по 7.1 со следующим дополнением.
Хроматограф жидкостный "Милихром" с УФ-детектором со спектральным диапазоном 190-360 нм, обеспечивающий одновременное измерение на не менее 3 длинах волн с уровнем шумов не более 10 единиц оптической плотности (е.о.п.).
Колонка аналитическая хроматографическая для ВЭЖХ, размером 80 (64, 120)х2 мм, заполненная сорбентом Силасорб 600 (размер частиц 5 мкм) с эффективностью не ниже 5000 теоретических тарелок.
Прибор для перегонки при атмосферном давлении [10].
Ретинол-ацетат (витамин А) фармакопейный [11].
Эргокальциферол кристаллический (витамин ) [12] или холекальциферол кристаллический (витамин
) [13].
Спирт изопропиловый [14].
Гексан [15].
Алюминия окись для хроматографии [16].
2,6-Ди-трет-бутил-п-крезол (бутиолокситолуол) [17].
Примечание - Допускается применение других типов хроматографов, сорбентов и соответствующих им растворителей, обеспечивающих эффективное разделение исследуемых компонентов. При этом условия разделения витаминов подбираются самостоятельно каждым пользователем.
8.2 Подготовка к испытанию
8.2.1 Приготовление элюирующего раствора
Готовят смесь гексана с изопропиловым спиртом в объемном соотношении 98,5:1,5 (98:2)
8.2.2 Очистка изопропилового спирта
Изопропиловый спирт перегоняют над гидроокисью калия или натрия (10 г гидроокиси требуется для перегонки 1 дм спирта).
Реактив должен иметь оптическую плотность не более 0,1 е.о.п. при =320-350 нм относительно дистиллированной воды.
8.2.3 Приготовление окиси алюминия
Реактив прокаливают в муфельной печи при температуре (750±10) °С в течение 4 ч, охлаждают до комнатной температуры в эксикаторе. К 91 г реактива добавляют 9 см дистиллированной воды, тщательно перемешивают и хранят в посуде с притертой пробкой.
Годен для использования после отстаивания в течение 3 ч.
8.2.4 Приготовление безводного сернокислого натрия по 7.2.3
8.2.5 Приготовление растворов ретинола
8.2.5.1 Приготовление раствора ретинола массовой концентрации 1000 МЕ/см.
Навеску ретинола-ацетата, соответствующую 50000 ME препарата, помещают в колбу со шлифом вместимостью 250 см, добавляют около 200 мг пирогаллола или гидрохинона (на кончике скальпеля), 30 см
этилового спирта и 5 см
раствора гидроокиси калия массовой долей 50%. Колбу соединяют с обратным холодильником и проводят омыление в водяной бане при температуре (85±2) °С в течение 30 мин, охлаждают до комнатной температуры под струей водопроводной воды и добавляют 15 см
дистиллированной воды. Затем содержимое колбы переносят в делительную воронку вместимостью 250 см
, промывают колбу 20 см
этилового спирта, который тоже переносят в делительную воронку. Добавляют 30 см
смеси диэтилового эфира и гексана в объемном соотношении 1:1, полученную смесь тщательно перемешивают. После расслаивания нижний слой (водно-спиртовый) сливают в коническую колбу, а гексано-эфирный оставляют в делительной воронке. Эту операцию экстракции ретинола гексано-эфирной смесью из водно-спиртового слоя в конической колбе проводят еще дважды по 7.2.5, каждый раз сливая в делительную воронку гексано-эфирный слой. Объединенный экстракт в делительной воронке промывают дистиллированной водой порциями по 30 см
до исчезновения розовой окраски промывных вод по реакции с раствором фенолфталеина. Промытый экстракт переносят в коническую колбу вместимостью 250 см
, пропуская его через бумажный фильтр и слой безводного сернокислого натрия (40-50 г). Делительную воронку и фильтрующий материал промывают дважды порциями гексано-эфирной смеси (20-30 см
). Экстракт выпаривают досуха в водяной бане при температуре не выше 60 °С в токе азота или под вакуумом на ротационном испарителе. Сухой остаток растворяют в гексане, количественно переносят в мерную колбу вместимостью 50 см
, добавляют 100 мг бутилокситолуола, перемешивают, объем раствора в колбе доводят гексаном до метки и снова тщательно перемеш
ивают.
8.2.5.2 Приготовление градуировочных растворов ретинола массовой концентрации 20, 100 и 500 МЕ/см
В три мерные колбы вместимостью по 50 см помещают 1; 5 и 25 см
раствора ретинола массовой концентрации 1000 МЕ/см
, доводят объемы растворов в колбах до метки гексаном и тщательно перемешивают.
Оптическую плотность растворов измеряют на спектрофотометре при длине волны 326 нм в кювете толщиной поглощающего свет слоя 1 см относительно гексана.
Массовую концентрацию ретинола в растворе , МЕ/см
вычисляют по формуле
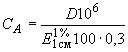 , (4)
, (4)
где - оптическая плотность раствора ретинола;
- коэффициент пересчета граммов в микрограммы;
- оптическая плотность раствора ретинола в гексане массовой концентрации 1 г в 100 см
при длине волны 326 нм и толщине поглощающего свет слоя 1 см (для ретинола
=1830);
0,3 - коэффициент пересчета массы ретинола в ME, мкг/МЕ.
8.2.6 Приготовление растворов -токоферола
8.2.6.1 Приготовление раствора -токоферола массовой концентрации 1000 мкг/см
Навеску витамина Е массой 0,1120 г в расчете на содержание чистого вещества помещают в круглодонную колбу со шлифом вместимостью 250 см и проводят омыление, экстракцию и обезвоживание по 7.2.5.
После выпаривания сухой остаток растворяют в 100 см гексана.
8.2.6.2 Приготовление градуировочных растворов -токоферола массовой концентрации 20, 100 и 500 мкг/см
В три мерные колбы вместимостью 50 см помещают 1; 5 и 25 см
раствора
-токоферола массовой концентрации 1000 мкг/см
, доводят объем раствора в колбах до метки гексаном и тщательно перемешивают.
Массовые концентрации -токоферола в растворах проверяют спектрофотометрически по 7.2.6 и вычисляют по формуле 1
.
8.2.7 Приготовление растворов витамина D
8.2.7.1 Приготовление раствора витамина D массовой концентрации 20000 МЕ/см
Навеску кристаллического эргокальциферола (холекальциферола) массой 0,100 г помещают в мерную колбу вместимостью 200 см, растворяют в гексане, объем раствора в колбе доводят до метки гексаном и тщательно перемешивают.
8.2.7.2 Приготовление градуировочных растворов витамина D массовой концентрации 50 и 100 МЕ/см
В две мерные колбы вместимостью 200 см помещают 0,5 и 1,0 см
раствора витамина D массовой концентрации 20000 МЕ/см
. Объемы растворов в колбах доводят до метки гексаном и тщательно перемешивают.
Оптическую плотность растворов измеряют на спектрофотометре при длине волны 265 нм в кювете толщиной поглощающего свет слоя 1 см относительно гексана.
Массовую концентрацию витамина D в растворе , МЕ/см
, вычисляют по формуле
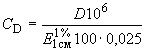 , (5)
, (5)
где - оптическая плотность раствора витамина D;
- коэффициент пересчета граммов в микрограммы;
- оптическая плотность раствора витамина D в гексане массовой концентрации 1 г в 100 см
раствора при длине волны 265 нм и толщине поглощающего свет слоя 1 см (для витамина
=465; для витамина
=500);
0,025 - коэффициент пересчета массы витамина D в ME, мкг/М
Е.
8.2.8 В растворы витаминов добавляют несколько кристаллов 2,6-ди-трет-бутил-п-крезола (бутиолокситолуола) и хранят в холодильнике не более 1 мес.
8.3 Проведение испытания
8.3.1 Омыление и экстракция
Навеску исследуемого продукта массой 5,00-10,00 г помещают в круглодонную колбу со шлифом вместимостью 250 см, добавляют 100-150 мг пирогаллола или гидрохинона (на кончике скальпеля) и соответственно 50-70 см
этилового спирта и 10-15 см
раствора гидроокиси калия массовой долей 50%. Дальнейшую процедуру омыления и экстракции проводят по 7.3.1. Сухой остаток витаминов растворяют в 4 см
гексана.
Примечание - Допускается для экстракции применять петролейный эфир.
8.3.2 Очистка раствора, полученного по 8.3.1, на колонке с окисью алюминия
8.3.2.1 Подготовка хроматографической колонки - по 7.3.2.
8.3.2.2 Элюирование витамина D
В колонку (8.3.2.1), не допуская высыхания верха колонки, вносят 4 см раствора (8.3.1) и промывают ее 20 см
петролейного эфира и 4 см
смеси петролейного и диэтилового эфира в объемном соотношении 1:1. Эту фракцию отбрасывают.
Витамин D элюируют 20 см смеси петролейного и диэтилового эфира в объемном соотношении 1:1. Элюат количественно переносят в коническую колбу вместимостью 50 см
и выпаривают досуха в водяной бане под током азота при температуре (60±2) °С.
Сухой остаток растворяют в 1 см гексана.
Полученный раствор (далее испытуемый раствор) используют для ВЭЖХ.
8.3.3 Подготовка жидкостного хроматографа к работе
Подготовку прибора осуществляют в соответствии с инструкцией по эксплуатации.
Перед началом работы колонку промывают элюентом при скорости его подачи 100-200 мкдм/мин в течение 5-10 мин.
8.3.4 Выполнение измерений на хроматографе "Милихром"
8.3.4.1 Условия проведения измерений
Измерения проводят в следующих условиях:
а) разделение компонентов проводят на колонке размером 64 (80, 120)х2 мм;
б) сорбент - Силосорб 600;
в) элюент - гексан-изопропиловый спирт в объемном соотношении 98,5:1,5 (98:2);
г) рабочие длины волн УФ-детектора - 264, 292 и 324 нм (соответственно для витаминов D, Е, А);
д) скорость элюирования - 150-200 мкдм/мин;
е) объем анализируемого раствора - 10-40 мкдм для витамина D и 4-5 мкдм
для витаминов А, Е.
8.3.4.2 Проведение измерений испытуемого раствора
Для измерений используют метод внешнего стандарта. В колонку хроматографа последовательно вводят равные объемы испытуемого и градуировочного растворов.
В качестве градуировочного выбирают раствор, высота пика которого наименее отличается от высоты пика испытуемого раствора.
Концентрация градуировочных растворов должна уточняться в день их использования по 8.2.5.2, 8.2.6.2 и 8.2.7.2.
Пик витамина на хроматограмме испытуемого раствора идентифицируют по времени удерживания.
Примеры хроматограмм экстрактов витаминов A, D, Е из белково-витаминно-минеральных добавок представлены в приложении А.
8.4 Обработка результатов
8.4.1 Содержание витаминов , витамина А - МЕ/кг, витамина Е - мг/кг, в испытуемой пробе вычисляют по формуле
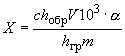 , (6)
, (6)
где - концентрация используемых градуировочных растворов, МЕ/см
(ретинол), мг/см
(
-токоферол);
- среднеарифметическое значение результатов измерений высоты (площади) пика испытуемого раствора для двух параллельных определений анализируемого компонента, мм или е.о.п.,
- объем разведения, см
(4 см
);
10 - коэффициент пересчета граммов в килограммы;
- коэффициент пересчета в ацетатную форму (для витамина А
=1,15, для витамина Е
=1,1);
- среднеарифметическое значение результатов измерений высоты (площади) пика градуировочного раствора для двух параллельных определений анализируемого компонента, мм или е.о.п.,
- масса навески испытуемой пробы, г.
Примечание - При расчете содержания витамина А высоты (площади) пиков испытуемого и градуировочного растворов рассчитывают как сумму высот (площадей) цис- и транс-формы р
етинола.
8.4.2 Содержание витамина D , МЕ/кг, в испытуемой пробе вычисляют по формуле
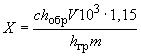 , (7)
, (7)
где - концентрация используемого градуировочного раствора, МЕ/см
;
- среднеарифметическое значение результатов измерений высоты (площади) пика испытуемого раствора для двух параллельных анализов, мм или е.о.п.;
- объем разведения, см
(4 см
);
10 - коэффициент пересчета граммов в килограммы;
1,15 - коэффициент, учитывающий превращение витамина D в провитамин; - среднеарифметическое значение результатов измерений высоты (площади) пика градуировочного раствора для двух параллельных анализов, мм или е.о.п;
- масса навески испытуемой пробы, г.
При определении витамина D, если в качестве градуировочного вещества используют эргокальциферол (витамин ), то числитель в формуле дополнительно умножают на коэффициент 0
,97.
8.4.3 Результаты вычисляют до третьей значащей цифры и округляют до двух значащих цифр.
8.4.4 Контроль сходимости результатов параллельных определений и представление результатов по 7.4.4.
9 Контроль точности испытаний
9.1 Контроль сходимости результатов параллельных определений - по 7.4.4.
9.2 Для контроля воспроизводимости используют рабочие пробы. Каждую пробу делят на две равные части и анализируют в соответствии с методикой настоящего стандарта, получают два результата испытаний в разных лабораториях или в одной, но выполненные разными исполнителями на разном оборудовании с использованием реактивов разных партий в разное время. Воспроизводимость считают удовлетворительной, если ![]() , где
, где ,
и
- результаты испытаний одной и той же пробы, полученные в двух разных лабораториях или в разных условиях в одной лаборатории, и их среднеарифметическое значение. Значение
приведено в таблице 2.
9.3 Контроль точности выполняют методом добавок. Рабочую пробу делят на две равные части, первую из которых анализируют в соответствии с методикой, а во вторую вводят известную добавку витамина и затем анализируют в соответствии с методикой настоящего стандарта. Значение добавки должно составлять 50%-150% содержания витамина в испытуемой пробе. Точность контрольных испытаний признают удовлетворительной, если ![]() , где
, где ,
и
- результаты контрольных испытаний пробы с добавкой, без добавки и значение добавки. Значение норматива
для вероятности
=0,90 вычисляют по формуле
![]() , (8)
, (8)
где и
- значения погрешности результатов анализа пробы без добавки и пробы с добавкой, вычисленные по 7.4.4.
Пример - Проведен анализ пробы с добавкой (=40 МЕ/кг) и без добавки (
=30 МЕ/кг) на содержание витамина А. Значение добавки составляет
=20 МЕ/кг, значение относительной погрешности
=25%. Результат контрольного анализа равен:
![]() .
.
Норматив контроля точности находят по формуле
![]()
Анализ выполнен с достаточной точностью, так как результат контрольного анализа меньше норматива контроля точности (10<10,5).
ПРИЛОЖЕНИЕ А (справочное). Хроматограммы экстрактов витаминов A, D, Е
ПРИЛОЖЕНИЕ А
(справочное)
Рисунок А.1 - Хроматограмма экстракта витамина А
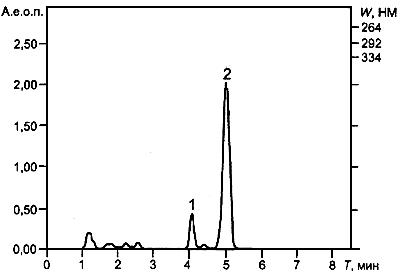
Рисунок А.1 - Хроматограмма экстракта витамина А:
1 - цис-форма, 2 - транс-форма
Рисунок А.2 - Хроматограмма экстракта витамина D
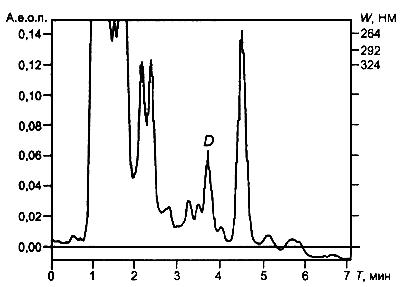
Рисунок А.2 - Хроматограмма экстракта витамина D
Рисунок А.3 - Хроматограмма экстракта витамина Е
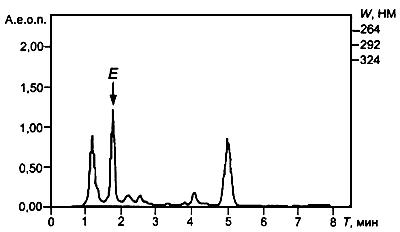
Рисунок А.3 - Хроматограмма экстракта витамина Е
ПРИЛОЖЕНИЕ Б (справочное). Библиография
ПРИЛОЖЕНИЕ Б
(справочное)
[1] ПБ 10-115-96 Правила устройства и безопасной эксплуатации сосудов, работающих под давлением
[2] ТУ 25-1819.0021-90 Секундомеры механические "Слава"
[3] ТУ 64-1.1411-76 Шкаф сушильный
[4] ТУ 6-09-1678-86 Фильтры обеззоленные (белая, красная, синяя ленты)
[5] ГФ СССР-X ст.695 Токоферола-ацетат
[6] ТУ 84-11-99-89 Этиловый абсолютированный спирт
[7] МРТУ 6-09-426-70 Алюминия окись безводная
[8] ГФ СССР-X ст.6 Кислота аскорбиновая
[9] ТУ 6-09-53-60-87 Фенолфталеин (индикатор)
[10] Воскресенский П.И. Техника лабораторных работ. Химия М., 1969, стр.490
[11] ГФ СССР-X ст.579 Раствор ретинола-ацетата в масле 3,44%
[12] ФС 42-1764-96 Эргокальциферол кристаллический
[13] ФС 421046299 Витамин 1000000 МЕ/г субстанция (производитель "Хоффманн-Ля Рош", Швейцария)
[14] ТУ 6.09-402-87 2-пропанол (изопропиловый спирт химически чистый)
[15] ТУ 6-09-3375-78 Гексан
[16] ТУ 6-09-3916-85 Окись алюминия для хроматографии
[17] ТУ 6.09-10-9954-74 2,6-Ди-трет-бутил-п-крезол
Текст документа сверен по:
официальное издание
М.: ИПК Издательство стандартов, 2004
