ГОСТ 33978-2016
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ И КОМБИКОРМА
Метод определения содержания тиреостатиков с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Food products and mixed feeds. Method for determination of thyreostats by high performance liquid chromatography - mass spectrometry
МКС 65.120
67.050
67.120
Дата введения 2018-01-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГБУ "ВГНКИ")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 25 октября 2016 г N 92-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 14 марта 2017 г. N 139-ст межгосударственный стандарт ГОСТ 33978-2016 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2018 г.
5 ВВЕДЕН ВПЕРВЫЕ
6 ПЕРЕИЗДАНИЕ. Ноябрь 2019 г.
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
ВНЕСЕНЫ: поправка, опубликованная в ИУС N 4, 2020 год; поправка, опубликованная в ИУС № 6, 2024 год, введенная в действие с 05.03.2024
Поправки внесены изготовителем базы данных
ВНЕСЕНО Изменение N 1, утвержденное и введенное в действие приказом Федерального агентства по техническому регулированию и метрологии от 12.12.2023 № 1558-ст c 15.03.2024
Изменение N 1 внесено изготовителем базы данных по тексту ИУС № 3, 2024
1 Область применения
Настоящий стандарт распространяется на непереработанные пищевые продукты - мясо (в том числе мясо птицы), субпродукты (печень), комбикорма, а также на мочу животных и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (далее - ВЭЖХ-МС/МС) для определения содержания тиреостатиков. Диапазон измерений содержания 6-пропил-2-тиоурацила, 6-метил-2-тиоурацила, 2-тиоурацила, 6-фенил-2-тиоурацила составляет от 2,0 до 30,0 мкг/кг, диапазон измерений содержания 2-меркаптобензимидазола составляет от 0,4 до 30,0 мкг/кг.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.2.085 Арматура трубопроводная. Клапаны предохранительные. Выбор и расчет пропускной способности
ГОСТ OIML R 76-1 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2603 Реактивы. Ацетон. Технические условия
ГОСТ 3118 Реактивы. Кислота соляная. Технические условия
ГОСТ 4198 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4328 Реактивы. Натрия гидроокись. Технические условия
ГОСТ ИСО 5725-6 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике**
________________
** В Российской Федерации действует ГОСТ Р ИCO 5725-6-2002.
Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
ГОСТ ISO 6497 Корма. Отбор проб
ГОСТ 6995 Реактивы. Метанол-яд.Технические условия
ГОСТ 7269 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9968 Метилен хлористый технический. Технические условия
ГОСТ 22300 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
ГОСТ 25336 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 28311 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29227 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31467 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов и классификаторов на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации (www.easc.by) или по указателям национальных стандартов, издаваемым в государствах, указанных в предисловии, или на официальных сайтах соответствующих национальных органов по стандартизации. Если на документ дана недатированная ссылка, то следует использовать документ, действующий на текущий момент, с учетом всех внесенных в него изменений. Если заменен ссылочный документ, на который дана датированная ссылка, то следует использовать указанную версию этого документа. Если после принятия настоящего стандарта в ссылочный документ, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение применяется без учета данного изменения. Если ссылочный документ отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
(Измененная редакция, Изм. N 1).
3 Сущность метода
Метод основан на экстракции тиреостатиков из анализируемой пробы, дериватизации и очистки методом твердофазной экстракции, с последующим их количественным определением методом ВЭЖХ-МС/МС в режиме мониторинга множественных реакций (MRM). Количественное определение тиреостатиков проводят методом внутреннего стандарта.
4 Требования безопасности и условия выполнения измерений
4.1 Применяемые в работе реактивы относятся к веществам 1-го и 2-го класса опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.3 Приготовление градуировочных растворов проводят в вытяжном шкафу.
4.4 При выполнении измерений с использованием жидкостного хроматографа соблюдают правила по электробезопасности по ГОСТ 12.1.019 и правила безопасной эксплуатации сосудов, работающих под давлением по ГОСТ 12.2.085.
4.5 К выполнению измерений методом ВЭЖХ-МС/МС допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации применяемой аппаратуры.
4.6 При выполнении измерений соблюдают следующие условия:
- температура окружающего воздуха | от 15°С до 30°С; |
- относительная влажность воздуха | от 20% до 80%. |
(Измененная редакция, Изм. N 1).
4.7 Утилизацию отходов проб и реактивов осуществляют в соответствии с требованиями нормативных документов, действующих на территории государства, принявшего настоящий стандарт.
(Введено дополнительно, Изм. N 1).
5 Средства измерений, аппаратура, материалы, посуда и реактивы
5.1 Для определения содержания тиреостатиков применяют следующие средства измерений, аппаратуру, посуду и материалы:
- весы высокого (II) класса точности по ГОСТ OIML R 76-1 с поверочным интервалом (e) не более 0,1 г и действительной ценой деления (d) не более 0,01 г;
- весы специального (I) класса точности по ГОСТ OIML R 76-1 с поверочным интервалом (e) не более 1 мг и действительной ценой деления (d) не более 0,1 мг;
- масс-спектрометр, оснащенный источником ионизации с электрораспылением, квадрупольными анализаторами, с диапазоном измерений от 25 до 1050 атомных единиц массы (а.е.м.) и относительным средним квадратическим отклонением выходного сигнала по площади пика не более 10%, с режимом получения и анализа фрагментных ионов (режим МС/МС);
- систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем, системы фильтрования и дегазации подвижных фаз, термостата хроматографической колонки, обеспечивающего температуру нагрева не менее 40°C;
- рН-метр или универсальный иономер диапазоном измерения от 4 до 9 ед. рН с погрешностью измерения ±0,05 ед. рН;
- баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм;
- встряхиватель (шейкер) для пробирок вибрационного, ротационного, линейного или орбитального типа;
- измельчитель-гомогенизатор лабораторный;
- камеру лабораторную морозильную с цифровым контроллером температуры и рабочим диапазоном температур от минус 15°С до минус 25°С;
- колонку хроматографическую длиной 150 мм и диаметром 2,1 мм с обращенно-фазным сорбентом С18, и диаметром частиц сорбента не более 5,0 мкм*;
______________
* Допускается применение хроматографических колонок, заполненных обращенно-фазным сорбентом С8 или С18 с диаметром частиц не более 5 мкм, длиной не менее 50 мм.
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов измерений, аттестованным в установленном порядке;
- модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом, позволяющий проводить концентрирование при температуре до 50°C;
- систему получения деионизированной воды высокой чистоты с удельным сопротивлением 18 МОм·см;
- устройство вакуумное для твердофазной экстракции;
- холодильник бытовой с морозильной камерой, цифровым контроллером температуры и рабочим диапазоном температур от 2°С до 8°С;
- центрифугу лабораторную рефрижераторную с центробежным ускорением не менее 3500 g и диапазоном температур от 4°С до 20°С;
- шкаф сушильный;
- картриджи готовые или набивные для твердофазной экстракции вместимостью не менее 12 см, заполненные 0,5 г силикагеля с диаметром частиц от 15 до 100 мкм;
- пробы, не содержащие тиреостатиков, подготовленные и проанализированные ранее в соответствии с требованиями разделов 7 и 8, в зависимости от типа исследуемой матрицы ("чистые" пробы)*;
________________
* Срок хранения "чистых" проб при температуре от минус 15°С до минус 25°С - не более трех месяцев.
- виалы (флаконы) стеклянные вместимостью 2 см с завинчивающимися крышками и тефлоновыми прокладками;
- виалы или пробирки полипропиленовые вместимостью 15 и 50 см с завинчивающимися крышками;
- колбы 2-10-2 по ГОСТ 1770;
- колбы 1-100(1000)-2 по ГОСТ 1770;
- колбы конические Кн-1-250(500, 1000)-29/32 ТС по ГОСТ 25336;
- пипетки 2-2-1-5(10, 25) по ГОСТ 29227;
- дозаторы механические одноканальные переменной вместимости 20-200, 100-1000 мм![]() по ГОСТ 28311;
по ГОСТ 28311;
- цилиндры 1-50(100,1000)-2 по ГОСТ 1770;
- систему получения инертного газа для концентрирования жидкостей.
(Поправка. ИУС N 4-2020), (Измененная редакция, Изм. N 1), (Поправка. ИУС № 6-2024).
5.2 При определении содержания тиреостатиков применяют следующие реактивы:
- 3-йодбензилбромид, ч.д.а.;
- ацетон по ГОСТ 2603;
- воду деионизированную для ВЭЖХ, полученную с использованием системы производства ультрачистой воды;
- дихлорметан по ГОСТ 9968, х.ч.;
- калия дигидрофосфат по ГОСТ 4198, ч.д.а.;
- кислоту соляную по ГОСТ 3118, х.ч.;
- метанол по ГОСТ 6995, х.ч.;
- натрия гидроксид по ГОСТ 4328, ч.д.а.;
- натрия гидрофосфат дигидрат, ч.д.а.;
- н-гексан, х.ч.;
- этилацетат по ГОСТ 22300, ч.д.а.;
- эфир диэтиловый, х.ч.
(Измененная редакция, Изм. N 1).
5.3 При определении содержания тиреостатиков в качестве образцов сравнения* применяют соединения с массовой долей основного вещества не менее 98,0%.
______________
* Допускается использовать в качестве образцов сравнения соединения с меньшей массовой долей основного вещества.
(Измененная редакция, Изм. N 1).
5.3.1 Для приготовления исходных растворов:
- 2-меркаптобензимидазол;
- 2-тиоурацил;
- 6-метил-2-тиоурацил;
- 6-пропил-2-тиоурацил;
- 6-фенил-2-тиоурацил.
5.3.2 Для приготовления исходного раствора внутреннего стандарта:
- 5,6-диметил-2-тиоурацил.
5.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также аппаратуры, реактивов и материалов по качеству не хуже вышеуказанных.
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и реактивов
6.1.1 Мойку и сушку посуды проводят в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.1.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.1.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105°С до 110°С.
6.1.4 Каждую новую партию реактивов проверяют на отсутствие контаминации анализируемыми соединениями путем проведения холостого опыта в соответствии с процедурой анализа.
6.2 Приготовление растворов
6.2.1 Приготовление раствора метанол - деионизированная вода в объемном соотношении 2:1
В коническую колбу вместимостью 250 см вносят 100 см
метанола и 50 см
деионизированной воды, перемешивают.
Срок хранения раствора при комнатной температуре - не более трех месяцев.
6.2.2 Приготовление раствора метанол - деионизированная вода в объемном соотношении 4:1
В коническую колбу вместимостью 250 см вносят 200 см
метанола и 50 см
деионизированной воды, перемешивают.
Срок хранения раствора при комнатной температуре - не более трех месяцев.
6.2.3 Приготовление раствора натрия гидрофосфата молярной концентрации 0,2 моль/дм
В мерную колбу вместимостью 1000 см вносят 35,6 г натрия гидрофосфат дигидрата, доводят объем до метки деионизированной водой.
Срок хранения раствора при комнатной температуре - не более одного месяца.
6.2.4 Приготовление раствора калия дигидрофосфата молярной концентрации 0,2 моль/дм
В мерную колбу вместимостью 1000 см вносят 27,2 г калия дигидрофосфата, доводят объем до метки деионизированной водой.
Срок хранения раствора при комнатной температуре - не более одного месяца.
6.2.5 Приготовление фосфатного буферного раствора с рН 8,0 ед. рН
В конической колбе вместимостью 1000 см смешивают 945 см
раствора гидрофосфата натрия (см. 6.2.3) и 55 см
раствора дигидрофосфата калия (см. 6.2.4). Измеряют рН, устанавливают его значение до (8,0±0,1) ед. рН раствором гидроксида натрия (см. 6.2.9) или раствором соляной кислоты (см. 6.2.10).
Срок хранения раствора при комнатной температуре - не более одного месяца.
6.2.6 Приготовление раствора 3-йодбензилбромида массовой концентрацией 5 мг/см
В мерную колбу вместимостью 10 см вносят 50,0 мг 3-йодбензилбромида, доводят объем раствора метанолом до верхней метки на колбе.
Срок хранения раствора при температуре от 2°С до 8°С - не более одних суток.
6.2.7 Приготовление раствора дихлорметан - гексан в объемном соотношении 1:3
В коническую колбу вместимостью 500 см вносят 100 см
дихлорметана и 300 см
гексана, перемешивают.
Срок хранения раствора при комнатной температуре - не более трех месяцев.
6.2.8 Приготовление раствора этилацетат - гексан в объемном соотношении 2:3
В коническую колбу вместимостью 500 см вносят 200 см
этилацетата и 300 см
гексана, перемешивают.
Срок хранения раствора при комнатной температуре - не более трех месяцев.
6.2.9 Приготовление раствора натрия гидроксида с концентрацией 1 моль/дм
В мерную колбу вместимостью 100 см вносят 90 см
деионизированной воды и 4,0 г гидроксида натрия, перемешивают, после чего объем в колбе доводят до метки деионизированной водой.
Срок хранения раствора при комнатной температуре - не более трех месяцев.
6.2.10 Приготовление раствора соляной кислоты с концентрацией 1 моль/дм
В мерную колбу вместимостью 100 см вносят 90 см
деионизированной воды и с помощью пипеточного дозатора добавляют 8,6 см
концентрированной соляной кислоты, после чего объем в колбе доводят до метки деионизированной водой и перемешивают.
Срок хранения раствора при комнатной температуре - не более трех месяцев.
6.3 Приготовление градуировочных растворов
6.3.1 Приготовление исходных стандартных растворов тиреостатиков массовыми концентрациями 1000 мкг/см (растворы
)
Готовят индивидуальные исходные стандартные растворы каждого тиреостатика концентрациями , равными 1000 мкг/см
каждый.
Для приготовления исходного стандартного раствора i-го тиреостатика в отдельную мерную колбу вместимостью 10 см помещают рассчитанную массу соответствующего химического вещества, эквивалентную 10 мг чистого тиреостатика, взвешенную с точностью до 0,1 мг. Добавляют 8 см
раствора метанол - деионизированная вода (см. 6.2.1) и помещают в ультразвуковую баню на 10 мин, затем доводят объем полученного раствора при температуре (20±2)°С до 10 см
этим же растворителем по метке на колбе.
Массу i-го химического вещества эквивалентную 10 мг i-го тиреостатика рассчитывают по формуле
![]() , (1)
, (1)
где С - концентрация стандартного раствора, мкг/см;
V - объем исходного стандартного раствора, см;
- массовая доля i-го тиреостатика в химическом веществе, %;
0,001 - коэффициент пересчета массы из мкг в мг.
Срок хранения растворов при температуре от минус 15°С до минус 25°С - не более одного года.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.3.2 Приготовление рабочих стандартных растворов тиреостатиков массовыми концентрациями 2 мкг/см (раствор
) и 0,04 мкг/см
(раствор
)
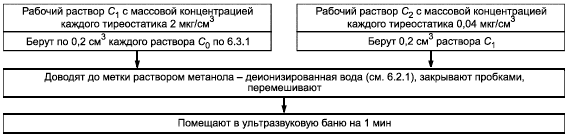
Рабочие стандартные растворы ,
готовят в мерных колбах вместимостью 10 см
согласно рисунку 1.
|
Рисунок 1 - Приготовление рабочих растворов ,
Раствор хранят при температуре от минус 15°С до минус 25°С - не более одного года.
Перед применением раствор выдерживают при комнатной температуре в темном месте не менее 30 мин.
Раствор хранят при температуре от 2°С до 8°С в течение одних суток.
6.3.3 Приготовление исходного раствора внутреннего стандарта тиреостатиков массовой концентрацией 200 мкг/см (раствор
)
В мерную колбу вместимостью 10 см вносят рассчитанную по формуле (1) массу 5,6-диметил-2-тиоурацила эквивалентную 2 мг основного вещества, взвешенную с точностью до 0,1 мг. Добавляют 8 см
раствора метанол - деионизированная вода (см. 6.2.1) и помещают в ультразвуковую баню на одну минуту, затем доводят объем полученного раствора при температуре (20±2)°С этим же растворителем до 10 см
по метке на колбе.
Раствор хранят при температуре от минус 15°С до минус 25°С. Срок годности - не более одного года.
Перед применением раствор выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.3.4 Приготовление рабочего раствора внутреннего стандарта тиреостатиков массовой концентрацией 1 мкг/см (раствор
)
Для приготовления рабочего раствора в мерную колбу вместимостью 10 см
переносят 0,05 см
раствора
, доводят до метки раствором метанол - деионизированная вода (см. 6.2.1), закрывают пробкой и перемешивают.
Раствор хранят при температуре от минус 15°С до минус 25°С. Срок годности - не более шести месяцев.
Перед применением раствор выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.3.5 Приготовление матричных градуировочных растворов тиреостатиков (растворы ![]() )
)
Матричные градуировочные растворы ![]() готовят в виалах или пропиленовых пробирках вместимостью 50 см
готовят в виалах или пропиленовых пробирках вместимостью 50 см из "чистых" проб массой 2,00 г, в которые вносят раствор внутреннего стандарта
и рабочие растворы определяемых тиреостатиков
,
в соответствии с таблицей 1.
Таблица 1 - Приготовление матричных градуировочных растворов ![]()
Обозначение и массовая концентрация приготовляемого матричного | Вносимый объем рабочего раствора, см | ||
градуировочного раствора |
|
|
|
| 0,03 | - | 0,04 |
| - | 0,80 | |
| - | 0,40 | |
| - | 0,10 | |
| - | 0,02 | |
Таблица 1 (Измененная редакция, Изм. N 1).
Виалы (пробирки) встряхивают в шейкере в течение одной минуты и проводят дальнейшую обработку проб согласно разделу 7.
Срок хранения растворов ![]() при температуре от 2°С до 8°С не более 24 ч.
при температуре от 2°С до 8°С не более 24 ч.
(Измененная редакция, Изм. N 1).
7 Отбор и подготовка проб
7.1 Отбор проб
7.1.1 Отбор проб мяса, печени - по ГОСТ 7269.
7.1.2 Отбор проб мяса птицы, печени - по ГОСТ 31467.
7.1.3 Объем отбираемых проб мочи должен быть не менее 40 см.
7.1.4 Отбор проб комбикормов - по ГОСТ ISO 6497.
7.1.5 Пробы, отобранные по 7.1.1 и 7.1.2, при отсутствии возможности проведения анализа в день отбора замораживают и хранят при температуре минус 25°С до проведения испытания, но не более 90 сут.
7.2 Подготовка проб
Мышечную ткань предварительно очищают от грубой соединительной ткани. Обработку анализируемой пробы проводят в соответствии с рисунком 2.
|
Рисунок 2 - Подготовка проб мяса, включая мясо птицы, печени, комбикормов, мочи
7.3 Очистка подготовленных проб методом твердофазной экстракции
Картриджи для твердофазной экстракции кондиционируют на вакуумном устройстве для ТФЭ, пропуская 10 см гексана. Затем через картридж пропускают пробу, полученную в соответствии с 7.2. Промывают картридж 5 см
гексана. Определяемые вещества элюируют с сорбента 10 см
раствора этилацетат - гексан (см. 6.2.8) в виалу или полимерную пробирку вместимостью 15 см
. Упаривают элюат досуха на системе упаривания растворителей при температуре не более 40°С. Остаток перерастворяют в 1 см
раствора метанол - деионизированная вода (см. 6.2.2), помещают в ультразвуковую баню при комнатной температуре на одну минуту и центрифугируют при 3500 g в течение 15 мин при температуре 4°С. Переносят экстракт в стеклянную виалу вместимостью 2 см
и используют для ВЭЖХ-МС/МС анализа.
8 Порядок выполнения анализа
8.1 Условия ВЭЖХ-МС/МС измерений
8.1.1 Хромато-масс-спектрометр включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры рабочих режимов масс-спектрометрического детектирования и хроматографического разделения.
8.1.2 Для колонки диаметром 2,1 мм, длиной 150 мм, с обращенно-фазным сорбентом С18 с размером частиц не более 5,0 мкм, соблюдают следующие условия хроматографирования:
- температура колонки - 40°С;
- скорость потока подвижной фазы - 0,2 см/мин;
- объем вводимой пробы - 20 мм.
Разделение проводят в режиме градиентного элюирования (в качестве подвижной фазы А используют деионизированную воду, подвижной фазы Б - метанол) в соответствии с таблицей 2.
Таблица 2 - Условия градиентного элюирования
Время, мин | Подвижная фаза А, % | Подвижная фаза Б, % |
0,0 | 25 | 75 |
11,0 | 15 | 85 |
13,0 | 15 | 85 |
13,1 | 25 | 75 |
23,0 | 25 | 75 |
8.1.3 Параметры воздействия на ионы в режиме мониторинга множественных реакций (MRM) приведены в таблице 3.
Таблица 3 - Параметры воздействия на ионы в режиме MRM при ионизации электрораспылением с регистрацией отрицательных ионов
Тиреостатик | Ион- | Ион- | Потенциал декласте- | Энергия соударений, эВ | Ускоряющее напряжение на выходе из ячейки столкновений, В |
2-Тиоурацил | 343 | 126,9 | -80 | -28 | -11 |
343 | 94,9 | -80 | -27 | -11 | |
6-Метил-2-тиоурацил | 357 | 126,9 | -80 | -30 | -11 |
357 | 108,9 | -80 | -27 | -11 | |
2-Меркаптобензимидазол | 365 | 147,9 | -80 | -30 | -11 |
365 | 103,9 | -80 | -53 | -11 | |
6-Пропил-2-тиоурацил | 385 | 126,9 | -80 | -30 | -11 |
385 | 350,9 | -80 | -25 | -11 | |
6-Фенил-2-тиоурацил | 419 | 170,9 | -80 | -30 | -11 |
419 | 126,9 | -80 | -35 | -11 | |
5,6-Диметил-2-тиоурацил* | 371 | 126,9 | -80 | -30 | -11 |
371 | 153,9 | -80 | -34 | -11 | |
* Внутренний стандарт. | |||||
Примечание - Приведенные параметры хроматографического разделения и масс-спектрометрического детектирования могут отличаться в зависимости от используемого оборудования.
8.1.4 Параметры источника ионизации и квадрупольного анализатора:
- напряжение на распыляющем капилляре (IS) минус 4500 В при регистрации отрицательных ионов;
- разрешение квадруполей Q1/Q3 - единичное;
- давление газа для фрагментации (CAD) - 41 кПа.
8.1.5 Контроль чувствительности методики осуществляют введением 20 мм матричных градуировочных растворов
и
(см. 6.3.5) в инжектор хроматографа. При анализе раствора
полученное соотношение сигнал/шум для каждого тиреостатика, за исключением 2-меркаптобензимидазола, должно быть не менее 3. При анализе раствора G
полученное соотношение сигнал/шум для 2-меркаптобензимидазола должно быть не менее 3.
8.2 Построение градуировочных графиков и проведение измерений
8.2.1 ВЭЖХ-МС/МС анализ выполняют в виде серии измерений, включающей следующие образцы:
- образец подвижной фазы А - для уравновешивания ВЭЖХ-МС/МС системы;
- чистую пробу;
- градуировочные растворы (см. 6.3.5);
- экстракты анализируемых проб, приготовленных по 7.2.
8.2.2 Определяют и регистрируют на хроматограмме времена удерживания пиков двух ионов-продуктов каждого тиреостатика, соответствующее времени удерживания, найденному при измерении градуировочных растворов в условиях по 8.1.1, 8.2.1. Проводят измерения градуировочных растворов, приготовленных по 6.3.5, в порядке возрастания их концентраций. Для построения градуировочного графика 2-меркаптобензимидазола используют данные анализа градуировочных растворов ![]() ; для построения градуировочных графиков других тиреостатиков используют данные анализа растворов
; для построения градуировочных графиков других тиреостатиков используют данные анализа растворов ![]() .
.
(Измененная редакция, Изм. N 1).
8.2.3 Вычисление площади пика проводят для каждого иона-продукта анализируемых тиреостатиков и их внутреннего стандарта. Количественное определение каждого тиреостатика проводят по одному, наиболее интенсивному, иону-продукту.
Для подтверждения достоверности определения аналитов при анализе градуировочных растворов для каждого тиреостатика определяют значение отношения площади пика менее интенсивного иона-продукта к площади пика более интенсивного иона-продукта - относительную ионную интенсивность. Значение отклонений относительных ионных интенсивностей, полученные в экстрактах анализируемых проб, не должны превышать установленных по градуировочным растворам значений более, чем указано в таблице 4.
Таблица 4 - Допустимые отклонения относительных ионных интенсивностей
Относительная ионная интенсивность, % от основного пика | Максимально допустимые отклонения для ВЭЖХ-МС/МС детектирования, % |
Св. 50 | ±20 |
Св. 20 до 50 включ. | ±25 |
Св. 10 до 20 включ. | ±30 |
Менее 10 включ. | ±50 |
8.2.4 Построение градуировочных графиков проводят в каждой серии анализов с помощью программного обеспечения хромато-масс-спектрометра.
При построении градуировочной характеристики используют линейную регрессию вида у=а+bх (где y является отношением площади пика аналита к площади пика внутреннего стандарта, х - отношением концентраций аналита и внутреннего стандарта), при этом коэффициент корреляции должен быть не менее 0,98.
8.2.5 Построение линейного градуировочного графика и расчет содержания тиреостатиков в анализируемых пробах выполняется системой обработки данных в автоматическом режиме.
8.2.6 Градуировочную характеристику считают приемлемой, если рассчитанное с помощью компьютерной системы обработки данных значение коэффициента корреляции (коэффициент регрессии) каждого тиреостатика 0,98, а значения отклонения содержания массовой доли определяемых соединений, рассчитанные по формуле (2), для каждой точки градуировочной характеристики не превышают 20%:
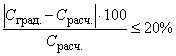 , (2)
, (2)
где С - содержание определяемого соединения, найденное по градуировочной характеристике, мкг/кг,
С - содержание определяемого соединения в градуировочном растворе, мкг/кг.
9 Метрологические характеристики
Установленный в настоящем стандарте метод обеспечивает выполнение измерений содержания тиреостатиков с расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата k=2 и доверительной вероятности Р=0,95, указанной в таблице 5.
Таблица 5 - Показатели точности метода при проведении измерений содержания тиреостатиков
Тиреостатик | Диапазон измерений содержания, мкг/кг | Значение относи- | Пока- | Предел повто- | Показатель воспроиз- |
6-Пропил-2-тиоурацил | От 2,0 до 15,0 включ. | 63 | 22 | 61 | 32 |
Св. 15,0 до 30,0 включ. | 30 | 10 | 28 | 15 | |
6-Метил-2-тиоурацил | От 2,0 до 30,0 включ. | 32 | 12 | 33 | 16 |
2-Меркапто-бензими- дазол | От 0,4 до 8,0 включ. | 59 | 21 | 58 | 28 |
Св. 8,0 до 30,0 включ. | 37 | 13 | 36 | 16 | |
2-Тиоурацил | От 2,0 до 8,0 включ. | 69 | 30 | 83 | 35 |
Св. 8,0 до 30,0 включ. | 33 | 14 | 39 | 15 | |
6-Фенил-2-тиоурацил | От 2,0 до 8,0 включ. | 63 | 21 | 58 | 32 |
Св. 8,0 до 30,0 включ. | 43 | 15 | 42 | 22 |
10 Обработка результатов измерений
10.1 Расчет содержания i-го тиреостатика, мкг/кг, выполняется в автоматическом режиме с помощью программного обеспечения хромато-масс-спектрометра по формуле
![]() , (3)
, (3)
где - концентрация i-го тиреостатика в анализируемой пробе, найденная по градуировочному графику, нг/см
;
- объем разведения сухого остатка, см
;
- масса навески анализируемой пробы, г.
10.2 За результат измерений принимают среднеарифметическое значение результатов двух параллельных определений, если выполняется условие приемлемости:
![]() , (4)
, (4)
где ,
- результаты параллельных определений содержания тиреостатика, мкг/кг;
r - значение предела повторяемости, % (в соответствии с таблицей 5).
10.3 Если условие (4) не выполняется, получают еще два результата в полном соответствии с данной методикой измерений. За результат измерений принимают среднеарифметическое значение результатов четырех определений, если выполняется условие:
![]() , (5)
, (5)
где ,
- максимальное и минимальное значения из полученных четырех результатов параллельных определений содержания тиреостатика, мкг/кг;
![]() - значение критического диапазона для уровня вероятности Р=0,95 и n-результатов определений.
- значение критического диапазона для уровня вероятности Р=0,95 и n-результатов определений.
![]() ,
,
для n=4
![]() , (6)
, (6)
где - показатель повторяемости, % (в соответствии с таблицей 5).
10.4 Если условие (5) не выполняется, выясняют причины превышения критического диапазона, устраняют их и повторяют выполнение измерений в соответствии с требованиями методики измерений.
11 Оформление результатов измерений
Содержание i-го тиреостатика, мкг/кг, представляют в виде
![]() , при Р=0,95, (7)
, при Р=0,95, (7)
где - среднее арифметическое значение вычислений двух параллельных измерений содержания i-го тиреостатика в анализируемой пробе (см. 10.2), мкг/кг;
- значение относительной расширенной неопределенности содержания i-го аналита для соответствующего диапазона измерений, % (в соответствии с таблицей 5);
![]() - значение расширенной неопределенности в абсолютных единицах, мкг/кг.
- значение расширенной неопределенности в абсолютных единицах, мкг/кг.
Числовое значение результата измерений должно оканчиваться цифрой того же разряда, что и значение расширенной неопределенности, содержащее не более двух значащих цифр.
В случае необходимости допускается представление результата измерений в мг/кг путем деления значения содержания i-го тиреостатика, полученного в соответствии с 10.1, и значения расширенной неопределенности ![]() в абсолютных единицах (мкг/кг) на 1000 (с сохранением количества значащих цифр).
в абсолютных единицах (мкг/кг) на 1000 (с сохранением количества значащих цифр).
(Измененная редакция, Изм. N 1).
12 Контроль стабильности результатов измерений
Контроль стабильности результатов измерений осуществляют в соответствии с документами, утвержденными в лаборатории. Рекомендуется использование контрольных карт Шухарта в соответствии с ГОСТ ИСО 5725-6*.
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
(Измененная редакция, Изм. N 1).
УДК 636.085:637.071:006.354 | МКС 65.120 |
67.050 | |
67.120 | |
Ключевые слова: пищевые продукты, комбикорма, моча животных, тиреостатики, метод определения содержания тиреостатиков с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием | |
Редакция документа с учетом
изменений и дополнений подготовлена