ГОСТ 34535-2019
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ, КОРМА, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ
Метод определения содержания кокцидиостатиков с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Food products, feeds, food raw materials. Method for determination of coccidiostats by high performance liquid chromatography - mass spectrometry
МКС 65.120
67.050
67.100.10
67.120.10
67.120.20
67.120.30
Дата введения 2020-04-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГБУ "ВГНКИ")
2 ВНЕСЕН Межгосударственным техническим комитетом по стандартизации МТК 335 "Методы испытаний агропромышленной продукции на безопасность"
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 июля 2019 г. N 120-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Киргизия | KG | Кыргызстандарт |
Молдова | MD | Институт стандартизации Молдовы |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
(Поправка. ИУС N 4-2020), (Поправка. ИУС N 8-2020).
4 Приказом Федерального агентства по техническому регулированию и метрологии от 27 августа 2019 г. N 528-ст межгосударственный стандарт ГОСТ 34535-2019 введен в действие в качестве национального стандарта Российской Федерации с 1 апреля 2020 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
ВНЕСЕНЫ: поправка, опубликованная в ИУС N 4, 2020 год; поправка, опубликованная в ИУС N 8, 2020 год; поправка, опубликованная в ИУС N 11, 2020 год
Поправки внесены изготовителем базы данных
ВНЕСЕНО Изменение N 1, утвержденное и введенное в действие приказом Федерального агентства по техническому регулированию и метрологии от 12.12.2023 № 1561-ст c 15.03.2024
Изменение N 1 внесено изготовителем базы данных по тексту ИУС № 3, 2024
1 Область применения
Настоящий стандарт распространяется на пищевые продукты и продовольственное сырье - молоко, сухие молочные продукты, яйца, яичный порошок, яичный меланж, мясо и мясные продукты, субпродукты (все виды животных), мясо и субпродукты птицы, рыбу, а также комбикорма и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором (ВЭЖХ-МС/МС) для определения содержания кокцидиостатиков.
Диапазон измерений - от 1,0 до 1000,0 мкг/кг.
(Измененная редакция, Изм. N 1).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.018 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.2.085 Арматура трубопроводная. Клапаны предохранительные. Выбор и расчет пропускной способности
ГОСТ OIML R 76-1 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2603 Реактивы. Ацетон. Технические условия
ГОСТ 4288 Изделия кулинарные и полуфабрикаты из рубленого мяса. Правила приемки и методы испытаний
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике*
________________
* В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002.
ГОСТ 5848 Реактивы. Кислота муравьиная. Технические условия
ГОСТ 6995 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9792 Колбасные изделия и продукты из свинины, баранины, говядины и мяса других видов убойных животных и птиц. Правила приемки и методы отбора проб
ГОСТ 13496.0 Комбикорма, комбикормовое сырье. Методы отбора проб
ГОСТ 22300 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
ГОСТ 25336 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26809.1 Молоко и молочная продукция. Правила приемки, методы отбора и подготовка проб к анализу. Часть 1. Молоко, молочные, молочные составные и молокосодержащие продукты
ГОСТ 28311 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29227 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 29245-91 Консервы молочные. Методы определения физических и органолептических показателей
ГОСТ 31339 Рыба, нерыбные объекты и продукция из них. Правила приемки и методы отбора проб
ГОСТ 31467 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
ГОСТ 31654 Яйца куриные пищевые. Технические условия
ГОСТ 31720 Пищевые продукты переработки яиц сельскохозяйственной птицы. Методы отбора проб и органолептического анализа
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации (www.easc.by) или по указателям национальных стандартов, издаваемым в государствах, указанных в предисловии, или на официальных сайтах соответствующих национальных органов по стандартизации. Если на стандарт дана недатированная ссылка, то следует использовать стандарт, действующий на текущий момент, с учетом всех внесенных в него изменений. Если заменен ссылочный стандарт, на который дана датированная ссылка, то следует использовать указанную версию этого стандарта. Если после принятия настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение применяется без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
(Измененная редакция, Изм. N 1).
3 Сущность метода
Метод основан на извлечении кокцидиостатиков из анализируемой пробы ацетонитрилом, очистке полученного экстракта методом твердофазной экстракции с последующим количественным определением их методом ВЭЖХ-МС/МС в режиме мониторинга множественных реакций.
Количественное определение проводят методом внутреннего стандарта.
4 Условия выполнения измерений и требования безопасности
4.1 При определении содержания кокцидиостатиков должны быть соблюдены следующие условия:
- температура окружающего воздуха | от 15°С до 27°С; | |
- относительная влажность воздуха | от 20% до 80%. |
4.2 Применяемые в работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.3 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.4 Приготовление градуировочных растворов проводят под тягой в вытяжном шкафу.
4.5 При проведении испытаний соблюдают правила безопасной эксплуатации сосудов, работающих под давлением, по ГОСТ 12.2.085.
4.6 При выполнении измерений на хромато-масс-спектрометре следует соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019, пожаровзрывобезопасности по ГОСТ 12.1.018 и инструкции по эксплуатации прибора.
4.7 К выполнению измерений допускают специалистов, имеющих высшее образование, прошедших соответствующий инструктаж, владеющих техникой хромато-масс-спектрометрии и изучивших инструкции по эксплуатации используемых приборов.
5 Средства измерений, вспомогательное оборудование, материалы, посуда и реактивы
5.1 Для определения содержания кокцидиостатиков применяют следующие средства измерений, вспомогательное оборудование, материалы и посуду:
- весы неавтоматического действия высокого класса точности по ГОСТ OIML R 76-1, с пределами допускаемой абсолютной погрешности взвешивания не более ±0,001 г;
- весы I класса точности с действительной ценой деления шкалы не более 0,1 мг;
- масс-спектрометр, оснащенный источником ионизации с электрораспылением, квадрупольными анализаторами, с диапазоном измерений от 25 до 1050 атомных единиц массы (а.е.м.) и относительным средним квадратическим отклонением выходного сигнала по площади пика не более 10%, с режимом получения и анализа фрагментных ионов (режим МС/МС);
- систему высокоэффективной жидкостной хроматографии, оснащенную бинарным насосом со смесителем, термостатом хроматографической колонки, обеспечивающим температуру нагрева до (40±1)°С;
- колонку хроматографическую*, заполненную обращенно-фазовым сорбентом с частицами размером не более 5,0 мкм, длиной 150 мм и внутренним диаметром 2 мм;
________________
* Например, типов Agilent Pursuit XRs C18, Phenomenex Luna C18. Данная информация приведена для удобства пользователей настоящего стандарта и не исключает возможности использования других колонок с аналогичными характеристиками. Допускается применение хроматографических колонок, заполненных обращенно-фазным сорбентом С8 или С18 с диаметром частиц не более 5 мкм, длиной не менее 50 мм.
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов измерений;
- модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом, позволяющий проводить концентрирование при температуре до 50°C;
- устройство вакуумное для твердофазной экстракции;
- картридж для твердофазной экстракции** вместимостью не менее 3 см, заполненный обращенно-фазовым сорбентом с частицами диаметром не более 50 мкм;
________________
** Например, моделей Waters Oasis HLB, Phenomenex Strata X. Данная информация приведена для удобства пользователей настоящего стандарта и не исключает возможности использования других моделей с аналогичными характеристиками. Допускается применение как готовых картриджей, так и набивных.
- измельчитель-гомогенизатор лабораторный;
- мельницу лабораторную для измельчения кормов;
- встряхиватель (шейкер) для пробирок вибрационного, ротационного, линейного или орбитального типа;
- центрифугу лабораторную рефрижераторную со скоростью вращения ротора не менее 15000 об./мин и диапазоном температур охлаждения от 4°С до 20°С, с адаптерами для пробирок вместимостью 15 см и микроцентрифужных пробирок вместимостью 1,5 см
;
- баню ультразвуковую с рабочей частотой не менее 20 кГц и объемом не менее 1 дм;
- шкаф сушильный;
- систему получения деионизированной воды высокой чистоты с удельным сопротивлением не более 18 Мом·см при температуре 20°С;*
________________
* Текст документа соответствует оригиналу. - .
- холодильник бытовой с рабочим диапазоном температур от 2°С до 8°С;
- камеру лабораторную морозильную с рабочим диапазоном температур от минус 15°С до минус 25°С;
- пробирки полипропиленовые вместимостью 15 см с навинчиваемыми пластмассовыми крышками;
- виалы (флаконы) стеклянные вместимостью 2 см с навинчиваемыми крышками и тефлоновыми прокладками диаметром 9 мм;
- пробы, не содержащие кокцидиостатики, подготовленные и проанализированные ранее в соответствии с требованиями разделов 7 и 8, в зависимости от типа анализируемой матрицы ("чистые" пробы***);
________________
*** Срок хранения "чистых" проб при температуре от минус 15°С до минус 25°С - не более 3 мес.
- дозаторы механические одноканальные переменной вместимости 10-100, 100-1000 мм![]() , 1-5 см
, 1-5 см![]() по ГОСТ 28311;
по ГОСТ 28311;
- пробирки полипропиленовые микроцентрифужные вместимостью 1,5 см;
- фильтры мембранные с порами диаметром не более 0,2 мкм;
- колбы Кн-1-250(1000)-14/23 ТС по ГОСТ 25336;
- пипетки 2-2-1-10 по ГОСТ 29227;
- колбы 1-10(100)-2 по ГОСТ 1770;
- цилиндры 1-10(100,1000)-2 по ГОСТ 1770;
- систему получения инертного газа для концентрирования жидкостей.
(Поправка. ИУС N 11-2020), (Измененная редакция, Изм. N 1).
5.2 При определении содержания кокцидиостатиков применяют следующие реактивы:
- ацетон по ГОСТ 2603;
- кислоту муравьиную по ГОСТ 5848, ч.д.а.;
- воду деионизированную для ВЭЖХ, полученную с использованием системы производства ультрачистой воды;
- метанол-яд по ГОСТ 6995, х.ч.;
- диметилсульфоксид (ДМСО) с массовой долей основного вещества не менее 99,0%;
- ацетонитрил для ВЭЖХ с массовой долей основного вещества не менее 99,9%;
- формиат аммония с массовой долей основного вещества не менее 99,0%;
- эфир этиловый уксусной кислоты (этилацетат) по ГОСТ 22300, х.ч.
5.3 При определении содержания кокцидиостатиков применяют:
5.3.1 Стандартные образцы кокцидиостатиков с массовой долей основного вещества не менее 90,0%:
- монензина натриевая соль;
- мадурамицина аммоний.
5.3.2 Стандартные образцы кокцидиостатиков с массовой долей основного вещества не менее 93,5%:
- наразин.
5.3.3 Стандартные образцы кокцидиостатиков с массовой долей основного вещества не менее 95,0%:
- лаидломицина пропионата калиевая соль;
- семдурамицина натриевая соль;
- декоквинат;
- толтразурил;
- тинидазол;
- динитрокарбанилид;
- диклазурил;
- толтразурила сульфон;
- галофугинона бромгидрат;
- этопабат;
- арприноцид;
- тернидазол;
- ронидазол;
- клопидол;
- ампролиума гидрохлорид;
- ласалоцида натриевая соль;
- робенидина гидрохлорид;
- салиномицина натриевая соль.
5.3.4 Внутренние стандарты кокцидиостатиков с массовой долей основного вещества не менее 95,0%:
- ронидазол-;
- динитрокарбанилид-;
- иономицина кальциевая соль;
- робенидин-;
- декоквинат-;
- этопабат-.
5.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерения, а также вспомогательного оборудования, реактивов и материалов по качеству не ниже вышеуказанных.
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и реактивов
6.1.1 Мойку и сушку посуды проводят в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.1.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.1.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105°С до 110°С.
6.1.4 Каждую новую партию реактивов проверяют на отсутствие контаминации анализируемыми соединениями путем проведения холостого опыта в соответствии с процедурой анализа.
6.2 Приготовление растворов
6.2.1 Приготовление подвижных фаз А и Б
6.2.1.1 Для приготовления подвижной фазы А в коническую колбу вместимостью 1000 см приливают 475 см
деионизированной воды, 250 см
метанола и 275 см
ацетонитрила, добавляют 0,5 г формиата аммония и 5,0 см
муравьиной кислоты. Полученный раствор дегазируют на ультразвуковой бане в течение 5 мин.
Срок хранения при комнатной температуре - не более 1 мес.
6.2.1.2 Для приготовления подвижной фазы Б в коническую колбу вместимостью 1000 смприливают 475 см
метанола и 525 см
ацетонитрила, добавляют 0,5 г формиата аммония и 0,5 см
муравьиной кислоты. Полученный раствор дегазируют на ультразвуковой бане в течение 5 мин.
Срок хранения при комнатной температуре - не более 1 мес.
6.2.2 Приготовление смеси метанола и ДМСО в объемном соотношении 1:1
В коническую колбу вместимостью 250 см мерным цилиндром отмеривают 50 см
метанола и 50 см
ДМСО, перемешивают.
Срок хранения при комнатной температуре - не более 1 мес.
6.3 Приготовление градуировочных растворов
6.3.1 Приготовление исходных растворов стандартов кокцидиостатиков массовыми концентрациями 100 мкг/см
Для приготовления исходных стандартных растворов рассчитывают массы стандартных образцов
![]() (мг), эквивалентные 10,0 мг соответствующих аналитов, по формуле
(мг), эквивалентные 10,0 мг соответствующих аналитов, по формуле
![]() , (1)
, (1)
где - массовая доля основного вещества в i-м стандартном образце, %
- молярная масса основного вещества в i-м стандартном образце, г/моль;
![]() - молярная масса i-го аналита, г/моль.
- молярная масса i-го аналита, г/моль.
Взвешивание стандартных образцов с рассчитанными массами проводят с точностью до первого десятичного знака.
Для приготовления индивидуальных стандартных растворов наразина, лаидломицина, декоквината, тинидазола, этопабата, тернидазола, ронидазола, ласалоцида, мадурамицина, робенидина, салиномицина в отдельные мерные колбы вместимостью 100 см
каждая вносят рассчитанные массы соответствующих стандартных образцов, приливают по 80 см
метанола, перемешивают.
Для приготовления индивидуальных стандартных растворов семдурамицина, толтразурила, диклазурила, толтразурила, галофугинона, арприноцида, клопидола, ампролиума, динитрокарбанилида, монензина в отдельные мерные колбы вместимостью 100 см
каждая вносят рассчитанные массы соответствующих стандартных образцов, приливают по 80 см
смеси метанола и ДМСО (6.2.2), перемешивают.
Колбы помещают в ультразвуковую баню на 1 мин, после чего доводят объемы растворов соответствующим растворителем до 100 см по меткам на колбах.
Срок хранения растворов при температуре от минус 15°С до минус 25°С - не более 2 лет.
Перед применением растворы выдерживают в термостате при температуре 20°С не менее 30 мин.
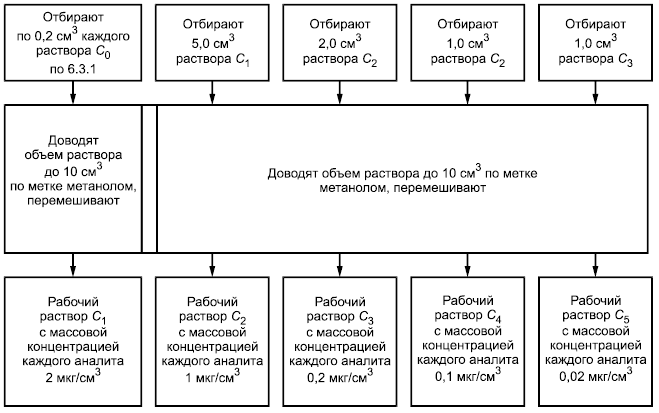
6.3.2 Приготовление рабочих стандартных растворов кокцидиостатиков -
Рабочие стандартные растворы -
готовят в мерных колбах вместимостью 10 см
в соответствии с рисунком 1.
|
Рисунок 1 - Приготовление рабочих растворов -
Растворы хранят при температуре от минус 15°С до минус 25°С не более 4 мес.
Перед применением растворы выдерживают в термостате при температуре 20°С не менее 30 мин.
Допускается приготовление рабочих стандартных растворов иных концентраций в заданном диапазоне измерений.
6.3.3 Приготовление исходных растворов внутренних стандартов кокцидиостатиков массовыми концентрациями 100 мкг/см
Для приготовления исходных растворов внутренних стандартов рассчитывают массы внутренних стандартов
(мг), эквивалентные 10,0 мг соответствующих аналитов по формуле (1).
Взвешивание образцов внутренних стандартов с рассчитанными массами проводят с точностью до первого десятичного знака.
Для приготовления индивидуальных растворов внутренних стандартов в отдельные мерные колбы вместимостью 100 см
каждая вносят рассчитанные массы ронидазола-
, иономицина кальциевой соли, робенидина-
; декоквината-
; этопабата-
, приливают по 80 см
метанола, перемешивают.
Для приготовления раствора динитрокарбанилида-
в мерную колбу вместимостью 100 см
вносят рассчитанную массу этого внутреннего стандарта, приливают по 80 см
смеси метанола и ДМСО (6.2.2), перемешивают.
Колбы помещают в ультразвуковую баню на 1 мин, после чего доводят объемы растворов соответствующим растворителем до 100 см по меткам на колбах.
Срок хранения растворов при температуре от минус 15°С до минус 25°С - не более 2 лет.
Перед применением растворы выдерживают в термостате при температуре 20°С не менее 30 мин.
Внутренние стандарты для кокцидиостатиков выбирают в соответствии с таблицей 1.
Таблица 1
Аналит | Наименование внутреннего стандарта |
Арприноцид | Ронидазол- |
Клопидол | |
Лаидломицин | |
Мадурамицин | |
Монензин | |
Ронидазол | |
Салиномицин | |
Семдурамицин | |
Тернидазол | |
Тинидазол | |
Толтразурил | |
Толтразурила сульфон | |
Диклазурил | |
Галофугинон | Иономицина кальциевая соль |
Ласалоцид | |
Наразин | |
Динитрокарбанилид | Динитрокарбанилид- |
Робенидин | Робенидин- |
Декоквинат | Декоквинат- |
Ампролиум | Этопабат- |
Этопабат |
6.3.4 Приготовление рабочего раствора внутренних стандартов кокцидиостатиков массовыми концентрациями 1000 нг/см
Для приготовления рабочего раствора в мерную колбу вместимостью 10 см
переносят по 0,1 см
растворов
, доводят до метки метанолом и перемешивают.
Срок хранения раствора при температуре от минус 15°С до минус 25°С - не более 4 мес.
Перед применением раствор выдерживают в термостате при температуре 20°С не менее 30 мин.
6.3.5 Приготовление матричных градуировочных растворов -
Матричные градуировочные растворы -
готовят в полипропиленовых пробирках вместимостью 15 см
из "чистых" проб массой 1,0 г, в которые вносят рабочий раствор внутренних стандартов
и рабочие растворы определяемых аналитов
-
в соответствии с таблицей 2.
Пробирки встряхивают в шейкере в течение 1-2 мин, выдерживают в темноте при комнатной температуре в течение 10 мин и проводят дальнейшую обработку растворов согласно разделу 7.
Срок хранения растворов -
при температуре от 2°С до 8°С - не более 2 сут.
Таблица 2 - Приготовление матричных градуировочных растворов -
Обозначение и массовая концентрация | Вносимый объем рабочего раствора, см | |||||
матричного градуировочного раствора | ||||||
| 0,5 | - | - | - | - | 0,05 |
| 0,25 | - | - | - | - | 0,05 |
| - | 0,1 | - | - | - | 0,05 |
| - | 0,05 | - | - | - | 0,05 |
| - | - | 0,05 | - | - | 0,05 |
| - | - | - | 0,05 | - | 0,05 |
| - | - | - | - | 0,05 | 0,05 |
7 Отбор и подготовка проб
7.1 Отбор проб
7.1.1 Отбор проб мяса, субпродуктов - по ГОСТ 7269.
7.1.2 Отбор проб мяса птицы, пищевых субпродуктов и полуфабрикатов из мяса птицы - по ГОСТ 31467.
7.1.3 Отбор проб рыбы - по ГОСТ 31339.
7.1.4 Отбор проб мясных продуктов - по ГОСТ 4288, ГОСТ 9792.
7.1.5 Отбор проб яиц - по ГОСТ 31654, пищевых яичных продуктов - по ГОСТ 31720.
7.1.6 Отбор проб молока и сухих молочных продуктов - по ГОСТ 26809.1.
7.1.7 Отбор проб комбикормов - по ГОСТ 13496.0.
7.1.8 Пробы, отобранные по 7.1.1-7.1.3, при отсутствии возможности анализа в день отбора замораживают и хранят при температуре от минус 15°С до минус 25°С до проведения анализа.
7.2 Подготовка проб
7.2.1 Подготовка проб мяса, субпродуктов, мясных продуктов, мяса и субпродуктов птицы, рыбы
Мышечную ткань предварительно очищают от грубой соединительной ткани, рыбу - от крупных костей, чешуи, не удаляя кожи. 100 г анализируемой пробы измельчают на гомогенизаторе и взвешивают 1,0 г гомогенизированной ткани в полипропиленовой пробирке вместимостью 15 см. Пипеточным дозатором в пробирку вносят 0,05 см
раствора внутренних стандартов
(6.3.4). Осторожно приливают 3 см
ацетонитрила и помещают пробирку на 15 мин в шейкер для экстракции. Затем центрифугируют при 4000 об./мин в течение 15 мин при температуре 10°С. Сливают органический слой в новую полипропиленовую пробирку вместимостью 15 см
, помещают ее на нагревательный модуль и упаривают в токе воздуха при температуре не более 40°С до 0,1-0,2 см
. К остатку приливают 2 см
деионизированной воды, перемешивают в шейкере 5 с и центрифугируют при 4000 об./мин в течение 10 мин при температуре 20°С. Полученный экстракт очищают методом твердофазной экстракции (ТФЭ).
Объемы деионизированной воды и метанола, пропускаемые через картридж, подбирают в зависимости от массы сорбента в картридже. Ниже приведены объемы для картриджа с массой сорбента 60 мг, в скобках приведены объемы для картриджа с массой сорбента 200 мг.
Перед нанесением экстракта на картридж последовательно кондиционируют сорбент 2(4) см метанола и 2(4) см
деионизированной воды. Затем пропускают через картридж полученный экстракт (при процедуре очищения вакуум или избыточное давление не применяют). Промывают картридж 2(4) см
деионизированной воды, сушат в вакууме водоструйного насоса в течение 10 мин и элюируют аналиты 2(4) см
метанола в новую полипропиленовую пробирку вместимостью 15 см
. Элюат помещают на нагревательный модуль и упаривают в токе воздуха при температуре не более 40°С до 0,05-0,1 см
. К полученному остатку приливают 0,9 см
раствора подвижной фазы А (6.2.1.1) и тщательно перемешивают, переливают экстракт в центрифужную полипропиленовую пробирку вместимостью 1,5 см
и центрифугируют при 15000 об./мин в течение 10 мин при температуре 20°С. Пипеточным дозатором переносят центрифугат в виалу для автосамплера жидкостного хроматографа. Полученный раствор используют для ВЭЖХ-МС/МС анализа.
(Измененная редакция, Изм. N 1).
7.2.2 Подготовка проб яичного порошка
Отобранную пробу яичного порошка перед анализом восстанавливают по ГОСТ 31720, тщательно перемешивают и взвешивают 1,0 г в полипропиленовой пробирке вместимостью 15 см. Пипеточным дозатором в пробирку вносят 0,05 см
раствора внутренних стандартов
(6.3.4). Осторожно приливают 3 см
ацетонитрила и помещают пробирку на 15 мин в шейкер для экстракции. Далее обработку и подготовку пробы к хроматографированию проводят по 7.2.1.
(Измененная редакция, Изм. N 1).
7.2.3 Обработка проб яиц и меланжа
Яйца отделяют от скорлупы и перемешивают на гомогенизаторе, меланж тщательно перемешивают. Взвешивают 1,0 г гомогенизированной пробы в полипропиленовой пробирке вместимостью 15 см. Пипеточным дозатором в пробирку вносят 0,05 см
раствора внутренних стандартов
(6.3.4). Осторожно приливают 3 см
ацетонитрила и помещают пробирку на 15 мин в шейкер для экстракции. Далее обработку и подготовку проб к хроматографированию проводят по 7.2.1.
7.2.4 Подготовка проб молока
Подготовку проб молока проводят по ГОСТ 26809.1. Сухие молочные продукты восстанавливают по ГОСТ 29245-91 (пункт 3.4).
Взвешивают 1,0 г гомогенизированной пробы в полипропиленовой пробирке вместимостью 15 см. Пипеточным дозатором в пробирку вносят 0,05 см
раствора внутренних стандартов
(6.3.4). Осторожно приливают 3 см
ацетонитрила и помещают пробирку на 15 мин в шейкер для экстракции. Далее обработку и подготовку проб к хроматографированию проводят по 7.2.1.
7.2.5 Подготовка проб комбикормов
Отобранную пробу комбикорма измельчают на лабораторной мельнице. Взвешивают 1,0 г гомогенизированной пробы в полипропиленовой пробирке вместимостью 15 см. Пипеточным дозатором в пробирку вносят 0,05 см
раствора внутренних стандартов
(6.3.4). Осторожно приливают 10 см
ацетонитрила, 1 см
деионизированной воды и помещают пробирку на 15 мин в шейкер для экстракции. Затем центрифугируют при 4000 об./мин в течение 15 мин при температуре 10°С. Далее обработку и подготовку пробы к хроматографированию проводят по 7.2.1.
8 Порядок выполнения анализа
8.1 Условия хроматографического разделения
8.1.1 Хромато-масс-спектрометр включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры рабочих режимов масс-спектрометрического детектирования и хроматографического разделения.
8.1.2 Например, для колонки длиной 150 мм, диаметром 2 мм, с обращенно-фазовым сорбентом с частицами размером не более 5,0 мкм соблюдают следующие условия хроматографического анализа:
- температура колонки - 40°С;
- скорость потока подвижной фазы - 0,2 см/мин;
- объем вводимой пробы - 10 мм.
8.1.3 Разделение проводят в режиме градиентного элюирования (приготовление подвижных фаз А и Б по 6.2.1): в начальный момент и до 2,0 мин - элюирование при 100% подвижной фазы А, с 2,0 по 4,0 мин - градиентное элюирование к 100% подвижной фазы Б, с 4,0 по 18,0 мин - элюирование при 100% подвижной фазы Б, с 18,0 по 18,10 мин - переход к элюированию в 100% подвижной фазы А, с 18,10 по 28,0 мин - уравновешивание колонки при 100% подвижной фазы А.
Параметры метода воздействия на ионы в режиме мониторинга множественных реакций (MRM) приведены в таблице 3.
Таблица 3 - Параметры воздействия на ионы в режиме MRM и условиях электрораспыления с регистрацией положительных или отрицательных (-) ионов
Кокцидиостатик | Ион-предшественник, m/z | Ион-продукт, m/z | Время выхода пика, мин | ||
Ампролиум | 243,2 | 150,1 | 94,1 | 2,0 | |
Клопидол | 192,0 | 101,0 | 86,8 | 2,3 | |
Ронидазол- | 204,1 | 143,1 | 2,2 | ||
Ронидазол | 201,1 | 140,1 | 55,0 | 2,2 | |
Тернидазол | 186,2 | 128,1 | 82,0 | 2,3 | |
Тинидазол | 248,2 | 121,1 | 93,0 | 2,4 | |
Арприноцид | 278,1 | 143,0 | 107,1 | 2,6 | |
Этопабат | 238,2 | 206,1 | 136,0 | 2,8 | |
Этопабат- | 243,2 | 211,1 | 2,8 | ||
Динитрокарбанилид- | -309,0 | 140,9 | 6,0 | ||
Динитрокарбанилид | -300,9 | 136,9 | 106,9 | 6,0 | |
Толтразурила сульфон | -456,0 | 456,0 | 42,0 | 6,0 | |
Диклазурил | -405,0 | -407,0 | 333,8 | 335,8 | 6,3 |
Галофугинон | 414,1 | 100,1 | 138,1 | 3,0 | |
Толтразурил | -424,0 | 424,0 | 41,9 | 6,4 | |
Робенидин | 334,1 | 155,1 | 138,0 | 8,9 | |
Робенидин- | 342,1 | 159,1 | 8,9 | ||
Декоквинат | 418,3 | 372,3 | 204,1 | 10,2 | |
Декоквинат- | 423,3 | 377,3 | 10,2 | ||
Ласалоцид | 613,4 | 377,2 | 359,3 | 10,5 | |
Семдурамицин | 890,6 | 629,5 | 393,2 | 10,4 | |
Монензин | 693,3 | 675,5 | 461,3 | 10,8 | |
Лаидломицин | 777,4 | 503,3 | 521,4 | 10,5 | |
Мадурамицин | 934,5 | 629,5 | 647,5 | 11,0 | |
Салиномицин | 773,5 | 431,3 | 531,3 | 11,3 | |
Наразин | 787,5 | 431,3 | 531,4 | 10,2 | |
Иономицина калиевая соль* | 732,5 | 279,1 | 10,2 | ||
* Внутренние стандарты. | |||||
Примечание - Приведенные выше параметры хроматографического разделения и масс-спектрометрического детектирования могут отличаться в зависимости от используемого оборудования.
8.1.4 Относительное отклонение времени удерживания кокцидиостатиков в анализируемых пробах от градуировочных данных не должно превышать 2,5%.
8.2 Установление градуировочной характеристики
8.2.1 Установление и расчет градуировочной характеристики проводят в каждой серии анализов с использованием программного обеспечения хромато-масс-спектрометрической системы.
8.2.2 Проводят измерения не менее трех матричных градуировочных растворов, приготовленных по 6.3.5, в порядке возрастания их концентраций. Определяют времена удерживания ион-продуктов аналитов и их внутренних стандартов.
8.2.3 Вычисление площади пика проводят для каждого ион-продукта анализируемых аналитов и их внутренних стандартов. Количественное определение кокцидиостатиков проводят по одному (наиболее интенсивному) ион-продукту. Для подтверждения наличия кокцидиостатиков рассчитывают отношения площади пика двух ион-продуктов для каждого аналита в градуировочном растворе.
8.2.4 Градуировочную характеристику устанавливают в координатах "отношение площади пика определяемого соединения к площади пика внутреннего стандарта этого соединения" - "отношение концентраций аналита и внутреннего стандарта". При построении градуировочной характеристики используют линейную функцию вида y=a+bx, при этом коэффициент корреляции должен быть не менее 0,98.
Установление градуировочной характеристики проводят при каждой серии измерений заново.
8.3 ВЭЖХ-МС/МС измерение
8.3.1 Для измерения содержания кокцидиостатиков проводят ВЭЖХ-МС/МС анализ в соответствии с руководством (инструкцией) по эксплуатации применяемого оборудования.
8.3.2 Анализ выполняют в виде серии измерений, включающей следующие образцы:
- подвижную фазу А (6.2.1.1);
- "чистую" пробу;
- градуировочные растворы (6.3.5);
- экстракты анализируемых проб, приготовленных по 7.2.
8.3.3 Определяют и регистрируют на хроматограмме время удерживания пиков двух ион-продуктов каждого аналита, соответствующее времени удерживания, найденному при измерении градуировочных растворов по 8.1.3.
9 Обработка результатов измерений
9.1 В соответствии с данными, полученными при измерении градуировочных растворов, проводят количественную обработку хроматограмм с использованием программного обеспечения. Метод обработки хроматограмм - внутренний стандарт.
9.2 Расчеты содержания кокцидиостатика и площади пика выполняются системой обработки данных в автоматическом режиме.
9.3 Вычисление площади пика проводят по ион-продукту с более интенсивным сигналом для каждого кокцидиостатика. Отклонения относительных ионных интенсивностей ионов в анализируемой пробе от относительных ионных интенсивностей ионов, полученных при анализе градуировочных растворов, не должны превышать значений, указанных в таблице 4.
Таблица 4 - Допустимые отклонения относительных ионных интенсивностей
Относительная ионная интенсивность, % от основного пика | Максимально допустимое отклонение для ВЭЖХ-МС/МС детектирования, % |
Св. 50 | ±20 |
Св. 20 до 50 включ. | ±25 |
Св. 10 до 20 включ. | ±30 |
Менее 10 включ. | ±50 |
9.4 Полученные результаты измерений анализируемой пробы округляют:
- в диапазоне значений от 1 до 100 мкг/кг включительно - до второго десятичного знака после запятой;
- в диапазоне значений от 100 до 1000 мкг/кг включительно - до первого десятичного знака после запятой.
За результат измерений принимают среднеарифметическое значение результатов двух параллельных измерений анализируемой пробы, выраженное в микрограммах на килограмм (мкг/кг), если выполняется условие приемлемости по ГОСТ ИСО 5725-6-2003 (пункт 5.2.2).
Значения предела повторяемости r приведены в таблице 5.
Таблица 5
Диапазон измерений содержания кокцидиостатиков, мкг/кг | Предел повторяемости r, %, при P=0,95, i=2 |
От 1,0 до 10,0 включ. | 25 |
Св. 10,0 " 100,0 " | 20 |
Св. 100,0 " 1000,0 " | 15 |
Полученные среднеарифметические значения двух параллельных измерений анализируемой пробы округляют:
- в диапазоне значений от 1 до 100 мкг/кг включительно - до первого десятичного знака после запятой;
- в диапазоне значений от 100 до 1000 мкг/кг включительно - до целого числа.
10 Метрологические характеристики
Установленный в настоящем стандарте метод обеспечивает выполнение измерений содержания кокцидиостатиков с относительной расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата k=2, указанной в таблице 6.
Таблица 6
Кокцидиостатик | Значение относительной расширенной неопределенности | ||
От 1,0 до 10 включ. | Св. 10 до 100 включ. | Св. 100 до 1000 включ. | |
Ампролиум | 65 | 43 | 30 |
Клопидол | 54 | 27 | 47 |
Ронидазол | 43 | 25 | 25 |
Тернидазол | 42 | 25 | 25 |
Тинидазол | 35 | 25 | 25 |
Арприноцид | 38 | 25 | 25 |
Этопабат | 55 | 32 | 28 |
Галофугинон | 31 | 55 | 66 |
Динитрокарбанилид | 51 | 30 | 25 |
Толтразурила сульфон | 80 | 40 | 40 |
Диклазурил | 55 | 66 | 66 |
Толтразурил | 55 | 46 | 28 |
Робенидин | 62 | 39 | 39 |
Декоквинат | 48 | 38 | 30 |
Ласалоцид | 49 | 48 | 45 |
Семдурамицин | 50 | 33 | 32 |
Монензин | 88 | 50 | 40 |
Лаидломицин | 85 | 50 | 50 |
Мадурамицин | 60 | 51 | 30 |
Салиномицин | 82 | 62 | 46 |
Наразин | 52 | 37 | 34 |
Примечание - Значения относительной расширенной неопределенности, указанные в таблице 4, соответствуют границам относительной погрешности результатов измерений при Р=0,95.
11 Оформление результатов измерений
Содержание i-го кокцидиостатика М, мкг/кг, представляют в виде
![]() , при Р=0,95, (2)
, при Р=0,95, (2)
где - среднеарифметическое значение двух параллельных измерений содержания i-го кокцидиостатика в анализируемой пробе, мкг/кг;
- значение относительной расширенной неопределенности содержания i-го кокцидиостатика для соответствующего диапазона измерений (см. таблицу 6), %.
В случае необходимости допускается представление результата измерений в мг/кг путем деления значения содержания i-го аналита, полученного в соответствии с 9.2, и значения расширенной неопределенности ![]() в абсолютных единицах (мкг/кг) на 1000 (с сохранением количества значащих цифр).
в абсолютных единицах (мкг/кг) на 1000 (с сохранением количества значащих цифр).
(Измененная редакция, Изм. N 1).
12 Контроль качества результатов измерений
Для контроля качества испытаний в соответствии с требованиями процедуры подготовки проб (7.2) необходимо в ходе анализа каждой серии проб проводить анализ контрольной пробы с приписанным значением содержания i-го кокцидиостатика.
Результаты измерений признают удовлетворительными при выполнении следующего неравенства
![]() , (3)
, (3)
где - результат анализа содержания i-го кокцидиостатика в образце для контроля, мкг/кг;
X - установленное значение содержания i-го кокцидиостатика в образце для контроля, мкг/кг;
- значение относительной расширенной неопределенности содержания i-го кокцидиостатика для соответствующего диапазона измерений (см. таблицу 6), %.
13 Контроль стабильности результатов измерений
Контроль стабильности результатов измерений осуществляют в соответствии с документами, утвержденными в лаборатории. Рекомендуется использование контрольных карт Шухарта в соответствии с ГОСТ ИСО 5725-6*.
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
(Измененная редакция, Изм. N 1).
УДК 637:614.3:006.354 | МКС | 65.120 | |
67.050 | |||
67.100.10 | |||
67.120.10 | |||
67.120.20 | |||
67.120.30 | |||
Ключевые слова: пищевые продукты, корма, продовольственное сырье, кокцидиостатики, метод определения содержания с помощью высокоэффективной жидкостной хроматографии с масс- спектрометрическим детектором | |||
Редакция документа с учетом
изменений и дополнений подготовлена