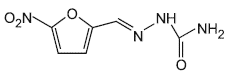ГОСТ Р 53992-2010
Группа Н09
Н19
Н11
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРОДУКТЫ ПИЩЕВЫЕ, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ
Метод определения остаточного содержания метаболитов нитрофуранов с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Food products, food raw materials. Method for determination of the nitrofuran metabolites residual content by high performance liquid chromatography-mass spectrometry (HPLC-MS)
ОКС 67.050
67.100
67.120
Дата введения 2012-01-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГУ "ВГНКИ")
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 335 "Методы испытаний агропромышленной продукции на безопасность"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2010 г. N 568-ст
4 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
1 Область применения
Настоящий стандарт распространяется на молоко, молочные продукты, яйца, яичный порошок, мясо и мясные продукты, включая мясо и продукты из мяса птицы, мед, креветки, и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием для определения остаточного содержания метаболитов нитрофуранов в диапазоне измерений массовой доли от 1,0 до 1000,0 мкг/кг.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51447-99 (ИСО 3100-1-91) Мясо и мясные продукты. Методы отбора проб
ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ Р 52121-2003 Яйца куриные пищевые. Технические условия
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ Р 53669-2009 Пищевые продукты переработки яиц сельскохозяйственной птицы. Методы отбора проб и органолептического анализа
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.2.085-2002 Сосуды, работающие под давлением. Клапаны предохранительные. Требования безопасности
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7631-2008 Рыба, нерыбные объекты и продукция из них. Методы определения органолептических и физических показателей
ГОСТ 13867-68 Продукты химические. Обозначения чистоты
ГОСТ 14261-77 Кислота соляная особой чистоты. Технические условия
ГОСТ 19792-2001 Мед натуральный. Технические условия
ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26809-86 Молоко и молочные продукты. Правила приемки, методы отбора и подготовка проб к анализу
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
3.1 Определение остаточных количеств метаболитов нитрофуранов (приложение А), образующих в организме стабильные связи с белками, проводят методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (ВЭЖХ-МС/МС).
3.2 Количественное определение остаточного содержания метаболитов нитрофуранов проводят методом внутреннего стандарта по площади пика идентифицированных соединений при помощи градуировочной кривой.
3.3 Детектирование анализируемых проб проводят в режиме регистрации выбранных реакций.
4 Средства измерений, вспомогательное оборудование, материалы, реактивы
4.1 При определении содержания метаболитов нитрофуранов применяют следующие средства измерений, вспомогательное оборудование и материалы:
- масс-спектрометр с диапазоном измерения от 100 до 500 атомных единиц массы (а.е.м.), массовым разрешением не менее 500, точностью измерения массы не ниже 0,2 а.е.м., с режимом получения и анализа фрагментных ионов (режим МС/МС);
- систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем, термостата хроматографической колонки, обеспечивающего температуру нагрева до 50°С;
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов масс-спектрометрических измерений;
- весы лабораторные I или II класса точности с наибольшим пределом взвешивания 200 и 500 г, с ценой деления шкалы 0,1 и 1,0 мг соответственно по ГОСТ Р 53228;
- рН-метр с набором электродов, с диапазоном измерений от 0 до 14 ед. рН и с пределами абсолютной погрешности измерений ±0,01 рН;
- пипетки одноканальные переменного объема 10-100 мм, 40-200 мм
, 200-1000 мм
, 1-5 см
с допустимой относительной погрешностью дозирования по гексану, метанолу и этилацетату не более 2%;
- модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом и максимальной температурой термостатирования 40°С;
- измельчитель-гомогенизатор лабораторный;
- встряхиватель вибрационный для пробирок орбитального типа движения с амплитудой встряхивания 3 мм и диапазоном скоростей от 150 до 2500 об/мин;
- центрифугу лабораторную рефрижераторную со скоростью вращения ротора не менее 10000 об/с и диапазоном температур охлаждения от 4°С до 20°С, с адаптерами для пробирок вместимостью 15 см и микроцентрифужных пробирок вместимостью 1,5 см
;
- баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм;
- ротационный испаритель со скоростью вращения от 20 до 280 об/мин и температурным диапазоном нагревательной бани от 30°С до 100°С;
- колонку хроматографическую обращенно-фазную длиной не менее 150 мм с диаметром частиц сорбента не более 3,5 мкм;
- устройство вакуумное для твердофазной экстракции;
- картридж для твердофазной экстракции объемом не менее 12 см, заполненный обращенно-фазным сорбентом с диаметром частиц не более 50 мкм;
- виалы (флаконы) полипропиленовые вместимостью 15 и 50 см с герметично закрывающимися пластмассовыми крышками;
- фильтры мембранные с размером пор не более 0,45 мкм;
- виалы (флаконы) стеклянные вместимостью 2 и 4 см с завинчивающимися крышками и тефлоновыми прокладками;
- вкладыши стеклянные для 2 см флаконов на 50 мм
;
- пробирки мерные стеклянные П-1-5-0,1ХС, П-2-10-14/23 по ГОСТ 1770;
- колбы круглодонные К-1-100-14/23 ТС по ГОСТ 25336;
- пипетки стеклянные градуированные по ГОСТ 29227;
- колбы мерные стеклянные К-2-100-2, К-2-1000-2 по ГОСТ 1770;
- цилиндры мерные стеклянные 1-25 (100, 500)-1 по ГОСТ 1770;
- бумагу универсальную индикаторную для определения рН;
- камеру лабораторную морозильную с цифровым контролером температуры и рабочим диапазоном температур от минус 18°С до минус 24°С.
Допускается использование других средств измерений, оборудования и материалов с метрологическими и техническими характеристиками не ниже указанных.
4.2 При определении содержания метаболитов нитрофуранов применяют следующие реактивы:
- кислоту соляную по ГОСТ 14261, ос.ч.;
- метанол по ГОСТ 6995, х.ч.;
- н-гексан, х.ч.;
- этилацетат по ГОСТ 22300, х.ч.;
- ацетон по ГОСТ 2603;
- спирт этиловый ректификованный по ГОСТ Р 51652;
- эфир диэтиловый (серный);
- метил-трет-бутиловый эфир для хроматографии;
- формиат аммония с содержанием основного вещества 99%;
- муравьиную кислоту по ГОСТ 5848, ч.д.а.;
- 2-нитробензальдегид (НБА) с содержанием основного вещества 98%;
- натрий фосфорнокислый додекагидрат;
- натрия гидроокись по ГОСТ 4328, ч.д.а.;
- ацетонитрил, ч.д.а.;
- воду деионизованную;
- воду дистиллированную по ГОСТ 6709.
Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.) по ГОСТ 13867.
4.3 Для определения содержания метаболитов нитрофуранов применяют следующие стандартные образцы:
4.3.1 Стандартные образцы метаболитов нитрофуранов:
- 3-амино-2-оксазолидинон (АОЗ) с содержанием основного вещества не менее 99,0% (Vetranal, 33347)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 3-амино-5-метилморфолино-2-оксазолидинон (АМОЗ), с содержанием основного вещества не менее 99,0% (Witega, NF003)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 1-амино-гидантоин (АГД) гидрохлорид с содержанием основного вещества не менее 99,0% (Witega, NF001)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- семикарбазид (СЕМ) гидрохлорид с содержанием основного вещества не менее 99,0% (Vetranal, 33656)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 3-[(2-нитрофенил)метилен]-амино-2-оксазолидинон (НФ-АОЗ) с содержанием основного вещества не менее 99,0%, (Witega, NF013)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 5-метилморфолино-3-[(2-нитрофенил)метилен]-3-амино-2-оксазолидинон (НФ-АМОЗ) с содержанием основного вещества не менее 99,0%, (Witega, NF011)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 1-[(2-нитрофенил)метилен]-амино-гидантоин (НФ-АГД) с содержанием основного вещества не менее 99,0% (Witega, NF009)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- (2-нитрофенил)метилен-семикарбазид (НФ-СЕМ) с содержанием основного вещества не менее 99,0%, (Witega, NF015)*.
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
4.3.2 Внутренние стандарты метаболитов нитрофуранов:
- d-3-амино-2-оксазолидинон (d
-AOЗ) с содержанием основного вещества не менее 99,0% (Witega, NF006)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- d-3-амино-5-метилморфолино-2-оксазолидинон (d
-AMOЗ) с содержанием основного вещества не менее 99,0% (Vetranal, 33881)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 1,2-N,С
-семикарбазид (1,2-N
,C
-CEM) гидрохлорид с содержанием основного вещества не менее 99,0% (Witega, NF008)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- (С)
1-аминогидантоин) ((С
)
-АГД) с содержанием основного вещества не менее 99,0% (Witega, NF002)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- d-3-[(2-нитрофенил)метилен]-амино-2-оксазолидинон (НФ-d
-АОЗ) с содержанием основного вещества не менее 99,0% (Witega, NF014)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- d-5-метилморфолино-3-[(2-нитрофенил)метилен]-3-амино-2-оксазолидинон (НФ-d
-АМОЗ) с содержанием основного вещества не менее 99,0% (Witega, NF012)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- (С)
1-[(2-нитрофенил)метилен]-амино-гидантоин (НФ-(С
)
-АГД) с содержанием основного вещества не менее 99,0% (Witega, NF015)*;
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
- 1,2-N,С
-(2-нитрофенил)метилен-семикарбазид (НФ-1,2-N
,C
-СЕМ) с содержанием основного вещества не менее 99,0% (Witega, NF016)*.
________________
* Стандартный образец является рекомендуемым к применению. Эта информация приведена для удобства пользователей настоящего стандарта.
5 Требования безопасности
5.1 Используемые в работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
5.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
5.3 Операции по приготовлению градуировочных растворов следует проводить под тягой в вытяжном шкафу.
5.4 При проведении испытаний следует соблюдать требования ГОСТ 12.2.085 и правила устройства и безопасной эксплуатации сосудов, работающих под давлением [1].
5.5 При выполнении измерений на хромато-масс-спектрометре следует соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019 и инструкцией по эксплуатации прибора.
5.6 К выполнению измерений методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации используемой аппаратуры.
6 Порядок подготовки к проведению измерений
6.1 Отбор проб
6.1.1 Отбор проб проводят в соответствии с методическими указаниями по отбору проб пищевой продукции с целью лабораторного контроля качества и безопасности, утвержденными федеральным органом исполнительной власти по ветеринарному и фитосанитарному надзору [2].
6.1.2 Отбор проб мяса и мясных продуктов, включая мясо и продукты из мяса птицы, проводят в соответствии с ГОСТ Р 51447.
6.1.3 Отбор проб молока и молочных продуктов проводят в соответствии с ГОСТ 26809.
6.1.4 Отбор проб меда проводят в соответствии с ГОСТ 19792.
6.1.5 Отбор проб яиц и яичного порошка производят в соответствии с ГОСТ Р 52121 и ГОСТ Р 53669.
6.1.6 Отбор проб креветок проводят в соответствии с ГОСТ 7631.
6.2 Подготовка хромато-масс-спектрометрической системы к выполнению измерений
Подготовку хромато-масс-спектрометра к работе осуществляют в соответствии с техническим руководством по эксплуатации прибора.
При этом должны быть соблюдены следующие условия:
- температура окружающего воздуха | от 20°С до 25°С; | |||
- атмосферное давление | от 84 до 106 кПа; | |||
- напряжение в электросети | (220±20) В; | |||
- частота тока в электросети | от 49 до 51 Гц; | |||
- относительная влажность воздуха | от 40% до 80%. | |||
6.3 Приготовление растворов
6.3.1 Приготовление раствора соляной кислоты молярной концентрации 0,1 моль/дм
В мерную колбу вместимостью 1000 см вносят 8,7 см
соляной кислоты, растворяют в дистиллированной воде и доводят объем до метки этим же растворителем.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.2 Приготовление раствора соляной кислоты молярной концентрации 0,2 моль/дм
В мерную колбу вместимостью 1000 см вносят 17,4 см
соляной кислоты, растворяют в дистиллированной воде и доводят объем до метки этим же растворителем.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.3 Приготовление раствора натрия гидроокиси молярной концентрации 2 моль/дм
В мерную колбу вместимостью 1000 см вносят 84,0 г натрия гидроокиси, растворяют в дистиллированной воде и доводят объем до метки этим же растворителем.
Срок хранения при комнатной температуре в сосуде из полимерных материалов - не более 1 мес.
6.3.4 Приготовление раствора нитробензальдегида (НБА) молярной концентрации 100 ммоль/дм
В мерной пробирке вместимостью 10 см растворяют 151,0 мг 2-нитробензальдегида в метаноле и доводят до метки.
Срок хранения при комнатной температуре - не более одной недели.
6.3.5 Приготовление раствора натрия фосфорнокислого додекагидрата молярной концентрации 0,3 моль/дм
В мерной колбе вместимостью 100 см растворяют 11,4 мг фосфата натрия додекагидрата в дистиллированной воде и доводят до метки.
Срок хранения при комнатной температуре - не более 6 мес.
6.3.6 Приготовление раствора муравьиной кислоты в смеси метил-трет-бутиловый эфир/метанол (90/10)
Готовят смесь эфир/метанол путем смешивания 90 см метил-трет-бутилового эфира и 10 см
метанола. В мерную колбу вместимостью 100 см
добавляют 2,7 см
муравьиной кислоты и доводят объем до метки смесью эфир/метанол.
Раствор используют свежеприготовленным.
6.3.7 Приготовление растворов элюентов мобильной фазы А и Б
6.3.7.1 Для приготовления раствора элюента мобильной фазы А в мерной колбе вместимостью 1000 см смешивают 500 см
метанола и 500 см
ацетонитрила.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.7.2 Для приготовления раствора элюента мобильной фазы Б в мерную колбу вместимостью 1000 см приливают деионизованную воду и добавляют 0,5 г формиата аммония и 0,41 см
муравьиной кислоты, объем доводят до метки деионизованной водой.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.8 Приготовление растворителя для проведения ВЭЖХ-МС/МС
Для приготовления растворителя для проведения ВЭЖХ-МС/МС анализа смешивают 15 см фазы А и 85 см
фазы Б.
6.4 Приготовление градуировочных растворов
6.4.1 Приготовление градуировочных растворов С для АОЗ, АМОЗ, СЕМ, АГД, d
-AOЗ, d
-AMOЗ, (С
)
-АГД, 1,2-N
,C
-CEM, НФ-АОЗ, НФ-АМОЗ, НФ-СЕМ, НФ-АГД, НФ-d
-АОЗ, НФ-d
-АМОЗ, НФ-(С
)
-АГД, НФ-1,2-N
,С
-СЕМ
Для приготовления градуировочных растворов на лабораторных весах взвешивают 10 мг* каждого стандарта и переносят в мерную пробирку вместимостью 10 см. Добавляют метанол, помещают в ультразвуковую баню на 1 мин, доводят полученный раствор до метки метанолом.
________________
* Массы навесок для стандартных образцов в виде гидрохлоридов СЕМ; 1,2-N,C
-CEM и АГД составляют 14,86; 14,86 и 13,17 мг соответственно.
Массовая концентрация каждого соединения в растворе С составляет 1 мг/см
.
6.4.2 Приготовление градуировочных растворов С-С
для АОЗ, АМОЗ, СЕМ, АГД, d
-AOЗ, d
-AMOЗ, (С
)
-АГД, 1,2-N
,C
-CEM, НФ-АОЗ, НФ-АМОЗ, НФ-СЕМ, НФ-АГД, НФ-d
-АОЗ, НФ-d
-АМОЗ, НФ-(С
)
-АГД, НФ-1,2-N
,С
-СЕМ
Для приготовления градуировочного раствора С переносят 1 см
раствора С
в мерную пробирку вместимостью 10 см
, доводят до метки метанолом и тщательно перемешивают. Массовая концентрация каждого аналита в растворе С
составляет 100 нг/мм
.
Растворы С и С
готовят аналогичным образом, используя 100 мм
С
для приготовления 10 см
раствора С
и 1000 мм
С
- для 10 см
раствора С
.
Массовая концентрация каждого аналита в растворе С составляет 10 нг/мм
, в растворе C
- 1 нг/мм
.
6.4.3 Приготовление смеси нитрофенильных производных АОЗ, АМОЗ, СЕМ, АГД (НФ-смесь)
Для приготовления смеси нитрофенильных производных переносят по 1000 мм каждого стандартного раствора С
(см. 6.4.1) в мерную пробирку вместимостью 10 см
и доводят объем до метки метанолом.
Массовая концентрация каждого аналита в полученном растворе С составляет 100 нг/см
.
6.4.4 Приготовление смеси АОЗ, АМОЗ, СЕМ, АГД (смеси метаболитов)
Для приготовления смеси в мерную пробирку вместимостью 10 см добавляют 100 мм
раствора С
АОЗ, 100 мм
раствора С
АМОЗ, 1000 мм
раствора С
АГД и 300 мм
раствора С
АГД (см. 6.4.1) и доводят до метки метанолом.
1 см данной смеси разбавляют метанолом в 10 раз и получают раствор С
.
6.4.5 Приготовление раствора внутреннего стандарта
Для приготовления раствора внутреннего стандарта в мерную пробирку вместимостью 10 см переносят по 100 мм
градуировочных растворов С
d
-АОЗ, d
-AMOЗ, (С
)
-АГД, 1,2-N
,C
-CEM (см. 6.4.1) и доводят до метки метанолом.
Полученный раствор разбавляют в 10 раз метанолом и используют в качестве внутреннего стандарта.
Массовая концентрация каждого аналита в полученном растворе составляет 0,1 нг/мм.
6.4.6 Приготовление смеси нитрофенильных производных АОЗ, АМОЗ, АГД и СЕМ (НФ-смесь 1)
Для приготовления смеси в мерную пробирку вместимостью 10 см добавляют по 1000 мм
С
растворов НФ-АОЗ и НФ-АМОЗ (см. 6.4.1), объем доводят до метки метанолом.
Далее при помощи последовательного разбавления готовят раствор концентрацией 0,1 нг/мм. Для этого 100 мм
полученного раствора разбавляют до 10 см
метанолом (С
НФ-смесь 1). 1000 мм
раствора С
НФ-смесь 1 вновь разбавляют до 10 см
метанолом, получая раствор С
НФ-смесь 1, который разбавляют в 1000 раз, получая раствор С
НФ-смесь 1.
6.4.7 Приготовление смеси нитрофенильных производных d-AOЗ, d
-AMOЗ, (С
)
-АГД, 1,2-N
,С
-СЕМ (НФ-смесь 2)
Для приготовления смеси нитрофенильных производных в мерную пробирку вместимостью 10 см добавляют по 1000 мм
С
растворов d
-АОЗ, d
-AMOЗ, (С
)
-АГД, 1,2-N
,C
-CEM (6.4.1), объем доводят до метки метанолом. Далее при помощи последовательного разбавления метанолом готовят раствор концентрацией 0,1 нг/мм
.
6.4.8 Приготовленные растворы хранят в морозильнике при температуре не выше минус 20°С в течение 1,5 лет. Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.5 Построение градуировочной характеристики
6.5.1 Градуировочную характеристику строят при помощи матричной градуировки. Для этого проводят обработку "чистых" проб, приготовленных и проанализированных ранее, не содержащих метаболитов нитрофуранов в соответствии с требованиями раздела 7, в зависимости от типа исследуемой матрицы. На стадии перерастворения перед введением в хроматограф в мерную пробирку вместимостью 5 см добавляют нитрофенильную смесь метаболитов (см. 6.4.3) с таким расчетом, чтобы окончательные массовые концентрации находились в пределах от 0,1 до 500 нг/см
. Затем добавляют 50 мм
смеси нитрофенильных дейтерированных производных (см. 6.4.7) и необходимое количество растворителя (см. 6.3.8), доводя объем до 1 см
.
6.5.2 Для получения градуировочных данных используют не менее трех уровней концентраций матричных градуировочных растворов. Определяемые в анализируемом образце массовые концентрации метаболитов нитрофуранов должны находиться в диапазоне концентраций градуировочной характеристики.
6.5.3 При градуировке хроматографа анализируют матричные градуировочные растворы различных уровней концентраций в условиях, приведенных в 6.2, 6.6. Затем, используя программное обеспечение для сбора и обработки хроматографических данных, для метаболитов нитрофуранов устанавливают градуировочные характеристики в виде зависимостей отношения площадей хроматографических пиков соответствующего соединения к площади пика внутреннего стандарта от массовой концентрации соединения в образце.
Построение графиков допускается проводить при помощи программы обработки данных ВЭЖХ-МС/МС или при помощи программы Excel (Microsoft Office).
6.5.4 Вычисление площади пика проводят для каждого дочернего иона анализируемых соединений. Допускается проведение количественных измерений по одному, наиболее интенсивному, дочернему иону. Для подтверждения наличия метаболитов нитрофуранов рассчитывают отношения площади пика двух дочерних ионов для каждого соединения, которые должны соответствовать значениям, указанным в таблице 1.
Таблица 1 - Параметры воздействия на ионы в режиме MRM и условиях электроспрея с регистрацией положительных ионов
Метаболиты нитрофуранов | Ион предшественник, m/z | Дочерние ионы, m/z |
2-НФ-АОЗ | 236,2 | 134,0/104,1 |
2-НФ-d | 240,3 | 134,0/149,1 |
2-НФ-АМОЗ | 335,2 | 291,1/262,1 |
2-НФ-d | 340,3 | 296,2/265,2 |
2-НФ-АГД | 249,2 | 134,0/104,1 |
2-НФ-(С | 251,9 | 133,9/179,1 |
2-НФ-СЕМ | 209,2 | 191,9/166,0 |
2-НФ-1,2-N | 212,2 | 168,0/195,2 |
6.5.5 Расчетные концентрации для обоих фрагментных ионов каждого метаболита нитрофуранов должны совпадать в пределах 20%.
Градуировочная зависимость считается приемлемой, если рассчитанное значение квадрата коэффициента корреляции для градуировочной кривой каждого фрагментного иона каждого метаболита нитрофуранов не менее 0,98.
6.6 Хроматографические условия измерений
6.6.1 Хромато-масс-спектрометр включают и настраивают в соответствии с техническим руководством по его эксплуатации и устанавливают следующие хроматографические параметры:
- скорость потока элюента - 300 мм/мин;
- объем вводимой пробы - 10 мм.
Разделение проводят в режиме градиентного элюирования (приготовление растворов элюентов согласно 6.3.7): в начальный момент - соотношение фазы А/Б по объему (80/20), с 0,0 по 8,0 мин - градиентное элюирование к 95% фазы Б, с 8,0 по 10,0 мин - элюирование в 95% фазы Б, с 10,0 по 10,5 мин - переход к элюированию в фазе А/Б по объему (80/20), с 10,5 по 15,0 мин - уравновешивание колонки в фазе А/Б по объему (80/20).
6.6.2 Для настройки масс-спектрометрического детектора применяют следующие параметры:
- температура источника - 120°С;
- температура газа десольвации - 450°С;
- скорость потока газа десольвации - 650 дм/ч;
- скорость потока вспомогательного газа - 80 дм/ч.
6.7 Подготовка лабораторной посуды и реактивов
6.7.1 Мойку и сушку посуды следует проводить в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Не допускается проведение подготовки посуды в данном помещении для других видов анализов. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.7.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.7.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105°С до 110°С.
7 Порядок выполнения измерений
7.1 Обработка проб органов, тканей животных и креветок
7.1.1 Мышечную ткань предварительно очищают от грубой соединительной ткани и грубого хитинового покрова. 100 г мышечной ткани измельчают на гомогенизаторе и взвешивают по 1,0 г гомогенизированной ткани в полипропиленовой виале вместимостью 50 см.
7.1.2 Удаление несвязанных метаболитов*
________________
* При определении связанных (образующих комплексы с белками) метаболитов, до процедуры гидролиза и дереватизации, необходима предварительная отмывка образцов от несвязанных (находящихся в свободном состоянии) метаболитов. При определении общих метаболитов предварительную процедуру отмывки не используют.
В виалу с гомогенизированной тканью (см.7.1.1) добавляют 1 см деионизированной воды и 4 см
охлажденного метанола, тщательно встряхивают и помещают на предварительно охлажденную до 4°С центрифугу и центрифугируют при 2000 об/мин в течение 15 мин. После центрифугирования удаляют органический слой. Образец вновь промывают трижды, добавляя каждый раз по 4 см
охлажденного метанола и удаляя органический слой. Затем процедуру экстракции и центрифугирования повторяют: дважды с добавлением 4 см
охлажденного этилового спирта и дважды с добавлением 4 см
охлажденного серного эфира, также удаляя органические слои. Объединенные экстракты собирают в чистую виалу.
7.1.3 Для гидролиза и дериватизации в виалу с гомогенизированной тканью по 7.1.1 или в виалу с экстрактом по 7.1.2 добавляют 50 мм раствора внутреннего стандарта (см. 6.4.5), тщательно встряхивают и оставляют на 15 мин. Добавляют 5 см
соляной кислоты (см. 6.3.1) и 75 мм
раствора НБА в метаноле (см. 6.3.4). Виалу закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 10 мин, затем помещают на нагревательный модуль при температуре 37°С на 16 ч.
7.1.4 Для нейтрализации по истечении 16 ч виалу с образцом снимают с нагревательного модуля и охлаждают до комнатной температуры. После охлаждения добавляют 0,5 см раствора натрия фосфорнокислого додекагидрата по 6.3.5 и тщательно перемешивают. Доводят рН до значения 7,0 при помощи раствора гидроокиси натрия (см. 6.3.3). Вновь тщательно перемешивают и оставляют на 5 мин. Значение рН проверяют по индикаторной бумаге и, при необходимости, доводят до нужного значения.
7.1.5 Для экстракции нитрофенильных производных к нейтрализованному образцу добавляют 4 см этилацетата и интенсивно перемешивают на встряхивателе в течение 10 мин. Затем помещают на предварительно охлажденную до 4°С центрифугу и центрифугируют при 3000 об/мин в течение 15 мин. Органический слой количественно переносят в круглодонную колбу. Данную процедуру повторяют два раза. Объединенные экстракты упаривают на ротационном испарителе при температуре от 40°С до 45°С.
7.1.6 Для подготовки к хроматографическому анализу перерастворяют сухой остаток в этилацетате порциями по 2 см и переносят в стеклянную виалу вместимостью 4 см
. Помещают на нагревательный модуль и упаривают досуха*. Затем сухой остаток перерастворяют в 500 мм
растворителя (см. 6.3.8) на ультразвуковой бане и проводят удаление жировых фракций при помощи гексана. Для этого гексан добавляют в виалу дважды по 2 см
, встряхивают и центрифугируют при 1500 об/мин в течение 10 мин при комнатной температуре. Гексановые слои отбрасывают. Полученный очищенный экстракт фильтруют через мембранный фильтр в стеклянный вкладыш, помещают в стеклянную виалу вместимостью 2 см
и используют для ВЭЖХ-МС/МС анализа.
________________
* В случае неполного упаривания к образцу добавляют 1 см этилового спирта и вновь помещают на нагревательный модуль, упаривая досуха.
7.2 Обработка проб меда
7.2.1 Для очистки образцов к навеске меда массой 2,0 г, взвешенной в полимерной виале вместимостью 15 см на лабораторных весах, добавляют 5,0 см
соляной кислоты (см. 6.3.2) и тщательно перемешивают. Полученный раствор наносят на картридж для твердофазной экстракции.
Для проведения твердофазной экстракции картридж для ТФЭ заполняют 0,5 г сорбента. Предварительно картридж кондиционируют 2 см метанола и уравновешивают 2 см
деионизированной воды. Пробу элюируют с сорбента при помощи 2 см
деионизованной воды.
7.2.2 Для гидролиза и дериватизации в виалу с очищенным образцом по 7.2.1 добавляют 50 мм раствора внутреннего стандарта (см. 6.4.5), тщательно встряхивают и оставляют на 15 мин. Добавляют 5 см
соляной кислоты (см. 6.3.2) и 150 мм
раствора НБА в метаноле (см. 6.3.4). Виалу закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 10 мин, затем помещают на нагревательный модуль при температуре 37°С на 18 ч.
7.2.3 Процедуру нейтрализации образца осуществляют в соответствии с 7.1.4.
7.2.4 Для экстракции нитрофенильных производных картридж для ТФЭ предварительно кондиционируют 1 см метанола, уравновешивают 1 см
деионизированной воды, затем наносят нейтрализованный образец. После нанесения образца картридж промывают сначала 2 см
деионизированной воды, затем 2 см
смеси метанол/вода в объемном соотношении 30/70 и сушат в течение 20 мин под вакуумом. Элюируют нитрофенильные производные с картриджа при помощи 3 см
раствора, приготовленного по 6.3.6.
7.2.5 Перерастворение и подготовку к хроматографированию проводят в соответствии с 7.1.6.
7.3 Обработка проб яиц, молока и молочных продуктов
7.3.1 Подготовка проб к анализу
7.3.1.1 Яйца
Яйца отделяют от скорлупы и перемешивают на гомогенизаторе.
7.3.1.2 Молоко, сливки, сметана, кисломолочные напитки и продукты, сухие молочные продукты
Отобранные пробы перед исследованием тщательно перемешивают.
7.3.1.3 Сыр, творог, творожные изделия
10 г сыра, творога или творожных изделий взвешивают на часовом стекле, чашке Петри, переносят в ступку и тщательно растирают.
7.3.1.4 Масло
Перед исследованием пробу расплавляют на водяной бане при температуре 40°С-45°С и перемешивают до получения однородной эмульсии.
7.3.2 На лабораторных весах взвешивают 1,0 г подготовленной пробы в полимерной виале вместимостью 15 см. Добавляют 50 мм
раствора внутреннего стандарта (см. 6.4.5), тщательно перемешивают и оставляют на 15 мин. Добавляют 5 см
соляной кислоты (см. 6.3.1), 75 мм
раствора НБА (см. 6.3.4), закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 10 мин. Затем помещают на нагревательный модуль при температуре 37°С на 16 ч.
7.3.3 Для нейтрализации по истечении 16 ч виалу с образцом (см. 7.3.1) снимают с нагревательного модуля и охлаждают до комнатной температуры. После охлаждения добавляют 0,5 см раствора натрия фосфорнокислого додекагидрата (см. 6.3.5) и тщательно перемешивают. Доводят рН до значения 7,0 при помощи раствора гидроокиси натрия (см. 6.3.3). Вновь тщательно перемешивают и оставляют на 5 мин. Значение рН проверяют по индикаторной бумаге и, при необходимости, доводят до нужного значения.
7.3.4 Для экстракции нитрофенильных производных к образцу, обработанному согласно 7.3.2, добавляют 4 см этилацетата и интенсивно перемешивают на встряхивателе в течение 10 мин. Далее виалу с образцом помещают на предварительно охлажденную до 4°С центрифугу и центрифугируют при 3000 об/мин в течение 15 мин. Органический слой количественно переносят в круглодонную колбу. Описанную процедуру экстракции проделывают еще два раза. Объединенные экстракты упаривают на ротационном испарителе при температуре от 40°С до 45°С.
7.3.5 Перерастворение и подготовку к хроматографическому анализу проводят согласно 7.1.6.
7.4 ВЭЖХ-МС/МС анализ
7.4.1 Для определения остаточного содержания метаболитов нитрофуранов проводят анализ в условиях, указанных в 6.6.
7.4.2 Время удерживания метаболитов нитрофуранов определяют при анализе градуировочных растворов.
7.4.3 При анализе каждой партии проб проводят обработку "чистого образца" в соответствии с 7.1-7.3 в зависимости от типа исследуемой матрицы. Наличие пиков, значения времени удерживания которых совпадают со значениями времени удерживания пиков определяемых компонентов, указывает на наличие контаминации анализируемых образцов при подготовке проб.
7.5 Обработка результатов хроматографического анализа
7.5.1 Расчеты содержания метаболитов нитрофуранов выполняют с помощью градуировочной характеристики следующим образом. Вычисляют отношение площади пика фрагментного иона к площади внутреннего стандарта с помощью программы обработки спектров, поставляемой вместе с хромато-масс-спектрометром. Затем, используя установленную градуировочную характеристику (см. 6.5), рассчитывают значение массовой концентрации соответствующего метаболита в подготовленной пробе.
7.5.2 За окончательный результат измерений содержания метаболитов нитрофуранов принимают среднеарифметическое значение двух определений, выполненных в условиях повторяемости, округленное до целого числа и выраженное в микрограммах на килограмм (мкг/кг).
8 Метрологические характеристики
Установленный в настоящем стандарте метод обеспечивает выполнение измерений содержания метаболитов нитрофуранов с расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата 2, указанной в таблице 2.
Примечание - Значения относительной расширенной неопределенности, указанные в таблице 2, соответствуют границам относительной погрешности результатов измерений при 0,95.
Таблица 2 - Значения относительной расширенной неопределенности измерений (при коэффициенте охвата 2)
, %, в диапазонах измерений содержаний метаболитов нитрофуранов, мкг/кг
Метаболит | Относительная расширенная неопределенность | ||||
от 1,0 до 2,0 включ. | св. 2,0 до 5,0 включ. | св. 5,0 до 10,0 включ. | от 10,0 до 100,0 включ. | св. 100,0 до 1000,0 включ. | |
АОЗ | 36 | 34 | 21 | 18 | 14 |
АМОЗ | 43 | 36 | 26 | 19 | 14 |
АГД | 44 | 30 | 25 | 22 | 13 |
СЕМ | 56 | 40 | 22 | 22 | 11 |
9 Оформление результатов измерений
9.1 Результат анализа в документах, предусматривающих его использование, представляют в виде
![]() , (1)
, (1)
где - среднеарифметическое значение двух параллельных измерений содержания
-го метаболита в анализируемой пробе, мкг/кг;
- расширенная неопределенность при коэффициенте охвата
2 определения содержания
-го метаболита нитрофуранов, определяемая по формуле (2), мкг/кг.
9.2 Значения расширенной неопределенности измерения рассчитывают с использованием значений относительной расширенной неопределенности при 2 (в соответствии с таблицей 2) по формуле
![]() , (2)
, (2)
где - среднеарифметическое значение двух параллельных измерений содержания
-го метаболита в анализируемой пробе, мкг/кг;
- значение относительной расширенной неопределенности содержания
-го метаболита нитрофуранов для соответствующего диапазона измерений, % (таблица 2).
10 Контроль качества результатов измерений
10.1 Контроль полноты извлечения внутреннего стандарта нитрофуранов и их метаболитов
10.1.1 Контроль извлечения внутренних стандартов нитрофуранов и их метаболитов выполняют в ходе каждого измерения (получения результата количественного химического анализа при соблюдении требований настоящего стандарта).
10.1.2 Рассчитанные программным обеспечением значения извлечения внутренних стандартов должны находиться в диапазоне от 40% до 130%. Если рассчитанное значение извлечения ниже или выше указанного диапазона, то результаты измерения содержания метаболита не принимают за окончательный результат. Проводят повторные исследования анализируемых проб.
10.2 Контроль неопределенности результатов измерений
При проведении испытаний рекомендуется в ходе анализа каждой партии образцов с использованием стандартной процедуры пробоподготовки (см. 7.1, 7.3) проводить анализ градуировочных растворов, приготовленных в соответствии с 6.4. Результаты измерений признают удовлетворительными при выполнении следующего неравенства:
![]() , (3)
, (3)
где - рассчитанное с помощью градуировочной характеристики значение содержания
-го метаболита в градуировочном растворе, мкг/кг;
- значение содержания
-го метаболита по паспорту на стандартный образец, мкг/кг;
- значение относительной расширенной неопределенности содержания
-го метаболита нитрофуранов для соответствующего диапазона измерений (таблица 2), %.
Приложение А
(справочное)
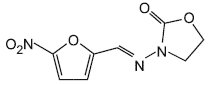
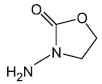
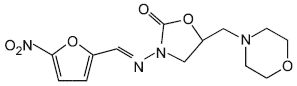
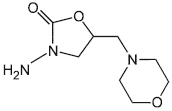
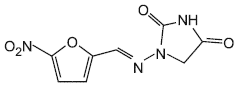
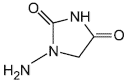
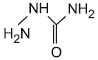
Молекулярные структуры нитрофуранов и их метаболитов
А.1 Молекулярные структуры нитрофуранов и их метаболитов приведены на рисунке А.1.
|
|
Фуразолидон | АОЗ |
|
|
Фуралтадон | АМОЗ |
|
|
Фурадонин | АГД |
|
|
Фурацилин | СЕМ |
а - нитрофураны | б - метаболиты |
Рисунок А.1
Приложение Б
(обязательное)
Контроль стабильности результатов измерений
Периодичность контроля стабильности результатов измерений регламентируют в руководстве по качеству лаборатории*.
________________
* Документ в информационных продуктах не содержится. За информацией о документе Вы можете обратиться в Службу поддержки пользователей. - .
Контроль стабильности результатов измерений в лаборатории при реализации методики осуществляют по ГОСТ Р ИСО 5725-6, используя контроль стабильности среднеквадратического (стандартного) отклонения промежуточной прецизионности рутинного анализа с изменяющимися факторами "время" и "оператор".
Применяя метод контрольных карт Шухарта, проверяют стабильность этих результатов измерений и оценивают стандартное отклонение промежуточной прецизионности с изменяющимися факторами "время" и "оператор". После отбора испытуемую пробу от каждой партии подготавливают в лаборатории для анализа. Одну пробу, подвергавшуюся анализу во время смены , анализирует повторно другой оператор в другую смену
, и результаты сравнивают. Значение стандартного отклонения промежуточной прецизионности
![]() устанавливают в лаборатории по результатам измерений за предыдущий период. Параметры контрольной карты пределов для каждого диапазона рассчитывают следующим образом:
устанавливают в лаборатории по результатам измерений за предыдущий период. Параметры контрольной карты пределов для каждого диапазона рассчитывают следующим образом:
- среднюю линию по формуле
![]() , (Б.1)
, (Б.1)
где ![]() - среднеквадратическое отклонение промежуточной прецизионности, %;
- среднеквадратическое отклонение промежуточной прецизионности, %;
- верхний предел действия по формуле
![]() ; (Б.2)
; (Б.2)
- верхний предел предупреждения по формуле
![]() . (Б.3)
. (Б.3)
Расхождение рассчитывают по формуле
![]() . (Б.4)
. (Б.4)
Расхождение наносят на карту в течение контролируемого периода.
Рекомендуется устанавливать контролируемый период так, чтобы количество результатов контрольных измерений было от 20 до 30. После этого проводят оценку стандартного отклонения промежуточной прецизионности ![]() результатов по формуле
результатов по формуле
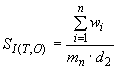 , (Б.5)
, (Б.5)
где - число измерений.
Полученное значение ![]() используют для последующего контроля стабильности результатов измерений.
используют для последующего контроля стабильности результатов измерений.
Библиография
[1] | Правила устройства и безопасной эксплуатации сосудов, работающих под давлением |
[2] | Методические указания по отбору проб пищевой продукции животного и растительного происхождения, кормов, кормовых добавок с целью лабораторного контроля их качества и безопасности |
УДК 664.002.3.001.4:006.354 | ОКС | 67.050 | Н | 09 | |
67.100 | 19 | ||||
67.120 | 11 | ||||
Ключевые слова: пищевые продукты, продовольственное сырье, метаболиты нитрофуранов, метод определения содержания с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием | |||||
Электронный текст документа
и сверен по:
, 2011