ГОСТ Р 58614-2019
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Продукция пищевая специализированная
Метод ВЭЖХ после очистки на иммуноаффинной колонке с предколоночной дериватизацией с флуориметрическим детектированием
ОКС 67.050
Дата введения 2020-04-01
Предисловие
1 РАЗРАБОТАН Федеральным государственным унитарным предприятием "Российский научно-технический центр информации по стандартизации, метрологии и оценке соответствия" (ФГУП "")
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 036 "Продукция специализированная пищевая"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2019 г. N 844-ст
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. N 162-ФЗ "О стандартизации в Российской Федерации". Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе "Национальные стандарты", а официальный текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет ()
1 Область применения
Дополнительная информация о валидации приведена в разделе 8 и в приложении А.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.1.005 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.4.021 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
ГОСТ 1770 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4517 Реактивы. Методы приготовления вспомогательных реактивов и растворов, применяемых при анализе
ГОСТ 4919.2 Реактивы и особо чистые вещества. Методы приготовления буферных растворов
ГОСТ 6709 Вода дистиллированная. Технические условия
ГОСТ 6995 Реактивы. Метанол-яд. Технические условия
ГОСТ 12026 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 25336 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 33303 Продукты пищевые. Методы отбора проб для определения микотоксинов
ГОСТ ISO 7886-1 Шприцы инъекционные однократного применения стерильные. Часть 1. Шприцы для ручного использования
ГОСТ OIML R 76-1 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ Р 52501 Вода для лабораторного анализа. Технические условия
ГОСТ Р ИСО 5725-1 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ Р ИСО 5725-2 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений. Если заменен ссылочный стандарт, на который дана датированная ссылка, то рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия). Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется применять в части, не затрагивающей эту ссылку.
3 Краткое описание
Фумонизины экстрагируют из пробы смесью цитратно-фосфатного буферного раствора, метанола и ацетонитрила. Отфильтрованный экстракт разбавляют водой и пропускают через иммуноаффинную колонку, содержащую специфические антитела к фумонизинам. Фумонизины элюируют с колонки метанолом и водой и определяют их количество с помощью ВЭЖХ с ФЛД с предварительной дериватизацией с помощью реагента ортофталевого диальдегида (ОФА).
4 Реактивы
Если не указано иное, используют только химические чистые реактивы, например по ГОСТ 4919.2, для анализа (ч.д.а) и воду степени чистоты 1 в соответствии с ГОСТ Р 52501. Кроме того, чистота растворителей должна быть не ниже степени чистоты для ВЭЖХ. Можно использовать имеющиеся на рынке растворы, свойства которых эквивалентны вышеуказанным.
ВНИМАНИЕ! Утилизация отходов растворителя должна быть произведена в соответствии с действующими законами в области защиты окружающей среды и нормативными актами об охране окружающей среды.
4.1 Ацетонитрил.
ВНИМАНИЕ! Ацетонитрил является опасным веществом. Пробы, отобранные в соответствии с ГОСТ 33303, взбалтывают с помощью орбитального шейкера в вытяжном шкафу. После взбалтывания пробы должны быть отфильтрованы в вытяжном шкафу.
4.2 Метанол.
4.3 Ортофталевый диальдегид (ОФА).
4.6 2-меркаптоэтанол.
4.7 Раствор цитратно-фосфатный буферный.
Один объем раствора лимонной кислоты (4.4) смешивают с одним объемом раствора натрия фосфорнокислого двухзамещенного (4.5).
4.8 Экстрагент.
Два объема цитрат-фосфатного буферного раствора (4.7) смешивают с одним объемом метанола по ГОСТ 6995 (4.2) и одним объемом ацетонитрила (4.1).
4.9 Кислота ледяная уксусная.
4.11 Смесь А, состоящая из ацетонитрила и воды.
Один объем ацетонитрила (4.1) смешивают с одним объемом воды. Этот растворитель используют для приготовления растворов по ГОСТ 4517 для доведения до необходимого объема.
4.12 Смесь В, состоящая из ацетонитрила и воды.
Три объема ацетонитрила (4.1) смешивают с семью объемами воды. Этот растворитель используют для приготовления градуировочных растворов и для повторного разведения высушенных экстрактов после очистки на иммуноаффинной колонке.
4.14 Раствор ОФА-реагента.
4.15 Подвижная фаза для ВЭЖХ.
4.15.1 Подвижная фаза А для ВЭЖХ.
30 объемов ацетонитрила (4.1) смешивают с 69 объемами воды и одним объемом ледяной уксусной кислоты (4.9).
4.15.2 Подвижная фаза В для ВЭЖХ.
60 объемов ацетонитрила (4.1) смешивают с 39 объемами воды и одним объемом ледяной уксусной кислоты (4.9).
4.16 Колонка иммуноаффинная.
ВНИМАНИЕ! Фумонизины являются нефротоксическими, гепатотоксическими и канцерогенными соединениями для крыс и мышей и считаются Международным агентством по изучению рака (IARC) потенциально канцерогенными для человека. С этими препаратами следует обращаться с особой осторожностью. Перчатки и защитные очки следует использовать в течение всех исследований, и все этапы подготовки стандартных растворов и растворов проб должны быть выполнены в вытяжном шкафу в соответствии с ГОСТ 12.1.005, ГОСТ 12.1.007, ГОСТ 12.4.021.
4.21 Растворы градуировочные смеси фумонизинов для ВЭЖХ.
Таблица 1 - Приготовление градуировочных растворов смеси фумонизинов для ВЭЖХ
Градуировочный раствор для ВЭЖХ | Разбавленный основной раствор смеси ФВ (4.20) мм | Конечная концентрация градуировочных растворов смеси ФВ (4.21) | Эквивалентные количества и в пробе | ||
|
| , мкг/см | , мкг/см | , мкг/кг | , мкг/кг |
1 | 100 | 0,04 | 0,01 | 20,0 | 5,0 |
2 | 200 | 0,08 | 0,02 | 40,0 | 10,0 |
3 | 400 | 0,16 | 0,04 | 80,0 | 20,0 |
4 | 1000 | 0,40 | 0,10 | 200,0 | 50,0 |
5 | 2400 | 0,96 | 0,24 | 480,0 | 120,0 |
Для экстракта пробы, повторно растворенной в 500 мкл смеси В, состоящей из ацетонитрила и воды (4.12). | |||||
5 Оборудование
Используют лабораторную посуду и лабораторное оборудование по ГОСТ 25336.
5.1 Весы аналитические, пригодные для взвешивания, предел погрешности 0,0001 г.
5.2 Весы лабораторные по ГОСТ OIML R 76-1, пригодные для взвешивания, предел погрешности до 0,1 г.
5.3 Баня водяная с регулируемым термостатом.
5.5 Встряхиватель лабораторный орбитальный.
5.6 Центрифуга, обеспечивающая центробежное ускорение до 3000 g.
5.10 Устройство для вакуумной фильтрации с возможностью присоединения иммуноаффинных колонок (4.16).
5.12 Насос вакуумный.
5.13 Бумага фильтровальная по ГОСТ 12026, например качественная, прочная, быстрой пропускной способности, диаметром 24 см и размером пор 30 мкм или аналогичная.
5.14 Фильтры из стеклянного микроволокна размером пор 1,6 мкм или аналогичные.
5.15 Блок нагревательный с подачей азота или воздуха.
5.19 Встряхиватель типа "Вортекс" или аналогичное перемешивающее устройство.
5.20 Система для ВЭЖХ в указанной ниже комплектации.
5.20.1 Система ввода проб.
5.20.3 Пробоотборник автоматический, способный выполнять автоматическую предколоночную дериватизацию с ОФА-реагентом, указанным в 6.4.1.
По результатам исследований признаны подходящими колонки С18 SymmetryShield компании Waters, Zorbax SB-C18 компании Agilent или аналогичные колонки.
5.20.5 Термостат колонок, который может работать при температуре 20°С.
Примечание - Колонки С18, заполненные обращенно-фазовым сорбентом, также могут быть использованы при комнатной температуре.
5.20.6 Детектор флуоресцентный, снабженный проточной кюветой, позволяющий проводить измерения при длине волны возбуждения 335 нм и длине волны эмиссии 440 нм.
5.20.7 Устройство записывающее, интегратор или система компьютерная обработки данных.
5.21 Настройки линейного градиента.
Условия градиента представлены в таблице 2.
Таблица 2 - Условия для градиентного элюирования
Время, мин | Скорость потока, | Подвижная фаза А, | Подвижная фаза В, |
| см /мин | % | % |
0,00 | 1,00 | 60 | 40 |
5,00 | 1,00 | 60 | 40 |
26,00 | 1,00 | 12 | 88 |
29,00 | 1,00 | 12 | 88 |
29,10 | 1,00 | - | 100 |
30,00 | 1,00 | - | 100 |
30,10 | 1,00 | 60 | 40 |
38,00 | 1,00 | 60 | 40 |
6 Проведение испытания
6.1 Экстракция
Пробу измельчают до величины частиц, проходящих сквозь сито с отверстиями размером 0,5 мм, а затем тщательно перемешивают, для того чтобы обеспечить однородную консистенцию.
6.2 Очистка экстракта на иммуноафинной колонке
6.3 Метод искусственного внесения фумонизинов
6.4 Дериватизация и количественное определение с помощью ВЭЖХ
6.4.1 Программа автоматизированной предколоночной дериватизации
Показано, что перечисленные ниже условия обеспечивают удовлетворительные результаты.
6.4.2 ВЭЖХ-анализ
6.4.3 Идентификация пиков
6.4.4 Определение
7 Расчеты
D - коэффициент разведения, который может быть применен;
8 Точность метода
8.1 Общие положения
Подробная информация о межлабораторных испытаниях для определения точности метода приведена в таблицах А.1-А.3 приложения А. Значения, полученные в результате этих межпабораторных испытаний, не обязательны для применения к другим диапазонам концентраций и/или другим типам матриц, отличным от тех, которые указаны в приложении В.
8.2 Повторяемость
Абсолютное расхождение между результатами двух отдельно проведенных испытаний, полученных одним лаборантом на идентичном материале для исследований с использованием такого же оборудования в течение короткого промежутка времени, не должно превышать предела повторяемости r более чем в 5% случаев (ГОСТ Р ИСО 5725-1, ГОСТ Р ИСО 5725-2).
мкг/кг, | r=51,0 мкг/кг | (искусственно контаминированные); |
мкг/кг, | r=56,6 мкг/кг | (искусственно контаминированные); |
мкг/кг, | r=135,5 мкг/кг | (естественно контаминированные); |
мкг/кг, | r=126,3 мкг/кг | (естественно контаминированные); |
мкг/кг, | r=107,5 мкг/кг | (естественно контаминированные). |
мкг/кг, | r=40,3 мкг/кг | (искусственно контаминированные); |
мкг/кг, | r=45,4 мкг/кг | (искусственно контаминированные); |
мкг/кг, | r=16,2 мкг/кг | (естественно контаминированные); |
мкг/кг, | r=51,2 мкг/кг | (естественно контаминированные); |
мкг/кг, | r=91,3 мкг/кг | (естественно контаминированные). |
мкг/кг, | r=13,2 мкг/кг | (искусственно контаминированные); |
мкг/кг, | r=11,5 мкг/кг | (искусственно контаминированные); |
мкг/кг, | r=22,1 мкг/кг | (естественно контаминированные); |
мкг/кг, | r=18,2 мкг/кг | (естественно контаминированные); |
мкг/кг, | r=17,6 мкг/кг | (естественно контаминированные). |
8.3 Воспроизводимость результатов
Абсолютное расхождение между результатами двух отдельно проведенных испытаний, полученных в двух лабораториях на идентичном материале для исследований, не должно превышать предела повторяемости R более чем в 5% случаев (ГОСТ Р ИСО 5725-1, ГОСТ Р ИСО 5725-2).
мкг/кг, | R=83,2 мкг/кг | (искусственно контаминированные); |
мкг/кг, | R=136,9 мкг/кг | (искусственно контаминированные); |
мкг/кг, | R=157,1 мкг/кг | (естественно контаминированные); |
мкг/кг, | R=218,1 мкг/кг | (естественно контаминированные); |
мкг/кг, | R=213,4 мкг/кг | (естественно контаминированные). |
мкг/кг, | R=65,2 мкг/кг | (искусственно контаминированные); |
мкг/кг, | R=107,2 мкг/кг | (искусственно контаминированные); |
мкг/кг, | R=127,1 мкг/кг | (естественно контаминированные); |
мкг/кг, | R=132,2 мкг/кг | (естественно контаминированные); |
мкг/кг, | R=165,5 мкг/кг | (естественно контаминированные). |
мкг/кг, | R=23,0 мкг/кг | (искусственно контаминированные); |
мкг/кг, | R=32,2 мкг/кг | (искусственно контаминированные); |
мкг/кг, | R=34,7 мкг/кг | (естественно контаминированные); |
мкг/кг, | R=44,0 мкг/кг | (естественно контаминированные); |
мкг/кг, | R=58,5 мкг/кг | (естественно контаминированные). |
9 Протокол испытаний
Протокол испытаний должен содержать следующие минимальные данные:
- информация, необходимая для идентификации пробы (вид пробы, ее происхождение, наименование пробы);
- ссылка на настоящий стандарт;
- дата и способ отбора пробы (если известны);
- дата поступления пробы в лабораторию;
- дата проведения испытания;
- результаты испытания с указанием единиц измерения;
- все особенности, установленные в ходе проведения испытания;
- все операции, не установленные в методике или рассматриваемые как необязательные и которые могут повлиять на результат испытания.
Приложение А
(справочное)
Данные о точности метода
Данные, приведенные в таблицах А.1-А.3, получены в результате межлабораторных испытаний, которые проводились в соответствии с протоколом испытания на предмет установления ценности параметров аналитических методов.
Проба | 1 | 2 | 3 | 4 | 5 |
Год проведения межлабораторного испытания | 2009 | 2009 | 2009 | 2009 | 2009 |
Количество лабораторий-участников | 10 | 10 | 10 | 10 | 10 |
Количество лабораторий, оставшихся после исключения допустивших ошибки | 8 | 10 | 10 | 10 | 9 |
Количество лабораторий, допустивших ошибки | 2 | 0 | 0 | 0 | 1 |
Количество принятых результатов | 16 | 20 | 20 | 20 | 18 |
Среднее арифметическое , мкг/кг | 111,6 | 293,4 | 211,2 | 322,5 | 458,0 |
Стандартное отклонение повторяемости , мкг/кг | 18,2 | 20,2 | 48,4 | 45,1 | 38,4 |
Относительное стандартное отклонение повторяемости , % | 16,3 | 6,9 | 22,9 | 14,0 | 8,4 |
Предел повторяемости , мкг/кг | 51,0 | 56,6 | 135,5 | 126,3 | 107,5 |
Стандартное отклонение воспроизводимости , мкг/кг | 29,7 | 48,8 | 56,1 | 77,9 | 76,2 |
Относительное стандартное отклонение воспроизводимости , % | 26,6 | 16,6 | 26,6 | 24,1 | 16,6 |
Предел воспроизводимости , мкг/кг | 83,2 | 136,9 | 157,1 | 218,1 | 213,4 |
Полнота извлечения, % | 89 | 94 | - | - | - |
Значение HorRat | 1,2 | 0,9 | 1,3 | 1,3 | 0,9 |
Значение HorRat | 1,2 | 0,9 | 1,3 | 1,3 | 0,9 |
Проба, искусственно внесенная Bambix fijne granen, содержит пшеницу, овес, рис, просо, ячмень, кукурузу и рожь. Проба, искусственно внесенная (мука из обработанной амилазой кукурузы и тапиоки, специи и витамин ). Проба, естественно загрязненная (печенья, содержащие пшеницу, ячмень, рожь, рис и кукурузу). Проба, естественно загрязненная (сухое молоко, растительное масло, рис, кукуруза, сахар, минералы и витамины). Проба, естественно загрязненная (предварительно приготовленная мука из пшеницы, овса, ржи, ячменя, риса, проса и кукурузы). Одна лаборатория из первоначальных 11 лабораторий-участников исключена из-за полученных в ней недействительных результатов. | |||||
Проба | 1 | 2 | 3 | 4 | 5 |
Год проведения межлабораторного испытания | 2009 | 2009 | 2009 | 2009 | 2009 |
Количество лабораторий-участников | 10 | 10 | 10 | 10 | 10 |
Количество лабораторий, оставшихся после исключения допустивших ошибки | 8 | 10 | 10 | 9 | 9 |
Количество лабораторий, допустивших ошибки | 2 | 0 | 0 | 1 | 1 |
Количество принятых результатов | 16 | 20 | 20 | 18 | 18 |
Среднее арифметическое , мкг/кг | 89,1 | 240,1 | 176,7 | 257,6 | 384,4 |
Стандартное отклонение повторяемости , мкг/кг | 14,4 | 16,2 | 41,5 | 18,3 | 32,6 |
Относительное стандартное отклонение повторяемости , % | 16,2 | 6,8 | 23,5 | 7,1 | 8,5 |
Предел повторяемости , мкг/кг | 40,3 | 45,4 | 116,2 | 51,2 | 91,3 |
Стандартное отклонение воспроизводимости , мкг/кг | 23,3 | 38,3 | 45,4 | 47,2 | 59,1 |
Относительное стандартное отклонение воспроизводимости , % | 26,2 | 16,0 | 25,7 | 18,3 | 15,4 |
Предел воспроизводимости , мкг/кг | 65,2 | 107,2 | 127,1 | 132,2 | 165,5 |
Полнота извлечения, % | 89 | 96 | - | - | - |
Значение HorRat | 1,1 | 0,8 | 1,2 | 0,9 | 0,8 |
Значение HorRat | 1,2 | 0,8 | 1,2 | 0,9 | 0,8 |
Проба, искусственно внесенная Bambix fijne granen, содержит пшеницу, овес, рис, просо, ячмень, кукурузу и рожь. Проба, искусственно внесенная (мука из обработанной амилазой кукурузы и тапиоки, специи и витамин ). Проба, естественно загрязненная (печенья, содержащие пшеницу, ячмень, рожь, рис и кукурузу) Проба, естественно загрязненная (сухое молоко, растительное масло, рис, кукуруза, сахар, минералы и витамины). Проба, естественно загрязненная (предварительно приготовленная мука из пшеницы, овса, ржи, ячменя, риса, проса и кукурузы). Одна лаборатория из первоначальных 11 лабораторий-участников исключена из-за полученных в ней недействительных результатов. | |||||
Проба | 1 | 2 | 3 | 4 | 5 |
Год проведения межлабораторного испытания | 2009 | 2009 | 2009 | 2009 | 2009 |
Количество лабораторий-участников | 10 | 10 | 10 | 10 | 10 |
Количество лабораторий, оставшихся после исключения допустивших ошибки | 8 | 10 | 10 | 9 | 9 |
Количество лабораторий, допустивших ошибки | 2 | 0 | 0 | 1 | 1 |
Количество принятых результатов | 16 | 20 | 20 | 18 | 18 |
Среднее арифметическое , мкг/кг | 22,5 | 53,3 | 34,5 | 50,8 | 73,6 |
Стандартное отклонение повторяемости , мкг/кг | 4,7 | 4,1 | 7,9 | 6,5 | 6,3 |
Относительное стандартное отклонение повторяемости , % | 21,0 | 7,6 | 22,9 | 12,9 | 8,6 |
Предел повторяемости , мкг/кг | 13,2 | 11,5 | 22,1 | 18,2 | 17,6 |
Стандартное отклонение воспроизводимости , мкг/кг | 8,2 | 11,5 | 12,4 | 15,7 | 20,9 |
Относительное стандартное отклонение воспроизводимости , % | 36,3 | 21,6 | 36,0 | 30,8 | 28,4 |
Предел воспроизводимости , мкг/кг | 23,0 | 32,2 | 34,7 | 44,0 | 58,5 |
Полнота извлечения, % | 90 | 85 | - | - | - |
Значение HorRat | 1,3 | 0,9 | 1,4 | 1,2 | 1,2 |
Значение HorRat | 1,7 | 1,0 | 1,6 | 1,4 | 1,3 |
Проба, искусственно внесенная Bambix fijne granen, содержит пшеницу, овес, рис, просо, ячмень, кукурузу и рожь. Проба, искусственно внесенная (мука из обработанной амилазой кукурузы и тапиоки, специи и витамин ). Проба, естественно загрязненная (печенья, содержащие пшеницу, ячмень, рожь, рис и кукурузу). Проба, естественно загрязненная (сухое молоко, растительное масло, рис, кукуруза, сахар, минералы и витамины). Проба, естественно загрязненная (предварительно приготовленная мука из пшеницы, овса, ржи, ячменя, риса, проса и кукурузы). Одна лаборатория из первоначальных 11 лабораторий-участников исключена из-за полученных в ней недействительных результатов. | |||||
Приложение Б
(справочное)
Примеры типичных хроматограмм
 |
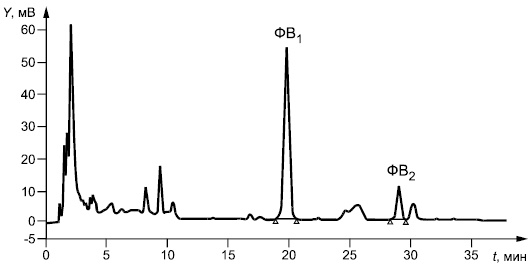 |
Приложение В
(справочное)
Сравнение методов по определению фумонизинов в зернах кукурузы, изложенных в настоящем стандарте, с методами, приведенными в ГОСТ EN 13585 и в ГОСТ EN 14352
Таблица В.1 - Сравнение методов, изложенных в настоящем стандарте, в ГОСТ EN 13585 и в ГОСТ EN 14352
Фумонизины | Метод, изложенный в настоящем стандарте | ГОСТ EN 14352 | ГОСТ EN 13585 | ||||
| Среднее значение, мкг/кг | , % | Среднее значение, мкг/кг | , % | Среднее значение, мкг/кг | , % | |
Измельченные цельные | 580,6 | 9 | 612,5 | 12 | 648,9 | 7 | |
зерна кукурузы (размер | 485,0 | 10 | 498,3 | 11 | 509,9 | 7 | |
частиц <500 мкм) | 95,6 | 9 | 114,2 | 15 | 139,0 | 8 | |
Измельченные цельные | 804,3 | 8 | 791,5 | 12 | 635,9 | 7 | |
зерна кукурузы (размер | 640,3 | 8 | 619,1 | 14 | 500,9 | 7 | |
частиц >500 мкм) | 164,0 | 9 | 172,4 | 6 | 135,0 | 8 | |
Кукурузная мука (размер | 210,6 | 5 | 204,5 | 3 | 161,1 | 10 | |
частиц от 350 мкм до 500 | 175,2 | 5 | 166,9 | 3 | 135,1 | 12 | |
мкм) | 35,4 | 6 | 37,6 | 3 | 26,0 | 5 | |
Кукурузная мука (размер | 3148,1 | 8 | 3264,3 | 4 | 2276,9 | 5 | |
частиц <350 мкм) | 2561,3 | 9 | 2642,6 | 4 | 1868,8 | 5 | |
586,8 | 7 | 621,7 | 6 | 408,1 | 8 | ||
Среднее содержание фумонизинов различается в значительной мере ( Р <0,05, анализ однофакторной дисперсии по Туки с пост-тестом, параметрический тест) от тех, у которых есть сноска b в той же строке. Фумонизины экстрагируют из измельченных зерен кукурузы смесью, состоящей из воды-ацетонитрила-метанола, а отфильтрованный экстракт очищают на иммуноаффинной колонке согласно ГОСТ EN 14352. Среднее содержание фумонизинов различается в значительной мере ( Р <0,05, анализ однофакторной дисперсии по Туки с пост-тестом, параметрический тест) от тех, у которых есть сноска а или b в той же строке. Фумонизины экстрагируют из измельченных зерен кукурузы смесью, состоящей из воды и метанола, а отфильтрованный экстракт очищают на колонке с насыщенной анионообменной смолой согласно ГОСТ EN 13585. Среднее содержание фумонизинов различается в значительной мере ( Р <0,05, анализ однофакторной дисперсии по Туки с пост-тестом, параметрический тест) от тех, у которых есть сноска а в той же строке. | |||||||
УДК 543.6:006.354 | ОКС 67.050 |
Ключевые слова: продукция пищевая специализированная, определение фумонизина , определение фумонизина , продукция для питания детей раннего возраста, пищевые продукты на основе кукурузы, метод ВЭЖХ, очистка на иммуноаффинной колонке, флуоресцентное детектирование, предколоночная дериватизация | |
