ГОСТ ISO 8638-2012
Группа Р24
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
КОМПЛЕКТ КРОВОПРОВОДЯЩИХ МАГИСТРАЛЕЙ ДЛЯ ГЕМОДИАЛИЗАТОРОВ, ГЕМОФИЛЬТРОВ И ГЕМОКОНЦЕНТРАТОРОВ
Технические требования и методы испытаний
Extracorporeal blood circuit for haemodialysers, haemofilters and haemoconcentrators. Technical requirements and test methods
МКС 11.040.020*
______________
* По данным официального сайта Росстандарт
ОКС 11.040.20, здесь и далее по тексту. -
.
Дата введения 2015-01-01
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием "Всероссийский научно-исследовательский институт стандартизации и сертификации в машиностроении" (ВНИИНМАШ)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол N 41-2012 от 24 мая 2012 г.)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Азербайджан | AZ | Азстандарт |
Армения | AM | Минторгэкономразвития |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Кыргызстан | KG | Кыргызстандарт |
Молдова | MD | Молдова-Стандарт |
Российская Федерация | RU | Ростехрегулирование |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
Украина | UA | Госпотребстандарт Украины |
4 Приказом Федерального агентства по техническому регулированию и метрологии от "19" декабря 2012 г. N 1926-ст межгосударственный стандарт ГОСТ ISO 8638-2012 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2015 г.
5 Настоящий стандарт идентичен международному стандарту ISO 8638:1989* Extra-corporeal blood circuit for haemodialysers, haemofilters and haemoconcentrators (Комплект кровопроводящих магистралей для гемодиализаторов, гемофильтров и гемоконцентраторов).
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Степень соответствия - идентичная (IDT).
Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам приведены в дополнительном приложении ДА.
Стандарт подготовлен на основе применения ГОСТ Р ИСО 8638-99
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта публикуется в указателе "Национальные стандарты".
Информация об изменениях к настоящему стандарту публикуется в указателе "Национальные стандарты", а текст изменений - в информационных указателях "Национальные стандарты". В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в информационном указателе "Национальные стандарты"
Введение
Настоящий стандарт распространяется на комплект кровопроводящих магистралей (далее - комплект), предназначенный для однократного применения и используемый с гемодиализаторами, гемофильтрами и гемоконцентраторами при экстракорпоральной перфузии. Приведенные в настоящем стандарте требования к комплекту способствуют обеспечению его безопасной и эффективной эксплуатации.
Установлено, что нецелесообразно определять свойства конструкционных материалов магистралей комплекта, а также устанавливать методы испытания на биосовместимость, стерильность, апирогенность и некоторые эксплуатационные характеристики. Поэтому настоящий стандарт требует, чтобы материалы, из которых изготовляют магистрали, были испытаны и информация по методам этих испытаний, наряду с полученными результатами, предоставлялась по запросу.
Требования к физическим величинам были ограничены теми значениями, которые необходимы для безопасного и эффективного функционирования устройства. При разработке проектно-конструкторской и нормативной документации необходимо учитывать конструктивную совместимость магистралей в части соединения с кровопроводящими полостями гемодиализаторов, гемофильтров и гемоконцентраторов, а также с устройствами сосудистого доступа. Технические требования настоящего стандарта к указанным соединениям были выбраны для минимизации риска утечки крови и доступа воздуха. Допускается использование указанных соединений как с резьбовыми блокирующими колпачками, так и без них.
1 Область применения
Настоящий стандарт устанавливает требования к комплекту кровопроводящих магистралей (далее - комплекту), предназначенному для однократного применения и используемому с гемодиализаторами, гемофильтрами и гемоконцентраторами.
Стандарт не определяет свойства конструкционных материалов, не устанавливает методы испытаний на биосовместимость, стерильность, апирогенность и отдельные эксплуатационные характеристики. Обоснование их исключения дано во "Введении".
Настоящий стандарт распространяется на комплект кровопроводящих магистралей однократного применения, состоящий из артериальной и венозной магистрали.
Стандарт не распространяется на гемодиализаторы, гемофильтры, гемоконцентраторы, устройства сосудистого доступа, перфузионные насосы, мониторы измерения давления и контроля воздушных включений в магистралях, гемодиализные и гемофильтрационные аппараты, а также аппараты для гемоконцентрации.
Примечание - Требования к гемодиализаторам, гемофильтрам и гемоконцентраторам определяет ISO 8637.
Требования настоящего стандарта являются обязательными.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты*:
________________
* Таблицу соответствия национальных стандартов международным см. по ссылке. - .
ISO 8637:1989 Haemodialysers, haemofilters and haemoconcentrators (Гемодиализаторы, гемофильтры и гемоконцентраторы)
ISO 472:1979 Plastics. Vocabulary Bilingual edition (Пластики. Словарь двуязычный)
ISO 594-2:1991 Conical fittings with a 6% (Luer) taper for syringes, needles and certain other medical equipment. Part 2. Lock fittings (Детали соединительные с конусностью 6% (Люэра) для шприцев, игл и другого медицинского оборудования. Часть 2. Люэровские наконечники)
ISO 7000:1989 Graphical symbols for use on equipment. Index and synopsis (Графические символы, наносимые на оборудование. Перечень и сводная таблица)
3 Определения
В настоящем стандарте применяют следующие термины с соответствующими определениями:
3.1 магистраль кровопроводящая артериальная: Составная часть экстракорпоральной системы, обеспечивающая соединение устройства сосудистого доступа пациента с входом полости по крови гемодиализатора, гемофильтра или гемоконцентратора.
3.2 апирогенность: Отсутствие пирогенов в пределах погрешности контроля для методов испытаний, которые приводятся в соответствующих государственных стандартах и описывают поддержание данного состояния с помощью защитных мер.
3.3 насосный сегмент: Составная часть кровопроводящей магистрали, обеспечивающая совместно с перфузионным насосом транспортирование крови в экстракорпоральной системе.
3.4 стерильность: Отсутствие живых микроорганизмов при проверках на стерильность и поддержание данного состояния с помощью защитных мер.
3.5 магистраль кровопроводящая венозная: Составная часть экстракорпоральной системы, обеспечивающая соединение выхода полости по крови гемодиализатора, гемофильтра или гемоконцентратора с устройством сосудистого доступа пациента.
4 Требования
4.1 Условия качественного производства
Магистрали комплекта следует изготовлять в условиях чистого производства.
Внутренняя поверхность магистралей должна быть свободна от видимых посторонних частиц. Испытание проводят в соответствии с 5.1.
4.2 Токсикология и биологическая совместимость
Магистрали комплекта должны быть нетоксичны.
Токсикологические испытания магистралей проводят в соответствии с действующим нормативным документом, утвержденным в установленном порядке, и по запросу информация о методе испытаний и результаты испытаний магистралей могут быть предоставлены изготовителем.
Испытание проводят в соответствии с 5.2.
4.3 Стерильность
Магистрали комплекта должны поставляться в стерильном виде. Испытание проводят в соответствии с 5.3.
4.4 Пирогенность
Магистрали комплекта должны быть апирогенны.
По запросу информация о методе испытаний и результаты испытаний магистралей могут быть предоставлены изготовителем.
Испытание проводят в соответствии с 5.4.
4.5 Последствия стерилизации
После стерилизации магистралей по методике, рекомендованной изготовителем, магистрали испытывают на отсутствие клинически значимых количеств токсических веществ, которые могут оказать отрицательные химическое, физическое и биологическое воздействия на кровь или обусловить выделение потенциально опасных веществ в кровь в клинически недопустимых количествах.
По запросу информация о методе испытаний и результаты испытаний магистралей могут быть предоставлены изготовителем.
Испытание проводят в соответствии с 5.5.
4.6 Механические характеристики
4.6.1 Конструкционная прочность
Магистрали комплекта:
- должны быть герметичны при избыточном давлении во внутренней полости, превышающем в 1,5 раза максимальное значение давления, установленное изготовителем;
- должны быть герметичны при вакуумметрическом давлении во внутренней полости минус 200 мм рт.ст.
Насосный сегмент магистрали должен обеспечивать непрерывный режим работы в течение не менее 24 ч при наихудших условиях эксплуатации.
Испытание проводят в соответствии с 5.6.1.
4.6.2 Соединения с гемодиализатором, гемофильтром или гемоконцентратором
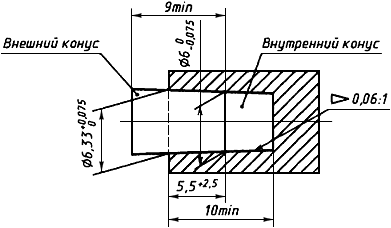
Присоединительные размеры деталей, обеспечивающих соединение магистралей с гемодиализатором, гемофильтром или гемоконцентратором, должны соответствовать приведенным на рисунках 1-3.
Рисунок 1 - Основные присоединительные размеры деталей, обеспечивающих соединение магистралей с гемодиализатором, гемофильтром или гемоконцентратором
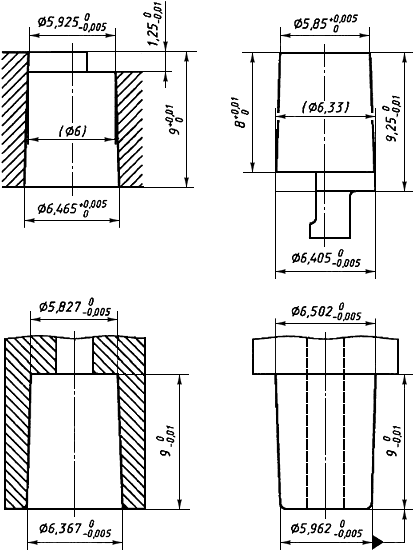
Рисунок 2 - Длина конусного сопряжения деталей, обеспечивающих соединение с кровопроводящей полостью
Рисунок 3 - Детали конических приспособлений с 6%-ным конусом для контроля соединения с кровопроводящей полостью гемодиализатора, гемофильтра или гемоконцентратора
Испытание проводят в соответствии с 5.6.2.
4.6.3 Соединение с устройством сосудистого доступа
Соединение магистрали с устройством сосудистого доступа должно обеспечиваться сопряжением типа "Луер-лок" конусностью 6%. Соединительное устройство должно соответствовать ISO 594-2.
Данное соединительное устройство проверяют в соответствии с 5.6.3.
4.6.4 Соединения с вспомогательными устройствами
Все элементы кровопроводящих магистралей, предназначенные для использования с вспомогательными устройствами, например гепариновые линии и линии датчиков давления, должны оканчиваться резьбовым соединением внутренним конусом 6% (Луер).
Данные соединительные устройства проверяют в соответствии с 5.6.4.
4.6.5 Инъекционный узел
Инъекционные узлы, входящие в состав магистралей комплекта, должны сохранять герметичность после прокалывания иглой внутренним диаметром 0,8 мм (N 21).
Инъекционный узел должен проектироваться таким образом, чтобы свести к минимуму риск прокалывания его иглой насквозь, что может повлечь за собой травму.
Испытание проводят в соответствии с 5.6.5.
4.6.6 Цветовое кодирование
Артериальная кровопроводящая магистраль комплекта должна иметь красный цветовой код, а венозная магистраль - голубой цветовой код. Цветовое кодирование приводят на видном месте на расстоянии до 100 мм от края магистрали.
Цветовое кодирование проверяют в соответствии с 5.6.6.
4.7 Физические характеристики
4.7.1 Объем
Объемы заполнения венозных и артериальных магистралей должны отличаться от установленных изготовителем соответствующих значений не более чем на ±20%.
Испытание проводят в соответствии с 5.7.1.
4.7.2 Сегмент насоса
Длина и внутренний диаметр насосных сегментов магистралей должны отличаться от установленных изготовителем соответствующих значений не более чем на ±5%.
Размеры проверяют в соответствии с 5.7.2.
5 Методы испытания
5.1 Условия качественного производства
Соответствие требованию, установленному в 4.1, определяют с помощью проверки.
5.2 Токсикология и биологическая совместимость
Токсикологические испытания и испытания на биологическую совместимость материалов магистралей, контактирующих с биологическими растворами, проводят на образцах изделий нового типа перед их реализацией, после внесения изменений в конструкционные материалы изготовляемых магистралей или после внесения изменений в метод стерилизации.
Примечание - Испытания проводят методами, установленными в соответствующих нормативных документах, утвержденных в установленном порядке.
5.3 Стерильность
Стерильность проверяют на образцах изделий нового типа перед их реализацией и контролируют каждую партию изделий.
5.4 Пирогенность
Испытание на пирогенность проводят на образцах изделий нового типа перед их реализацией, а затем производитель должен контролировать изготовляемую продукцию с целью гарантии апирогенности.
5.5 Последствия стерилизации
Испытания на наличие потенциально опасных осадков проводят по методике токсикологических испытаний на образцах изделий нового типа перед их реализацией и после внесения изменений в конструкционные материалы, а затем производитель должен контролировать изготовляемую продукцию с целью гарантии безопасности.
5.6 Механические характеристики
5.6.1 Конструкционная прочность
Данное испытание проводят на образцах изделий нового типа перед их реализацией.
5.6.1.1 Сущность метода
Моделируется использование магистралей комплекта, в ходе которого прокалывают инъекционные узлы. Затем магистрали испытывают на герметичность при избыточном и вакуумметрическом давлениях (4.6.1).
5.6.1.2 Реагенты
5.6.1.2.1 Для моделирования перфузата используют антикоагулированную бычью или человеческую плазму массовой концентрацией протеина (60±5) г/л.
5.6.1.2.2 Свежеприготовленная дистиллированная вода.
5.6.1.3 Аппаратура
5.6.1.3.1 Перфузионный насос, рекомендуемый изготовителем. При отсутствии рекомендаций изготовителя используют наиболее распространенный в клинической практике гемодиализа, гемофильтрации или гемоконцентрирования регулируемый роликовый перфузионный насос, обеспечивающий постоянство окклюзии и герметичность под действием испытательной нагрузки.
5.6.1.3.2 Сосуд для перфузата из нержавеющей стали или пластика.
5.6.1.3.3 Нагревательное устройство, обеспечивающее температуру перфузата (37±1)°С.
5.6.1.3.4 Зажим, обеспечивающий прокалывание инъекционного узла в одном и том же месте.
5.6.1.3.5 Игла наибольшим внутренним диаметром, рекомендованная изготовителем, или внешним диаметром 0,8 мм (N 21).
5.6.1.3.6 Эталонные соединения, которые отвечают требованиям, установленным в ISO 594-2 (см. рисунок 3 настоящего стандарта).
5.6.1.3.7 Соединители кровопроводящих трубопроводов, отвечающие требованиям, установленным в 4.6.3 ISO 8637.
5.6.1.3.8 Соединители устанавливают на кровопроводящие трубопроводы (если они не герметичные) и вспомогательные трубопроводы (5.6.1.3.6), которые могут выдержать условия испытаний.
5.6.1.3.9 Источник избыточного давления воздуха, обеспечивающий заданное давление во внутренних полостях магистралей при испытаниях.
5.6.1.3.10 Источник вакуумметрического давления, обеспечивающий заданное вакуумметрическое давление во внутренних полостях магистралей при испытаниях.
5.6.1.3.11 Мановакуумметр с погрешностью измерения ±10 мм рт.ст.
5.6.1.3.12 Сосуд, заполненный водой, в который погружают магистрали при испытаниях.
5.6.1.4 Отбор образцов магистралей
Из продукции изготовителя произвольно отбирают образцы магистралей, которые должны быть подвергнуты испытаниям по параметрам безопасности и качества. Объем выборки должен быть статистически обоснован.
5.6.1.5 Методика
5.6.1.5.1 Моделирование диализа осуществляют путем перемещения в режиме рециркуляции через кровопроводящие магистрали комплекта плазмы (5.6.1.2.1) при температуре (37±1)°С и при рекомендуемом изготовителем максимальном давлении и расходе рециркуляции.
По истечении 15 мин перфузии протыкают иглой инъекционные узлы магистралей, если они имеются, шесть раз в одном и том же месте (5.6.1.3.5).
Продолжают перфузию в течение 24 ч.
5.6.1.5.2 Подсоединяют магистрали в соответствии с рисунком 4 и создают во внутренней полости магистралей давление, в 1,5 раза превышающее максимальное рабочее давление, рекомендуемое изготовителем. Погружают на 1 мин магистрали в воду температурой (37±1)°С, поддерживая постоянное давление во внутренней полости магистралей.
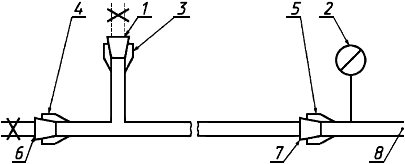
1 - внутренний соединитель вспомогательного трубопровода (5.6.1.3.6); 2 - манометр; 3 - внешний соединитель вспомогательного трубопровода (4.6.4); 4 - соединитель с гемодиализатором, гемофильтром, гемоконцентратором (4.6.2); 5 - внешний соединитель с устройством сосудистого доступа (5.6.1.3.6); 6 - соединитель с полостью по крови гемодиализатора, гемофильтра, гемоконцентратора (5.6.1.3.7); 7 - внутренний соединитель с устройством сосудистого доступа (5.6.1.3.6); 8 - к источнику избыточного давления воздуха
Примечание - Пунктирные линии обозначают, что используется другая магистраль комплекта. Знак "X" на трубопроводе указывает, что он пережат. Разрыв между двумя краями магистрали обозначает другие элементы, например сегмент перфузионного насоса или ловушку воздуха.
Рисунок 4 - Схема испытания на конструкционную прочность кровопроводящих магистралей
Через 30 с осматривают магистрали и соединения с устройством сосудистого доступа и вспомогательными трубопроводами на предмет утечки воздуха, которая характеризуется непрерывным потоком мелких пузырьков.
5.6.1.5.3 Заполняют часть магистралей и их соединения, которые могут испытывать воздействие вакуумметрического давления, дистиллированной водой (5.6.1.2.2) и создают вакуумметрическое давление минус 200 мм рт.ст.
Осматривают магистрали на предмет утечки воздуха, которая характеризуется устойчивым потоком мелких пузырьков.
5.6.1.5.4 По завершении испытания убеждаются, что сегмент насоса не поврежден.
5.6.1.6 Оформление результатов
5.6.1.6.1 Испытание на герметичность при избыточном давлении (выше максимального в 1,5 раза)
Испытание считают неудовлетворительным, если по истечении 30 с отмечается постоянный поток пузырьков воздуха (5.6.1.5.2).
Результат испытания фиксируют как удовлетворительный или неудовлетворительный.
5.6.1.6.2 Испытание при вакуумметрическом давлении
Испытание считают неудовлетворительным, если оно сопровождается появлением пузырьков в трубопроводах магистралей.
Результат испытания фиксируют как удовлетворительный или неудовлетворительный.
5.6.1.6.3 Если сегмент насоса поврежден (5.6.1.5.4), полученный результат фиксируют как неудовлетворительный.
5.6.1.7 Протокол испытания
Испытание фиксируют как удовлетворительное, если все отобранные образцы выдержали испытание, и неудовлетворительным, если какой-либо из образцов не выдержал испытания.
Кроме того, приводят объем выборки, который должен быть статистически обоснован.
5.6.2 Соединения с гемодиализатором, гемофильтром или гемоконцентратором
Соответствие требованиям, установленным в 4.6.2, определяют путем проверки.
5.6.3 Соединение с устройством сосудистого доступа
Соответствие требованиям, установленным в 4.6.3, определяют путем проверки.
5.6.4 Соединения с вспомогательными устройствами
Соответствие требованиям, установленным в 4.6.4, определяют путем проверки.
5.6.5 Инъекционные узлы
Герметичность инъекционного узла после прокалывания его иглой (5.6.1.5.1) испытывают методом, приведенным в 5.6.1.
Соответствие требованиям дезинфекции и защиты оператора от укола иглой определяют путем проверки.
5.6.6 Цветовое кодирование
Соответствие требованиям, установленным в 4.6.6, определяют путем проверки.
5.7 Физические характеристики
5.7.1 Объем
Данное испытание является арбитражным и проводится по методике, описанной ниже. Могут использоваться и другие методы испытания при условии, что полученные результаты будут отличаться от результатов, полученных при арбитражных испытаниях не более чем на ±5%.
Данное испытание проводят на образцах изделий нового типа перед их реализацией и не учитывают при контроле качества изделия.
5.7.1.1 Сущность метода
Измерение объема воды, заполняющей кровопроводящие трубопроводы магистралей.
5.7.1.2 Реагент
Водопроводная вода.
5.7.1.3 Аппаратура
5.7.1.3.1 Мерный цилиндр с погрешностью измерения не более ±2%.
5.7.1.3.2 Зажимы или герметичные устройства для герметизации вспомогательных трубопроводов.
5.7.1.4 Выборка
Из продукции изготовителя произвольно отбирают образцы магистралей, которые должны быть подвергнуты испытаниям по параметрам безопасности и качества. Объем выборки должен быть статистически обоснован.
5.7.1.5 Методика
Пережимают вспомогательные трубопроводы и заполняют кровопроводящие трубопроводы магистралей водой. Затем полностью сливают воду, заполняющую магистрали, в мерный цилиндр и определяют объем слитой жидкости.
5.7.1.6 Оформление результатов
Выражают полученный объем в миллилитрах и вычисляют процентное отношение полученного объема к объему, установленному изготовителем.
5.7.1.7 Протокол испытания
Испытание считают удовлетворительным, если его результат в отношении каждой выборки не отличается более чем на 20% от объема, установленного изготовителем.
5.7.2 Сегмент насоса
Соответствие требованиям, установленным в 4.7.2, определяют в отношении каждой партии магистралей, изготовленных и испытанных по параметрам безопасности и качества. Для проверки насосных сегментов из готовой продукции отбирают образцы магистралей. Объем выборки должен быть статистически обоснован.
6 Упаковка, маркировка и эксплуатационная документация
6.1 Упаковка и маркировка
6.1.1 Потребительская тара (упаковка)
На упаковке должна быть приведена следующая информация:
- наименование и адрес изготовителя;
- наименование изделия;
- идентификационный код изготовителя изделия;
- номер партии изготовленного товара;
- заключение о стерильности, апирогенности и токсичности всего изделия или его частей;
- месяц и год стерилизации с точностью до 30 дней, начиная с фактической даты стерилизации;
- указание об одноразовом назначении изделия.
Примечание - Может также использоваться условное обозначение 1051 из ISO 7000 - ;
- указание: "Перед применением прочтите инструкции";
- инструкция по подготовке магистрали к использованию;
- инструкции и предупреждения о хранении и обращении.
6.1.2 Транспортная тара
На транспортной таре должна быть приведена следующая информация:
- наименование и адрес изготовителя;
- наименование и адрес дистрибьютера, если они отличаются от наименования и адреса изготовителя;
- наименование изделия, описание содержимого и число содержащихся изделий;
- идентификационный код изготовителя изделия;
- номер партии изготовленного товара;
- заключение о стерильности, апирогенности и токсичности всего изделия или его частей;
- месяц и год стерилизации с точностью до 30 дней, начиная с фактической даты стерилизации;
- инструкции и предупреждения о хранении и обращении.
6.2 Документация
6.2.1 Эксплуатационные документы
К транспортной таре должна быть приложена следующая информация:
- наименование и адрес изготовителя;
- наименование изделия;
- идентификационный код изготовителя изделия;
- заключение о стерильности, апирогенности и токсичности всего изделия или его частей, а также информация о методе стерилизации;
- указание об одноразовом назначении изделия.
Примечание - Может также использоваться условное обозначение 1051 из ISO 7000 - ;
- различные предупреждения, включая следующие (но не ограничиваясь ими):
1) предельные значения давления и расхода крови,
2) предупредительная информация для пользователя о том, что он обязан гарантировать совместимость магистрали с устройством, с которым она используется, например детектором воздуха, клапаном безопасности, перфузионным насосом и монитором давления, при этом особое внимание должно быть уделено ее совместимости с детектором воздуха,
3) информация о том, что в случае применения магистралей для перемещения крови через газообменное устройство, входная магистраль должна иметь синий цветовой код, а выходная - красный;
- инструкция по подготовке магистрали к использованию;
- разъяснение цветового кодирования, которое используют для идентификации артериальных и венозных магистралей;
- инструкции по прочтению справочных документов перед использованием магистралей, если в них содержится дополнительная информация.
6.2.2 Справочные документы
Пользователю должна быть предоставлена следующая информация, если она не приводится в эксплуатационных документах (6.2.1):
- подробное описание необходимого вспомогательного оборудования;
- общий объем заполнения магистрали кровью при полностью заполненной ловушке воздуха;
- длина и внутренний диаметр насосного сегмента;
- общее описание комплекта магистралей;
- ориентация соединения с гемодиализатором относительно трубопроводов по диализирующему раствору;
- инструкция о подсоединении линий контроля давления магистралей к мониторам давления, обеспечивающая при эксплуатации предотвращение попадания крови в монитор давления;
- перечень дезинфектантов для наружного применения (например при взятии проб крови), которые совместимы с деталями магистрали, и предупреждение, что совместимость других дезинфектантов с деталями магистрали должна быть определена перед клиническим использованием;
- давление на входе венозной магистрали при перфузии 32% () раствора глицерина в воде с расходом 400 мл/мин, температуре (37±1°С и давлении на выходе венозной магистрали 50 мм рт.ст.;
- направление кровотока, при необходимости;
- расположение соединений трубопровода;
- рекомендуемая методика завершения режима работы, при необходимости;
- типичная гидравлическая схема;
- указание о том, что по просьбе пользователя ему может быть предоставлена следующая информация:
1) описание методов испытаний магистралей комплекта,
2) общие наименования конструкционных материалов в соответствии с ISO 472 (5.2, 5.7.1 и 5.7.2),
3) количество и диапазон размеров микрочастиц и волокон на выходе комплекта магистралей, подготовленного согласно рекомендациям изготовителя к клиническому использованию, а также описание метода, используемого для проведения данного испытания,
4) результаты испытаний соединений деталей и трубопроводов магистралей и описание методов испытаний,
5) количество и диапазон размеров твердых частиц, занесенных при прокалывании иглой инъекционного узла, и описание метода, используемого для проведения указанного испытания.
Приложение ДА
(справочное)
Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам
Таблица ДА.1
Обозначение и наименование международного стандарта | Степень соответствия | Обозначение и наименование межгосударственного стандарта |
ISO 8637:1989 Гемодиализаторы, гемофильтры и гемоконцентраторы | IDT | ГОСТ ISO 8637-2012 Гемодиализаторы, гемофильтры и гемоконцентраторы. Технические требования и методы испытаний |
ISO 472:1979 Пластики. Словарь двуязычный | - | * |
ISO 594-2:1991 Детали соединительные с конусностью 6% (Люэра) для шприцев, игл и другого медицинского оборудования. Часть 2. Люэровские наконечники | - | * |
ISO 7000:1989 Графические символы, наносимые на оборудование. Перечень и сводная таблица | - | * |
* Соответствующий межгосударственный стандарт отсутствует. До его утверждения рекомендуется использовать перевод на русский язык данного международного стандарта. Перевод данного международного стандарта находится в Федеральном информационном фонде технических регламентов и стандартов. Примечание - В настоящем стандарте использовано следующее условное обозначение степени соответствия стандарта: - IDT - идентичные стандарты. | ||
УДК 616-089.819:006.354 | МКС 11.040.020 | Р24 | IDT |
Ключевые слова: медицинское изделие, кровь, диализ, гемодиализаторы, технические условия, испытания, упаковка, маркировка | |||
Электронный текст документа
и сверен по:
, 2013