ГОСТ 34151-2017
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ
Определение витамина C с помощью высокоэффективной жидкостной хроматографии
Foodstuffs. Determination of vitamin С by high performance liquid chromatography
МКС 67.080.01
Дата введения 2019-01-01
Предисловие
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением науки Институтом физиологии растений им.К.А.Тимирязева Российской академии наук (ИФР РАН) и Федеральным государственным бюджетным научным учреждением "Всероссийский научно-исследовательский институт технологии консервирования" (ФГБНУ "ВНИИТеК")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 1 июня 2017 г. N 51)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 2 августа 2017 г. N 787-ст межгосударственный стандарт ГОСТ 34151-2017 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2019 г.
5 ВВЕДЕН ВПЕРВЫЕ
6 В настоящем стандарте учтены основные положения BS EN 14130:2003* "Продукты пищевые. Определение витамина C с помощью высокоэффективной жидкостной хроматографии" ("Foodstuffs. Determination of vitamin С by HPLC")
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
1 Область применения
Настоящий стандарт устанавливает метод определения витамина C в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Содержание витамина C определяется в виде суммы L(+)-аскорбиновой и L(+)-дегидроаскорбиновой кислот.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79* Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
________________
* В Российской Федерации действует ГОСТ Р 12.1.019-2009.
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ ISO 3696-2013** Вода для лабораторного анализа. Технические требования и методы контроля
________________
** В Российской Федерации действует ГОСТ Р 52501-2005 (ИСО 3696:1987) "Вода для лабораторного анализа. Технические условия".
ГОСТ ISO 5725-2-2003*** Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
________________
*** В Российской Федерации действует ГОСТ Р ИСО 5725-2-2002.
ГОСТ ISO 7886-1-2011 Шприцы инъекционные однократного применения стерильные. Часть 1. Шприцы для ручного использования
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
Метод основан на экстракции витамина C из пробы раствором метафосфорной кислоты, с последующим восстановлением L(+)-дегидроаскорбиновой кислоты до L(+)-аскорбиновой кислоты и определением общего содержания L(+)-аскорбиновой кислоты с применением высокоэффективной жидкостной хроматографии (ВЭЖХ) со спектрофотометрическим детектированием при длине волны 265 нм.
4 Реактивы
4.1 Общие положения
При проведении определений, если не оговорены другие условия, используют только реактивы установленной аналитической чистоты и воду не ниже первой степени чистоты по ГОСТ ISO 3696.
4.2 Реактивы и растворы
4.2.1 Кислота метафосфорная (HPO)
.
4.2.2 Натрий фосфат трехзамещенный 12-водный NaPO
·12H
O с массовой долей основного вещества не менее 98,0%.
4.2.3 Калий фосфат однозамещенный (дигидрофосфат) KHPO
с массовой долей не менее 99,0%.
4.2.4 L-цистеин CH
NO
S с массовой долей не менее 99,0%.
4.2.5 N-цетил-N,N,N-триметиламмонийбромид (цетримид) CH
BrN с массовой долей не менее 99,0%.
4.2.6 Метанол (для ВЭЖХ) с массовой долей не менее 99,0%.
4.2.7 Кислота метафосфорная, раствор массовой концентрации [(HPO
)
]=200 г/дм
200 г метафосфорной кислоты (см. 4.2.1) растворяют в воде в мерной колбе вместимостью 1 дм, объем содержимого в колбе доводят водой до метки.
Срок годности раствора - 1 мес при температуре 4°С.
4.2.8 Кислота метафосфорная, раствор массовой концентрации [(HPO
)
]=20 г/дм
50 см раствора метафосфорной кислоты, приготовленной по 4.2.7, переносят пипеткой в мерную колбу вместимостью 500 см
, объем содержимого в колбе доводят водой до метки.
Раствор готовят в день проведения определения.
4.2.9 Натрий фосфорнокислый трехзамещенный, раствор массовой концентрации (Na
PO4·12H
O)=200 г/дм
200 г фосфорнокислого натрия трехзамещенного (см. 4.2.2) растворяют в воде в мерной колбе вместимостью 1 дм, объем содержимого в колбе доводят водой до метки.
4.2.10
L-цистеин, раствор массовой концентрации (C
H
NO
S)=40 г/дм
20 г L-цистеина (см. 4.2.4) растворяют в воде в мерной колбе вместимостью 500 см, объем содержимого в колбе доводят водой до метки.
Раствор готовят в день проведения определения.
4.2.11 Фаза подвижная для ВЭЖХ
13,6 г дигидрофосфата калия (см. 4.2.3) растворяют в стакане в 900 см воды. Раствор фильтруют через мембранный фильтр с размером пор 0,45 мкм (раствор A).
1,82 г N-цетил-N,N,N-триметиламмонийбромида (см. 4.2.5) растворяют в стакане в 100 см метанола (см. 4.2.6). Полученный раствор фильтруют через мембранный фильтр с размером пор 0,45 мкм (раствор B).
Смешивают 900 см раствора A и 100 см
раствора B. Полученную подвижную фазу для ВЭЖХ при необходимости перед употреблением дегазируют.
4.2.12 Крахмал (применяют по выбору пользователя), раствор массовой концентрации 1 г/100 см.
4.2.13 Йод (применяют по выбору пользователя), раствор молярной концентрации с(l)=0,05 моль/дм
.
4.2.14 Кислота серная, раствор молярной концентрации с(HSO
)=0,1 моль/дм
.
4.3 Стандартные вещества
4.3.1 Кислота аскорбиновая (или L(+)-аскорбиновая) с массовой долей w(CH
O
) не менее 99,7%
(R)-5-[(S)-1,2-дигидроксиэтил]-3,4-дигидрокси-5-Н-фуран-2-он.
4.3.2 Кислота эриторбовая (изоаскорбиновая), D(-)-аскорбиновая с массовой долей ?=w(CH
O
) не менее 99,0%
(R)-5-[(R)-1,2-дигидроксиэтил]-3,4-дигидрокси-5-Н-фуран-2-он.
4.4 Основные стандартные растворы
4.4.1 Основной стандартный раствор аскорбиновой кислоты массовой концентрации ( C
H
O
)=1 мг/см
Растворяют около 100 мг аскорбиновой кислоты (см. 4.3.1), взятой с точностью до 0,1 мг, в 100 см раствора метафосфорной кислоты, приготовленной по 4.2.8.
Раствор готовят в день проведения определения.
Для увеличения срока хранения основного раствора аскорбиновой кислоты добавляют L-цистеин.
4.4.2 Основной стандартный раствор эриторбовой (изоаскорбиновой) кислоты массовой концентрации ( C
H
O
)=1 мг/см
Растворяют около 100 мг изоаскорбиновой кислоты (см. 4.3.2), взятой с точностью до 0,1 мг, в 100 см раствора метафосфорной кислоты, приготовленной по 4.2.8.
Раствор готовят в день проведения определения.
4.4.3 Вычисление точной концентрации основного стандартного раствора (выполняют по выбору пользователя)
Взвешивают в конической колбе около 150 мг аскорбиновой кислоты, добавляют 10 см раствора серной кислоты (см. 4.2.14) и 80 см
воды, не содержащей диоксида углерода. После добавления раствора крахмала (см. 4.2.12) титруют раствором йода (см. 4.2.13) до появления устойчивой синей окраски. Масса аскорбиновой кислоты, эквивалентная 1 см
раствора йода, пошедшего на титрование, составляет 8,81 мг.
Массовую долю основного компонента в стандартном веществе , %, вычисляют по формуле
 , (1)
, (1)
где - объем раствора йода, пошедший на титрование, см
;
8,81 - масса аскорбиновой кислоты, эквивалентная 1 см раствора йода, пошедшего на титрование, мг;
100 - коэффициент пересчета результата в проценты; - масса навески стандартного вещества, мг.
4.5 Градуировочные растворы
4.5.1 Градуировочные растворы аскорбиновой кислоты с массовой концентрацией (C
H
O
) от 5 до 50 мкг/см
От 0,5 до 5 см основного раствора аскорбиновой кислоты, приготовленного по 4.4.1, переносят пипеткой в мерные колбы вместимостью 100 см
, объем содержимого в колбах доводят до метки раствором метафосфорной кислоты, приготовленным по 4.2.8.
Растворы готовят в день проведения определения.
4.5.2 Градуировочный раствор эриторбовой (изоаскорбиновой) кислоты с массовой концентрацией (C
H
O
)=10 мкг/см
(готовят по выбору пользователя)
1 см основного раствора изоаскорбиновой кислоты, приготовленного по 4.4.2, переносят пипеткой в мерную колбу вместимостью 100 см
, объем содержимого в колбе доводят до метки раствором метафосфорной кислоты, приготовленным по 4.2.8. Концентрация приготовленного раствора должна быть в пределах от 5 до 20 мкг/см
.
Раствор готовят в день проведения определения.
Допускается применение других химических реактивов по качеству не ниже вышеуказанных.
5 Средства измерений, вспомогательное оборудование и посуда
5.1 Общие положения
Используют обычные приборы и оборудование.
5.2 Спектрофотометр с рабочим спектральным диапазоном в ультрафиолетовой области, пригодный для измерения оптической плотности при требуемых длинах волн, с комплектом кювет.
5.3 Хроматограф жидкостный
ВЭЖХ-система, состоящая из насоса, устройства ввода пробы, спектрофотометрического детектора, пригодного для измерения оптической плотности при длине волны 265 нм и компьютерной системы сбора и обработки данных.
5.4 Колонка для ВЭЖХ разделения
5.4.1 Общие положения
Допускается применение колонки с другим размером частиц сорбента или размерами колонки, по отношению к тем, что указаны в настоящем стандарте. Критерием пригодности колонки является разделение пиков L-аскорбиновой и изоаскорбиновой кислот на уровне базовой (горизонтальной) линии.
5.4.2 Параметры хроматографической колонки
Колонка с внутренним диаметром 4,0 мм, длиной 250 мм, заполненная сорбентом* на основе силикагеля с привитыми группами C размером частиц сорбента 5 мкм.
________________
* Lichrospher 100 RP 18 является примером подходящего сорбента. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламой этого продукта.
5.5 Устройство для фильтрации
Мембранный фильтр с размером пор, например, 0,2 или 0,45 мкм. Фильтрование подвижной фазы и раствора пробы перед использованием или вводом в хроматограф продлевает срок службы колонки.
5.6 Весы неавтоматического действия специального класса точности по ГОСТ OIML R 76-1 пределом допускаемой абсолютной погрешности ±0,001 г.
5.7 Иономер (рН-метр) любого типа, в комплекте с комбинированным стеклянным электродом и пределом абсолютной погрешности измерения ±0,1 ед. рН.
5.8 Пипетки градуированные различной вместимости по ГОСТ 29227.
5.9 Мерные колбы, пробирки и цилиндры различной вместимости по ГОСТ 1770.
5.10 Мешалка магнитная.
5.11 Стаканы исполнения 1 и колбы конические Кн различной вместимости по ГОСТ 25336.
5.12 Мельница лабораторная или гомогенизатор любого типа, для измельчения проб.
5.13 Шприцы однократного применения по ГОСТ ISO 7886-1.
5.14 Виалы стеклянные из темного стекла с крышкой и септой из полимерного материала подходящей вместимости.
Допускается применение других средств измерений с метрологическими характеристиками, вспомогательного оборудования и посуды с техническими характеристиками не ниже вышеуказанных.
6 Проведение определений
6.1 Общие положения
При проведении определений необходимо обеспечивать предельно короткий промежуток времени между приготовлением растворов проб и градуировочных растворов и их определением. Температура в помещении при проведении определений не должна превышать 25°С.
Максимальный срок использования градуировочных растворов - 8 ч с момента их приготовления.
6.2 Подготовка пробы
Пробу гомогенизируют. Если проба представляет собой продукт твердой консистенции, ее измельчают на мельнице подходящей конструкции и снова тщательно перемешивают. Определение проводят сразу после гомогенизации. Подготовку проб свежих фруктов и овощей проводят одновременно с экстракцией (см. 6.3.1).
6.3 Приготовление раствора пробы
6.3.1 Экстракция
Навеску пробы подходящей массы, например, 3 г (при содержании витамина C в пробе около 50 мг/100 г), взвешенной с точностью до 1 мг, помещают в мерную колбу вместимостью 100 см. Добавляют 80 см
раствора метафосфорной кислоты, приготовленной по 4.2.8, содержимое колбы тщательно перемешивают, после чего объем в колбе доводят до метки. Содержимое колбы снова перемешивают, после чего фильтруют. Полученный раствор представляет собой экстракт из пробы.
Для свежих фруктов и овощей навеску предварительно измельченной ножом пробы массой от 2 до 10 г, взвешенной с точностью до 1 мг, помещают в стакан вместимостью 100 см, затем вносят некоторое количество раствора метафосфорной кислоты, приготовленной по 4.2.8. Содержимое стакана гомогенизируют, количественно переносят в мерную колбу вместимостью 100 см
, перемешивают и фильтруют. Полученный раствор представляет собой экстракт из пробы.
Примечание - Стабильность аскорбиновой кислоты в растворе можно повысить, например, путем добавления к раствору метафосфорной кислоты 125 см раствора L-цистеина, приготовленного по 4.2.10, дитиотреитола (DTTA) или диэтилентриаминфосфорной кислоты (DTPA). При этом следует иметь в виду, что эти стабилизаторы могут влиять на качество хроматографического разделения. Данная процедура не использовалась при проведении межлабораторных испытаний.
6.3.2 Проведение реакции восстановления
20 см отфильтрованного экстракта (см. 6.3.1) переносят в стакан вместимостью 50 см
, добавляют 10 см
раствора L(+)-цистеина. Устанавливают значение рН полученного раствора в пределах 7,0-7,2 ед. рН (по рН-метру) путем добавления по каплям раствора трехзамещенного натрия фосфата, приготовленного по 4.2.9, при постоянном перемешивании на магнитной мешалке. По достижении указанного значения рН раствор выдерживают точно 5 мин при постоянном перемешивании. По истечении указанного времени устанавливают значение рН раствора в пределах 2,5-2,8 ед. рН (по рН-метру) путем добавления по каплям раствора метафосфорной кислоты, приготовленной по 4.2.7, при постоянном перемешивании на магнитной мешалке. Полученный раствор количественно переносят в мерную колбу вместимостью 50 см
, при этом электроды рН-метра, рабочий элемент магнитной мешалки и стакан, в котором находился раствор, ополаскивают водой, перенося смывы в ту же колбу. Объем содержимого в мерной колбе доводят до метки водой, содержимое колбы перемешивают. Полученный раствор фильтруют через мембранный фильтр (см. 5.5), фильтрат используют для хроматографического определения.
Если в продукте имеется информация о наличии загустителей, рекомендуется провести их осаждение перед хроматографическим определением во избежание порчи хроматографической колонки. Для этого к порции восстановленного раствора пробы объемом 4 см добавляют 1 см
метанола (см. 4.2.6). Полученный раствор перемешивают и фильтруют через мембранный фильтр (см. 5.5). Фильтрат используют для хроматографического определения.
6.4 Идентификация
Идентифицируют пик L-аскорбиновой кислоты путем сравнения времени удерживания на хроматограмме раствора пробы и на хроматограмме градуировочного раствора. Идентификацию пика L-аскорбиновой кислоты можно также проводить путем добавления стандартного раствора в раствор пробы.
Ниже приведены условия хроматографического определения, обеспечивающие требуемую степень хроматографического разделения и пригодные для количественного определения (см. также рисунок A.1. Данные условия были использованы при проведении межлабораторных испытаний):
- неподвижная фаза | колонка* заполненная сорбентом на основе силикагеля с привитыми группами C | ||
- подвижная фаза | раствор A + раствор B (см. 4.2.11); | ||
- скорость потока подвижной фазы | 0,7 см | ||
- объем петли инжектора | 30 мм | ||
- длина волны детектирования | 265 нм. |
Данные параметры хроматографического определения позволяют также идентифицировать пик изоаскорбиновой кислоты, не являющейся витамином С.
Примечание - В качестве других приемлемых параметров хроматографического определения можно использовать подвижную фазу, состоящую из 10% ацетонитрила и 90% смешанного водного раствора однозамещенного фосфата калия массовой концентрации 13,6 г/дм и цетримида массовой концентрации 2 г/дм
в сочетании с колонкой, заполненной обращенно-фазовым сорбентом с привитыми октильными группами (C
) с размером частиц 10 мкм, длиной 250 мм, внутренним диаметром 4,6 мм, при скорости потока (1,0±0,1) см
/мин.
6.5 Количественное определение
В зависимости от системы, последовательно инжектируют одинаковые объемы стандартного раствора и раствора пробы (не более 50 мм). Обработку результатов проводят по методу внешнего стандарта либо с использованием градуировочной характеристики. При вычислении по методу внешнего стандарта вычисляют площадь пика или его высоту, результаты сопоставляют с соответствующими значениями, полученными при определении стандартного раствора или используют градуировочный график. При использовании градуировочного графика проверяют его на линейность.
7 Обработка результатов
Вычисление результата определения проводят с использованием градуировочной характеристики с помощью программного обеспечения либо применяют следующий упрощенный способ.
Массовую долю аскорбиновой кислоты , мг/100 г, вычисляют по формуле
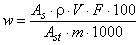 , (2)
, (2)
где - площадь или высота пика L-аскорбиновой кислоты на хроматограмме раствора пробы (см. 6.3.2), в единицах площади или высоты;
- массовая концентрация L-аскорбиновой кислоты в градуировочном растворе, мкг/см
;
- общий объем приготовленного по 6.3.1 раствора пробы перед проведением реакции восстановления, см
;
- коэффициент разбавления при восстановлении раствора пробы (в данном случае
=2,5);
100 - коэффициент пересчета результата в мг на 100 г; - площадь или высота пика L-аскорбиновой кислоты на хроматограмме градуировочного раствора (см. 4.5.1) в единицах площади или высоты;
- масса навески пробы, г;
1000 - коэффициент пересчета из микрограммов в миллиграммы.
В случае, если процедура определения включала в себя осаждение (см. 6.3.2), результат, полученный по формуле (2), умножают на коэффициент 1,25.
8 Прецизионность измерений
8.1 Общие положения
Значения характеристик прецизионности при определении витамина C были получены в 1997 г. в результате межлабораторных сравнительных испытаний, проведенных в соответствии с ГОСТ ISO 5725-2 (приложение B). Для других диапазонов содержания витамина C и иных типов образцов значения характеристик прецизионности методики могут отличаться от значений, приведенных в приложении B.
8.2 Повторяемость
Абсолютное расхождение между результатами двух независимых единичных испытаний, полученными одним методом на идентичном объекте испытаний в одной лаборатории одним оператором с использованием одного оборудования в течение короткого промежутка времени, не должно превышать предел повторяемости r более чем в 5% случаев.
Значения предела повторяемости равны:
- для апельсинового сока: =54,6 мг/100 г,
=6,4 мг/100 г;
- овощного консервированного супа: =35,6 мг/100 г,
=3,7 мг/100 г;
- сухого молока (порошок): =100,3 мг/100 г,
=17,9 мг/100 г;
- супа-концентрата сублимационной сушки: =169,3 мг/100 г,
=42,0 мг/100 г;
- сухого завтрака (концентрат): =102,6 мг/100 г,
=28,7 мг/100 г;
- фруктовых консервов для детского питания: =47,1 мг/100 г,
=7,1 мг/100 г.
8.3 Воспроизводимость
Абсолютное расхождение между результатами двух единичных испытаний, полученными одним методом на идентичном объекте испытаний в разных лабораториях разными операторами с использованием разного оборудования, не должно превышать предел воспроизводимости R более чем в 5% случаев.
Значения предела воспроизводимости равны:
- для апельсинового сока: =54,6 мг/100 г, R=30,3 мг/100 г;
- овощного консервированного супа: =35,6 мг/100 г, R=21,7 мг/100 г;
- сухого молока (порошок): =100,3 мг/100 г, R=32,2 мг/100 г;
- супа-концентрата сублимационной сушки: =169,3 мг/100 г, R=74,3 мг/100 г;
- сухого завтрака (концентрат): =102,6 мг/100 г, R=56,2 мг/100 г;
- фруктовых консервов для детского питания: =47,1 мг/100 г, R=23,9 мг/100 г.
9 Протокол испытаний
Протокол результатов испытаний должен содержать следующие сведения:
- всю информацию, необходимую для идентификации пробы;
- ссылку на настоящий стандарт или на использованный метод;
- дату и время отбора пробы (если известны);
- дату поступления пробы в лабораторию;
- дату проведения испытания;
- результаты испытания с указанием единиц измерения;
- все особенности, наблюдавшиеся при проведении испытания;
- все операции, не оговоренные в методике или считающиеся как необязательные, которые могли повлиять на результат испытания.
10 Требования безопасности
10.1 Условия безопасного проведения работ
При проведении измерений следует соблюдать требования:
- пожарной безопасности в соответствии с ГОСТ 12.1.004;
- безопасности при работе с вредными веществами в соответствии с ГОСТ 12.1.007;
- электробезопасности - по ГОСТ 12.1.019 и в соответствии с руководствами по эксплуатации используемого оборудования.
10.2 Требования к квалификации операторов
К выполнению испытаний и обработке результатов допускаются специалисты, имеющие высшее или специальное образование, опыт работы в химической лаборатории и изучившие инструкцию по эксплуатации жидкостного хроматографа. Первое применение метода в лаборатории должно проводиться под руководством специалиста, владеющего теорией высокоэффективной жидкостной хроматографии и имеющего практические навыки в этой области.
Приложение А (справочное). Пример хроматограммы
Приложение А
(справочное)
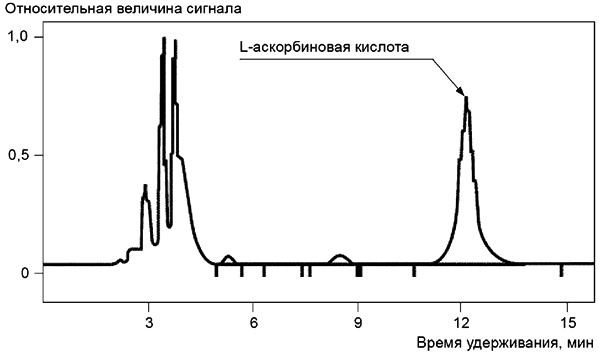
А.1 Пример хроматограммы при определении аскорбиновой кислоты в апельсиновом соке с помощью ВЭЖХ приведен на рисунке А.1.
Рисунок А.1 - Пример хроматограммы при определении аскорбиновой кислоты в апельсиновом соке с помощью ВЭЖХ
|
Рисунок А.1 - Пример хроматограммы при определении аскорбиновой кислоты в апельсиновом соке с помощью ВЭЖХ (время удерживания: =11,953 мин)
Приложение Б (справочное). Данные по прецизионности методики
Приложение Б
(справочное)
Б.1 Приведенные ниже данные получены в 1997 г. в результате межлабораторных испытаний по ГОСТ ISO 5725-2. Процедура проведения испытания не включала в себя операцию восстановления L-дегидроаскорбиновой кислоты.
Таблица Б.1 - Данные по прецизионности определения общего содержания витамина C
Образец | 1 | 2 | 3 | 4 | 5 | 6 |
Год проведения испытаний | 1997 | 1997 | 1997 | 1997 | 1997 | 1997 |
Число лабораторий-участников | 15 | 15 | 15 | 15 | 15 | 15 |
Число лабораторий за исключением выбросов | 14 | 15 | 14 | 14 | 14 | 14 |
Число принятых результатов | 28 | 30 | 28 | 28 | 28 | 28 |
Среднее значение | 54,6 | 35,6 | 100,3 | 169,3 | 102,6 | 47,1 |
Стандартное отклонение повторяемости | 2,3 | 1,3 | 6,3 | 14,8 | 10,2 | 2,5 |
Относительное стандартное отклонение повторяемости, % | 4,2 | 3,6 | 6,3 | 8,8 | 9,9 | 5,3 |
Предел повторяемости | 6,4 | 3,7 | 17,9 | 42,0 | 28,7 | 7,1 |
Стандартное отклонение воспроизводимости | 10,7 | 7,7 | 11,4 | 26,2 | 19,8 | 8,5 |
Относительное стандартное отклонение воспроизводимости, % | 19,7 | 21,6 | 11,4 | 15,5 | 19,3 | 18,0 |
Предел воспроизводимости R, (2,83· | 30,3 | 21,7 | 32,2 | 74,3 | 56,2 | 23,9 |
1 - апельсиновый сок; 2 - овощной консервированный суп; 3 - сухое молоко; 4 - суп-концентрат сублимационной сушки; 5 - сухой завтрак (концентрат); 6 - фруктовые консервы для детского питания. |
УДК 664.841:664.851:543.06:006.354 | МКС 67.080.01 |
Ключевые слова: продукты пищевые, витамин C, метод высокоэффективной жидкостной хроматографии, определение |
Электронный текст документа
и сверен по:
официальное издание
М.: Стандартинформ, 2017