ГОСТ 32382-2013
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Гидролиз
Test methods for chemicals of environmental hazard
Hydrolysis
МКС 71.100.01
Дата введения 2014-08-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила, рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием "Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ" (ФГУП "ВНИЦСМВ"), Техническим комитетом по стандартизации ТК 339 "Безопасность сырья, материалов и веществ" на основе собственного перевода на русский язык англоязычной версии документа, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 18 октября 2013 г. N 60-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Азербайджан | AZ | Азстандарт |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Казахстан | KZ | Госстандарт Республики Казахстан |
Молдова | MD | Молдова-Стандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
Украина | UA | Минэкономразвития Украины |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 ноября 2013 г. N 789-ст межгосударственный стандарт ГОСТ 32382-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 августа 2014 г.
5 Настоящий стандарт идентичен международному документу OECD, Test N 111:2004* "Гидролиз как функция рН" ("Hydrolysis as a Function of pH", IDT).
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Наименование настоящего стандарта изменено относительно наименования указанного международного документа для приведения в соответствие с ГОСТ 1.5 (подраздел 3.6)
6 ВВЕДЕН ВПЕРВЫЕ
7 ПЕРЕИЗДАНИЕ. Апрель 2019 г.
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
Введение
Химические вещества могут попадать в поверхностные воды напрямую, при смыве, при опрыскивании, с поверхностными стоками, через дренажные системы, при удалении промышленных, бытовых или сельскохозяйственных жидких отходов, посредством атмосферного осаждения. Далее они могут претерпевать изменения в этих водах в результате химических (например, гидролиз, окисление), фотохимических и/или микробиологических процессов.
Испытание проводят для того, чтобы:
- определить зависимость скорости гидролиза исследуемого вещества от рН;
- идентифицировать или определить природу продуктов гидролиза, которые могут оказывать воздействие на организмы, а также определить скорость их образования и уровень снижения скорости гидролиза.
Проведение таких исследований может оказаться необходимым для веществ, попадающих в воду напрямую или которые с большой вероятностью попадут в окружающую среду одним из описанных выше путей.
1 Область применения
Настоящий стандарт устанавливает метод лабораторного анализа для оценки абиотических гидролитических превращений химических веществ в водных системах при значениях рН, встречающихся в окружающей среде (рН 4-9) [1]-[7].
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 (время удаления 50%) [DT50 (Disappearance time 50)]: Время, за которое концентрация вещества упадет до 50%.
2.2 исследуемое вещество (Test substance): Любое вещество, исходные или соответствующие продукты трансформации.
2.3 период полуразложения () [Half-life (t0.5)]: Время, необходимое для гидролитического разложения 50% исследуемого вещества в случае, если реакция может быть описана кинетикой первого порядка, то есть не зависима от концентрации вещества.
2.4 продукты гидролиза (Hydrolysis products): Все вещества, образующиеся вследствие гидролитической трансформации исследуемого вещества.
2.5 продукты трансформации (Transformation products): Все вещества, образующиеся в результате биотических или абиотических трансформаций исследуемого вещества.
3 Общие положения
3.1 Принцип метода
3.1.1 К стерильным водным буферным растворам с различными значениями рН (рН 4,0, 7,0 и 9,0) добавляют исследуемое вещество. Растворы с исследуемым веществом инкубируют в темноте при контролируемых лабораторных условиях (при постоянной температуре). Через определенные промежутки времени буферные растворы анализируют на содержание исследуемого вещества и продуктов гидролиза. Баланс вещества проще рассчитать при использовании радиоактивно маркированного исследуемого вещества (например, ).
3.1.2 Многоуровневый подход, используемый в настоящем стандарте, подробно описан в приложении А. Переход на каждый следующий уровень зависит от результатов предыдущего.
3.2 Применимость метода
Данный метод применим к химическим веществам (радиоактивно маркированным или немаркированным), для анализа которых был разработан достаточно точный и чувствительный аналитический метод. Он применим к нелетучим, а также практически нелетучим веществам, хорошо растворимым в воде. Метод нельзя использовать для анализа веществ, характеризующихся высокой летучестью из водных растворов (например, фумигантов, органических растворителей), так как нельзя обеспечить наличие вещества в растворе при заданных экспериментальных условиях. Также метод сложно применить к веществам с очень низкой растворимостью в воде.
3.3 Информация об исследуемом веществе
3.3.1 Для определения скорости гидролиза вещества оно может быть как радиоактивно маркированным, так и немаркированным. Как правило, предпочтение отдается маркированному материалу для исследования каскада гидролитических реакций и для расчета баланса вещества; однако в определенных случаях использование радиоактивно маркированного вещества не является обязательным. Рекомендуется вводить изотопы , но возможно использование и других изотопов, таких как
,
,
.
Метку следует вводить в наиболее стабильную часть/части молекулы.
Например, если в структуре вещества содержится одно кольцо, то необходимо ввести метку в это кольцо; если же в структуре вещества два кольца или более, следует проводить отдельные исследования для определения судьбы каждого маркированного кольца и получения достаточной информации об образовании продуктов гидролиза. Чистота исследуемого вещества должна быть не ниже 95%.
3.3.2 До проведения теста на гидролиз должна быть известна следующая информация:
- растворимость в воде [1];
- растворимость в органических растворителях;
- давление паров [2] и/или константа Генри;
- коэффициент разделения н-октанол/вода;
- константа диссоциации () [3];
- скорость прямого и непрямого фотопревращения в воде, если применимо.
3.3.3 Должны быть известны аналитические методы для количественного анализа исследуемого вещества и, если применимо, для идентификации и количественного анализа продуктов гидролиза в водных растворах.
3.4 Вещества сравнения
3.4.1 При возможности должны быть использованы вещества сравнения для идентификации и количественного анализа продуктов гидролиза спектроскопическими и хроматографическими методами или другими подходящими чувствительными методами анализа.
3.5 Единицы измерений
Единицы измерений представлены в приложении В.
3.6 Критерии качества
3.6.1 Эффективность определения
Необходимо провести анализ по крайней мере двух идентичных буферных растворов сразу после добавления исследуемого вещества для изначального подтверждения воспроизводимости аналитического метода и применимости метода внесения исследуемого вещества. Эффективность определения на последующих стадиях эксперимента определяется балансом вещества (при использовании радиоактивно маркированного материала). Она должна находиться в диапазоне от 90 до 110% как для маркированных, так и для немаркированных соединений. Если достичь данного диапазона технически сложно, допускается эффективность определения 70% немаркированного исследуемого вещества. В этом случае следует приводить должное обоснование.
3.6.2 Воспроизводимость и чувствительность аналитического метода
3.6.2.1 Удостовериться в воспроизводимости аналитического метода/методов для количественного определения исследуемого вещества и продуктов гидролиза можно, проведя повторный анализ этих же буферных растворов (или их экстрактов) после того, как образуется значительное количество определяемых продуктов гидролиза.
3.6.2.2 Аналитический метод должен быть достаточно чувствительным для определения количественного содержания исследуемого вещества, вплоть до 10% и менее от его начальной концентрации. Аналитические методы также должны быть достаточно чувствительны для количественной характеристики продуктов гидролиза, составляющих от 10% вносимого исследуемого вещества и более (в любой момент исследования), а также до 25% и менее от его максимальной концентрации.
3.6.3 Доверительные интервалы для кинетических данных реакции гидролиза
Доверительные интервалы должны быть рассчитаны и представлены для всех коэффициентов регрессии, констант скорости реакции, периодов полураспада и любых других кинетических параметров (например, ).
4 Описание метода исследования
4.1 Оборудование и установка
4.1.1 Испытание вещества необходимо проводить в стеклянной посуде (например, в пробирках, небольших флаконах) в темноте и стерильных условиях, если это необходимо, кроме случаев, когда заранее известные параметры (такие как коэффициент разделения н-октанол/вода) указывают на то, что вещество может прилипать к стеклу. В таких случаях возможно использование альтернативных материалов (таких как тефлон). Проблему прилипания вещества к стеклу также можно решить одним из следующих способов:
- определить массы исследуемого вещества и продуктов гидролиза, адсорбировавшихся на стекле;
- использовать ультразвуковую ванну;
- промывать всю тару раствором растворителя в каждый период отбора проб;
- использовать специальные средства;
- использовать увеличенное количество сорастворителя при добавлении исследуемого вещества к тест-системе; при этом необходимо убедиться, что этот сорастворитель не влияет на процесс гидролиза.
4.1.2 Для инкубации растворов обычно используют термостатируемые на водяной бане встряхиватели или термостатически контролируемые инкубаторы.
4.1.3 Необходимо стандартное лабораторное оборудование, включающее, в частности, следующее:
- рН-метр;
- аналитические приборы, такие как оборудование для проведения газовой хроматографии (ГХ), высоко эффективная газовая хроматография (ВЭЖХ), тонкослойной хроматографии, включающее подходящие системы детектирования для анализа радиоактивно маркированных и немаркированных веществ или обратный метод изотопного разведения;
- приборы для идентификации веществ [например, масс-спектрометрии (МС), ГХ-МС, ВЭЖХ-МС, спектроскопии ядерного магнитного резонанса (ЯМР) и др.];
- жидкостной сцинтилляционный счетчик;
- делительные воронки для жидкостной экстракции;
- приборы для концентрирования растворов и экстрактов (например, ротационный испаритель);
- прибор для контроля температуры (например, водяная баня).
4.1.4 Химические реагенты, включающие, например:
- органические растворители (ч.д.а.), такие, как гексан, дихлорметан и др.;
- жидкий сцинтиллятор;
- буферные растворы.
4.1.5 Вся стеклянная тара, вода (ч.д.а.) и буферные растворы, используемые в исследовании, должны быть простерилизованы.
4.2 Внесение исследуемого вещества
4.2.1 В различные буферные растворы следует вносить водный раствор исследуемого вещества (приложение С). Для достижения надлежащего растворения исследуемого вещества при его внесении и смешивании при необходимости можно использовать небольшие количества смешиваемых с водой растворителей (таких как ацетонитрил, ацетон, спирт), как правило, не более 1% в объемном отношении. Если необходимо использование более высоких концентраций растворителей (например, в случае плохорастворимых веществ), это возможно только в том случае, если будет доказано, что растворитель не влияет на гидролитическое разложение исследуемого вещества.
4.2.2 Использование специальных средств в общем случае не рекомендуется, так как нельзя исключить вероятность, что компоненты этих средств оказывают влияние на гидролитическое разложение исследуемого вещества. Использование специальных средств является приемлемой альтернативой в случае плохорастворимых веществ и при адсорбции веществ на стенках стеклянной тары.
4.2.3 При испытании должна быть использована одна концентрация исследуемого вещества, при этом она не должна быть более 0,01 М или половины концентрации насыщения.
4.3 Буферные растворы
4.3.1 Исследование гидролитического разложения вещества следует проводить при значениях рН 4, 7 и 9. Для этого из реагентов и воды (ч.д.а.) должны быть приготовлены соответствующие буферные растворы. Состав некоторых буферных систем приведен в приложении С. Буферная система потенциально может оказать влияние на протекание реакции гидролиза. В этом случае следует заменить буферную систему на альтернативную.
_______________
Рекомендуется использовать боратный или ацетатный буфер вместо фосфатного.
4.3.2 Необходимо установить рН каждого буферного раствора с точностью до 0,1, используя откалиброванный рН-метр.
4.4 Условия проведения испытания
4.4.1 Эксперименты на гидролитическое разложение следует проводить при постоянных температурах. Для дальнейшей экстраполяции результатов важно поддерживать температуру в диапазоне ±0,5°С.
4.4.2 Если заранее неизвестна способность вещества к гидролизу, следует проводить предварительное тестирование (1-й уровень) при температуре 50°С. Кинетические исследования более высоких уровней следует проводить как минимум при трех различных температурах (включая тестирование при 50°С), за исключением случаев, когда вещество оказалось неспособным к гидролитическому разложению при предварительном тестировании 1-го уровня. Рекомендуемый температурный диапазон для проведения исследований - 10-70°С (желательно проведение хотя бы одного теста при температуре 25°С), который включает и температуру 25°С, и большинство температур, с которыми можно столкнуться в реальных условиях.
4.5 Свет и кислород
4.5.1 Возможно применение любых подходящих методов для того, чтобы все исследования на гидролитическое разложение проводились в условиях, исключающих фотолитические эффекты. Также следует принимать все возможные меры для избегания присутствия кислорода в анализируемых растворах (например, барботированием гелием, азотом или аргоном в течение пяти минут перед приготовлением раствора).
4.5.2 Предварительный тест следует проводить в течение пяти дней, а тестирования более высокого уровня - до тех пор, пока не гидролизуются 90% исследуемого вещества, или в течение 30 дней, в зависимости от того, какой период будет короче.
4.6 Проведение испытания
Предварительное испытание проводят при (50±0,5)°С и значениях рН, равных 4,0, 7,0 и 9,0. Если за пять дней степень гидролитического разложения составляет менее 10% исследуемого вещества (![]() 1 года), вещество считается гидролитически стабильным, и обычно дополнительных испытаний не требуется. Предварительное тестирование не требуется, если известно, что вещество является нестабильным при температурах
1 года), вещество считается гидролитически стабильным, и обычно дополнительных испытаний не требуется. Предварительное тестирование не требуется, если известно, что вещество является нестабильным при температурах, характерных для окружающей среды. Используемый аналитический метод должен быть достаточно чувствительным для определения 10% снижения концентрации исследуемого вещества.
_______________
Такая информация может быть получена из других источников, таких как: данные по гидролитическому разложению похожих структурно соединений, из литературных источников или других предварительных полуколичественных исследований гидролитического разложения исследуемого вещества, проведенных на более ранних этапах анализа.
4.7 Гидролиз нестабильных соединений (уровень 2)
Исследования более высокого уровня следует проводить при значениях рН, при которых вещество оказалось нестабильным в ходе предварительного испытания, описанного выше. Буферные растворы, содержащие исследуемое вещество, должны термостатироваться при выбранных температурах. Для определения, протекает ли гидролиз как реакция первого порядка, необходимо проанализировать каждую реакционную смесь таким образом, чтобы получить шесть разделенных во времени точек, соответствующих гидролизу 10-90% вещества. При каждом из шести отборов проб следует анализировать содержание в параллельных пробах (для каждого образца должна быть как минимум одна параллельная проба, содержащаяся в отдельном реакционном сосуде, всего необходимо получить 12 точек). Отбор аликвот из одной совокупной пробы раствора исследуемого вещества является неприемлемым, так как в этом случае невозможно провести анализ изменчивости данных, также данные действия могут привести к загрязнению раствора исследуемого вещества. В конце исследований более высокого уровня (т.е. при 90-процентном гидролизе исследуемого вещества или по истечении 30 дней) следует проводить анализы на стерильность раствора. Однако если разложения (трансформации) не наблюдалось, то тесты на стерильность проводить необязательно.
4.8 Идентификация продуктов гидролиза (уровень 3)
Любые продукты гидролитического разложения исследуемого вещества, соответствующие 10% или более от вносимого вещества, должны быть определены подходящими аналитическими методами.
4.9 Дополнительные исследования
Возможно дополнительное тестирование гидролитически нестабильного вещества при других значениях рН (кроме 4, 7, 9). Например, для изучения поведения вещества в условиях, приближенных к физиологическим, возможно проведение исследования при более низких значениях рН (например, рН 1,2) и при физиологически значимой температуре (37°С).
5 Данные и отчетность
5.1 Обработка результатов
5.1.1 Значения количества исследуемого вещества и продуктов гидролиза следует приводить в процентном отношении от вносимой концентрации в начале эксперимента и в надлежащих случаях в мг/л для каждого отбора проб, при каждом значении рН и температуре проведения исследования. В случае если использовалось радиоактивно маркированное вещество, дополнительно необходимо рассчитать баланс масс, выраженный в процентном отношении от вносимой в начале исследования концентрации тестируемого вещества.
5.1.2 Необходимо графически представить зависимость логарифма концентрации исследуемого вещества от времени. Любые значимые продукты гидролитического разложения исследуемого вещества (равные или более 10% концентрации вносимого вещества) необходимо идентифицировать и также представить на графике зависимость логарифма их концентрации от времени аналогично исходному веществу. Это позволит проанализировать скорости их образования и убыли.
5.1.3 Применяя соответствующие кинетические модели, следует определить более точно значения для периодов полураспада или значений . Необходимо приводить периоды полураспада и/или значения
(включая доверительные пределы) для каждого значения рН и температуры, а также необходимо описать применяемую кинетическую модель и привести коэффициент смешанной корреляции
. В случаях, где это является уместным, необходимо осуществить аналогичные расчеты для продуктов гидролиза.
5.1.4 Если исследования скорости реакции проводились при других температурах, константы скорости реакции гидролиза псевдопервого порядка ![]() могут быть представлены как функции от температуры. Вычисление основывается на представлении
могут быть представлены как функции от температуры. Вычисление основывается на представлении в виде суммы констант скоростей реакции кислотно-, основно- и нейтрально катализируемого гидролиза (
,
,
![]() соответственно) и уравнения Аррениуса:
соответственно) и уравнения Аррениуса:
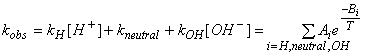 ,
,
где и
- коэффициенты регрессии, рассчитываемые по пересечению графика с осью и наклону прямой, представляющей собой линейную зависимость
от обратного значения абсолютной температуры в кельвинах (
).
Используя уравнение Аррениуса для кислотно-, основно- и нейтрально катализируемого гидролиза, можно вычислить скорости реакции гидролиза псевдопервого порядка и соответственно периоды полураспада для других температур, для которых провести прямое определение констант скорости реакции не представляется практически выполнимым.
5.1.5 Отчет об исследовании должен включать следующую информацию.
Исследуемое вещество:
- общепринятое название, химическое название, номер CAS, структурная формула (включая указание на положение метки, если используется меченный радиоизотопом материал), а также имеющие значение физико-химические свойства;
- чистота (примеси) исследуемого вещества;
- чистота метки маркированного химического вещества и молярная активность (при необходимости).
Буферные растворы:
- дата и описание приготовления растворов;
- используемый буфер и вода;
- молярная концентрация и рН буферных растворов.
Условия проведения испытания:
- дата проведения испытания;
- количество примененного исследуемого вещества;
- метод и растворители (тип и количество), использованные для внесения исследуемого вещества;
- объем инкубируемого буферного раствора, содержащего исследуемое вещество;
- описание метода инкубации растворов;
- рН и температура, при которой проводили исследование;
- время отбора проб;
- методы экстракции;
- методы количественного определения и идентификации исследуемого вещества и продуктов его гидролитического разложения в буферных растворах;
- количество репликаций.
Результаты:
- повторяемость и чувствительность использованных аналитических методов;
- результаты экстракции;
- данные репликаций и средние значения в табличной форме;
- массовый баланс во время и в конце исследования (когда используется радиоактивно маркированное тестируемое вещество);
- результаты предварительного исследования;
- все исходные данные и графики.
Следующая информация является обязательной только в том случае, если необходимо определить скорость гидролитического разложения:
- кривые концентраций относительно времени исследуемых веществ и при необходимости продуктов гидролиза при каждом значении рН и значении температуры;
- таблицы результатов, полученных при применении уравнения Аррениуса для температуры 20-25°С, с рН, константой скорости (ч или день
), периодом полураспада или
, температурой (°С), включая доверительные интервалы и коэффициенты корреляции
или сопоставимые сведения;
- предложенный путь гидролиза.
5.2 Интерпретация и оценка результатов
Большинство гидролитических реакций протекают со скоростями, характерными для реакций первого порядка, и поэтому периоды полураспада не зависят от концентрации [уравнение (4) в приложении В]. Это позволяет применять результаты лабораторных исследований, проводимых при концентрациях 10-10
М, для оценки поведения веществ в условиях окружающей среды (
10
М).
Приложение А
(обязательное)
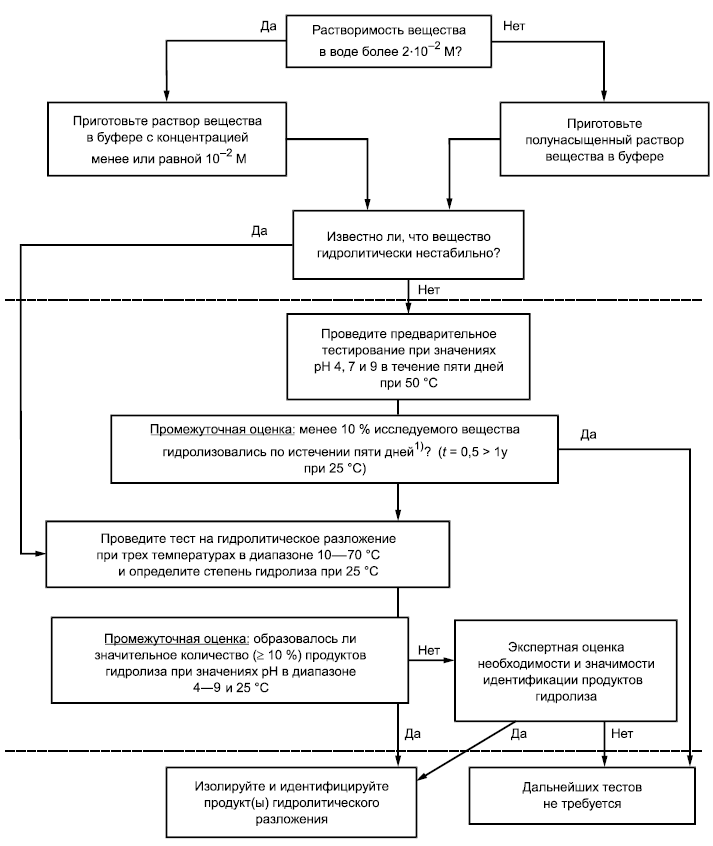
Многоуровневая схема тестирования гидролитического разложения вещества
|
_______________
10-процентный гидролиз исследуемого вещества при 50°С соответствует периоду полураспада, равному примерно 30 дням, что соответствует значению около 1 г при темперетуре 25°С.
Приложение В
(обязательное)
Единицы измерения
Гидролиз - реакция исследуемого вещества c водой, при которой происходит обмен группы
с
-группой в реакционном центре вещества
![]() . (B.1)
. (B.1)
Скорость убывания концентрации в рамках этой упрощенной модели может быть представлена как
скорость![]() , реакция второго порядка,
, реакция второго порядка,
скорость![]() , реакция первого порядка,
, реакция первого порядка,
в зависимости от ступени, определяющей скорость реакции. Так как вода присутствует в избытке к исследуемому веществу, реакции такого типа обычно описываются реакцией псевдопервого порядка, в которой наблюдаемая константа скорости реакции описывается соотношением
![]() (В.2)
(В.2)
и может быть найдена из уравнения
![]() , (В.3)
, (В.3)
где - константа скорости реакции, измеренная при различных температурах,
- время,
и
- концентрации
во времена 0 и
.
_______________
Если график зависимости логарифма концентрации от времени не представляет собой прямую (соответствующую скорости реакции первого порядка), то использование уравнения (3) не является правомочным для определения константы скорости гидролиза исследуемого вещества.
Единица измерения данной константы: (время), а время полураспада (время, при котором прореагирует 50%
) можно определить из соотношения:
![]() . (B.4)
. (B.4)
Определение константы при другой температуре
Если известны константы скорости реакции для двух температур, константа скорости реакции для других температур может быть рассчитана из уравнения Аррениуса:
![]() ,
,
или
![]() .
.
График зависимости от
![]() представляет собой прямую с углом наклона
представляет собой прямую с углом наклона ![]() ,
,
где - константа скорости реакции, измеренная при различных температурах;
- энергия активации, кДж/моль;
- абсолютная температура, K;
- газовая постоянная, 8,314 Дж/(моль
К).
Энергия активации может быть рассчитана с помощью регрессионного анализа или из следующего уравнения
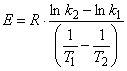 , (В.5)
, (В.5)
где ![]() .
.
Приложение С
(рекомендуемое)
Буферные системы
Таблица С.1 - Буферные растворы Кларка и Лабса
_______________
Приведенные значения рН рассчитаны с помощью стандартных уравнений Соренсена (
![]() ), 1909. Реальные значения рН выше приведенных в таблице В.1 на 0,04.
), 1909. Реальные значения рН выше приведенных в таблице В.1 на 0,04.
Состав | рН |
0,2н | |
47,5 мл | 1,0 |
32,25 мл | 1,2 |
20,75 мл | 1,4 |
13,15 мл | 1,6 |
8,3 мл | 1,8 |
5,3 мл | 2,0 |
3,35 мл | 2,2 |
0,1 М бифталат калия + 0,1н | |
46,70 мл 0,1н | 2,2 |
39,60 мл 0,1н | 2,4 |
32,95 мл 0,1н | 2,6 |
26,42 мл 0,1н | 2,8 |
20,32 мл 0,1н | 3,0 |
14,70 мл 0,1н | 3,2 |
9,90 мл 0,1н | 3,4 |
5,97 мл 0,1н | 3,6 |
2,63 мл 0,1н | 3,8 |
0,1 М бифталат калия + 0,1н | |
0,40 мл 0,1н | 4,0 |
3,70 мл 0,1н | 4,2 |
7,50 мл 0,1н | 4,4 |
12,15 мл 0,1н | 4,6 |
17,70 мл 0,1н | 4,8 |
23,85 мл 0,1н | 5,0 |
29,95 мл 0,1н | 5,2 |
35,45 мл 0,1н | 5,4 |
39,85 мл 0,1н | 5,6 |
43,00 мл 0,1н | 5,8 |
45,45 мл 0,1н | 6,0 |
0,1 М монокалийфосфат + 0,1н | |
5,70 мл 0,1н | 6,0 |
8,60 мл 0,1н | 6,2 |
12,60 мл 0,1н | 6,4 |
17,80 мл 0,1н | 6,6 |
23,45 мл 0,1н | 6,8 |
29,63 мл 0,1н | 7,0 |
35,00 мл 0,1н | 7,2 |
39,50 мл 0,1н | 7,4 |
42,80 мл 0,1н | 7,6 |
45,20 мл 0,1н | 7,8 |
46,80 мл 0,1н | 8,0 |
0,1 М | |
2,61 мл 0,1н | 7,8 |
3,97 мл 0,1н | 8,0 |
5,90 мл 0,1н | 8,2 |
8,50 мл 0,1н | 8,4 |
12,00 мл 0,1н | 8,6 |
16,30 мл 0,1н | 8,8 |
21,30 мл 0,1н | 9,0 |
26,70 мл 0,1н | 9,2 |
32,00 мл 0,1н | 9,4 |
36,85 мл 0,1н | 9,6 |
40,80 мл 0,1н | 9,8 |
43,90 мл 0,1 н | 10,0 |
Таблица С.2 - Цитратный буфер
Состав | рН |
0,1 М цитрат калия однозамещенный + 0,1н | |
49,7 мл 0,1н | 2,2 |
43,4 мл 0,1н | 2,4 |
36,8 мл 0,1н | 2,6 |
30,2 мл 0,1н | 2,8 |
23,6 мл 0,1н | 3,0 |
17,2 мл 0,1н | 3,2 |
10,7 мл 0,1н | 3,4 |
4,2 мл 0,1н | 3,6 |
0,1 М цитрат калия однозамещенный + 0,1н | |
2,0 мл 0,1н | 3,8 |
9,0 мл 0,1н | 4,0 |
16,3 мл 0,1н | 4,2 |
23,7 мл 0,1н | 4,4 |
31,5 мл 0,1н | 4,6 |
39,2 мл 0,1н | 4,8 |
46,7 мл 0,1н | 5,0 |
54,2 мл 0,1н | 5,2 |
61,0 мл 0,1н | 5,4 |
68,0 мл 0,1н | 5,6 |
74,4 мл 0,1н | 5,8 |
81,2 мл 0,1н | 6,0 |
| |
Таблица С.3 - Боратные смеси Соренсена
Состав | Соренсен | Вальбум, рН при | |||
тетрабората натрия, мл |
| 18°С | 10°С | 40°С | 70°С |
0,05 М тетраборат натрия + 0,1н | |||||
5,25 | 4,75 | 7,62 | 7,64 | 7,55 | 7,47 |
5,50 | 4,50 | 7,94 | 7,98 | 7,86 | 7,76 |
5,75 | 4,25 | 8,14 | 8,17 | 8,06 | 7,95 |
6,00 | 4,00 | 8,29 | 8,32 | 8,19 | 8,08 |
6,50 | 3,50 | 8,51 | 8,54 | 8,40 | 8,28 |
7,00 | 3,00 | 8,08 | 8,72 | 8,56 | 8,40 |
7,50 | 2,50 | 8,80 | 8,84 | 8,67 | 8,50 |
8,00 | 2,00 | 8,91 | 8,96 | 8,77 | 8,59 |
8,50 | 1,50 | 9,01 | 9,06 | 8,86 | 8,67 |
9,00 | 1,00 | 9,09 | 9,14 | 8,94 | 8,74 |
9,50 | 0,50 | 9,17 | 9,22 | 9,01 | 8,80 |
10,00 | 0,00 | 9,24 | 9,30 | 9,08 | 8,86 |
0,05 М тетраборат натрия + 0,1н | |||||
10,0 | 0,0 | 9,24 | 9,30 | 9,08 | 8,86 |
9,0 | 1,0 | 9,36 | 9,42 | 9,18 | 8,94 |
8,0 | 2,0 | 9,50 | 9,57 | 9,30 | 9,02 |
7,0 | 3,0 | 9,68 | 9,76 | 9,44 | 9,12 |
6,0 | 4,0 | 9,97 | 10,06 | 9,67 | 9,28 |
Таблица С.4 - Фосфатные смеси Соренсена
Состав | рН |
0,0667 М монокалийфосфат + 0,0667 М динатрийфосфат при 20°С | |
99,2 мл | 3,8 |
98,4 мл | 4,0 |
97,3 мл | 4,2 |
95,5 мл | 4,4 |
92,8 мл | 4,6 |
88,9 мл | 4,8 |
83,0 мл | 5,0 |
75,4 мл | 5,2 |
65,3 мл | 5,4 |
53,4 мл | 5,6 |
41,3 мл | 5,8 |
29,6 мл | 6,0 |
19,7 мл | 7,4 |
12,8 мл | 7,6 |
7,4 мл | 7,8 |
3,7 мл | 8,0 |
Библиография
[1] OECD (1981). Hydrolysis as a Function of pH. OECD Guideline for Testing of Chemicals Nr. 111, adopted 12 May 1981
[2] US-Environmental Protection Agency (1982). 40 CFR 796.3500, Hydrolysis as a Function of pH at 25 С. Pesticide Assessment Guidelines, Subdivision N. Chemistry: Environmental Fate
[3] Agriculture Canada (1987). Environmental Chemistry and Fate Guidelines for registration of pesticides in Canada
[4] European Union (EU) (1995). Commission Directive 95/36/EC amending Council Directive 91/414/EEC concerning the placing of plant protection products on the market. Annex V: Fate and Behaviour in the Environment
[5] Dutch Commission for Registration of Pesticides (1991). Application for registration of a pesticide. Section G: Behaviour of the product and its metabolites in soil, water and air
[6] BBA (1980). Merkblatt Nr. 55, Teil I und II: ![]() des Verhaltens von Pflanzenbehandlungsmitteln im Wasser (October 1980)
des Verhaltens von Pflanzenbehandlungsmitteln im Wasser (October 1980)
[7] SETAC (1995). Procedures for Assessing the Environmental Fate and Ecotoxicity of Pesticides. Mark R. Lynch, Ed
[8] OECD (2000). Guidance document on aquatic toxicity testing of difficult substances and mixtures, OECD Environmental Health and Safety Publications Series on Testing and Assessment Nr .23
[9] OECD (1993). Guidelines for the Testing of Chemicals. Paris. OECD (1994-2000): Addenda 6-11 to Guidelines for the Testing of Chemicals
[10] Nelson H., Laskowski D., Thermes S., and Hendley P. (1997). Recommended changes in pesticide fate study guidelines for improving input to computer models. (Text version of oral presentation at the 14th Annual Meeting of the Society of Environmental Toxicology and Chemistry, Dallas TX, November 1993)
[11] Mabey W. and Mill T. (1978). Critical review of hydrolysis of organic compounds in water under environmental conditions. J. Phys. Chem. Ref. Data 7, 383-415
УДК 658.382.3:006.354 | МКС 71.100.01 |
Ключевые слова: химическая продукция, воздействие на окружающую среду, окружающая среда, метод испытаний, гидролиз | |
Электронный текст документа
и сверен по:
, 2019