ГОСТ 33060-2014
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ
ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Изучение адсорбции-десорбции замкнутым равновесным методом
Method of testing the chemicals hazardous to the environment. Adsorption-desorption using a batch equilibrium method
МКС 71.040.50
Дата введения 2023-12-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием "Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ" (ФГУП "ВНИЦСМВ") на основе собственного перевода на русский язык англоязычной версии документа, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 20 октября 2014 г. N 71-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
Азербайджан | AZ | Азстандарт |
Армения | AM | ЗАО "Национальный орган по стандартизации и метрологии" Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Киргизия | KG | Кыргызстандарт |
Молдова | MD | Институт стандартизации Молдовы |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 25 октября 2023 г. N 1234-ст межгосударственный стандарт ГОСТ 33060-2014 введен в действие в качестве национального стандарта Российской Федерации с 1 декабря 2023 г.
5 Настоящий стандарт идентичен международному документу OECD Test No. 106* "Изучение адсорбции-десорбции замкнутым равновесным методом" ("Adsorption-Desorption Using a Batch Equilibrium Method", IDT).
Наименование настоящего стандарта изменено относительно указанного международного документа для приведения в соответствие с ГОСТ 1.5 (подраздел 3.6)
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных (государственных) стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
Введение
Это Руководство основано на предложении, представленном Европейской Комиссией в 1993 году, и учитывает замечания, сделанные странами - членами ОЭСР. Определенная деятельность предпринималась в Европейском союзе по разработке этого вида испытаний. Она включала интенсивные исследования с участием и в тесном сотрудничестве Федерального министерства Германии по охране окружающей среды (UBA), университета Киля, Европейской Комиссии и Объединенного Исследовательского Центра Испры (Италия) [1], [2]. В 1988 году UBA организовало кольцевой тест с участием 27 лабораторий стран Европейского союза [3]. В 1995 году в Белгирате (Италия) был проведен семинар ОЭСР по выбору почв для данного теста [4], где также были одобрены основные его элементы.
Другие руководства по адсорбции-десорбции существуют только на национальном уровне и в основном используются для испытаний пестицидов [5]-[11].
Значимость и применимость метода заключается в следующем:
1 Адсорбционно-десорбционные исследования весьма полезны для получения ценной информации о передвижении и распределении химических веществ в почве, воде и воздухе [12]-[21]. Они могут использоваться для оценки или прогноза способности химического вещества к разложению, трансформации или поглощению микроорганизмами, его вымывания из почвенного профиля, улетучивания из почвы и смыва с ее поверхности в природные водоемы. Адсорбционные данные также могут быть использованы для сравнения химических веществ и для математического моделирования их поведения в почве.
2 Распределение химического вещества между твердой и водной фазами почвы - это сложный процесс, зависящий от многих параметров: химической природы вещества, свойств почв и климатических факторов, таких как температура, осадки, уровень солнечной радиации и ветер. Таким образом, множество явлений и механизмов включаются в процесс адсорбции химических веществ почвой и не могут быть в полной мере объяснены при помощи упрощенных лабораторных моделей, представленных в этом Руководстве. Однако, несмотря на то, что такого рода исследования не могут описать все возможные в природе случаи, они все равно дают нам важную информацию об адсорбции химических веществ почвой в естественных условиях.
1 Область применения
1.1 Данный стандарт предназначен для оценки сорбционно-десорбционного поведения различных веществ в почве. С его помощью можно получать значения величин сорбции для предсказания поведения веществ в различных природных условиях: с этой целью коэффициент равновесной сорбции определяется как функция почвенных характеристик (содержание органического вещества, гранулометрический состав, сложение почвы, pH и др.). Поэтому приходится использовать различные типы почв с целью оценки всех возможных взаимодействий данного вещества с почвой в естественных условиях.
1.2 В данном стандарте адсорбция представляется как процесс связывания химического вещества поверхностью почвенных частиц. Здесь она не разделяется на различные сорбционные процессы (физическая и химическая сорбция) и такие явления, как поверхностное каталитическое разложение, объемная адсорбция и поверхностные химические реакции. Адсорбция, происходящая на почвенных коллоидных частицах (<0,2 мкм), постоянно генерируемых почвой, не принимается в расчет в полной мере.
1.3 Почвенные параметры, которые являются наиболее важными для изучения сорбции, - это содержание органического углерода [3], [4], [12]-[14], [41], [43], [44]-[48], гранулометрический состав и сложение почвы [3], [4], [41]-[48], pH для веществ, способных к ионизации [3], [4], [42]. Другие почвенные характеристики, которые могут оказать влияние на сорбционно-десорбционное равновесие, такие как эффективная емкость катионного обмена, содержание аморфных гидроксидов железа и алюминия, особенно нужно принимать в расчет при исследовании вулканических, тропических почв [4] и почв со специфической поверхностью [49].
1.4 Тест, служащий для оценки адсорбции химического вещества почвами разных типов, различающихся по содержанию органического вещества, гранулометрическому составу, сложению и рН, включает в себя три стадии:
1) подготовительная стадия служит для определения:
- соотношения почва - раствор;
- количества исследуемого вещества, сорбируемого почвой, и времени установления равновесия;
- количества вещества, сорбируемого стенками тестовой посуды, и стойкости вещества во время проведения тестов.
3) построение изотермы сорбции Фрейндлиха для установления влияния концентрации вещества на степень адсорбции его почвой. Исследование кинетики десорбции и построение десорбционной изотермы Фрейндлиха приведены в приложении A.
2 Нормативные ссылки
В настоящем стандарте нормативные ссылки отсутствуют.
3 Термины и определения
Определения, обозначения и единицы измерения даны в разделе "Данные и отчет" и приложении B. Масса почвы в приведенных в них уравнениях приведена к абсолютно сухой почве.
4 Принцип теста
4.2 Как вариант, количество адсорбированного вещества может быть определено и напрямую анализом почвы (прямой метод). Хотя это делает процедуру определения более длинной и трудоемкой, так как появляется необходимость проводить экстракцию вещества из почвы соответствующим растворителем, тот метод можно рекомендовать в тех случаях, когда разницу между начальной и конечной концентрацией вещества трудно определить с нужной точностью. Примеры таких случаев: адсорбция вещества стенками посуды; нестабильность вещества во время эксперимента; слабая адсорбция, приводящая к незначительным изменениям концентрации вещества в растворе; наоборот, сильная адсорбция, которая оставляет в растворе незначительные количества вещества, которые трудно определить с необходимой точностью. При использовании радиоактивной метки процесс экстракции может быть заменен сжиганием почвенной фазы и измерением радиоактивности сцинтилляционным методом. Однако данный метод не позволяет отделить радиоактивность самого вещества от радиоактивности его метаболитов, поэтому он может применяться только для веществ, стабильных в течение всего эксперимента.
5 Информация о тестируемом веществе
5.1 Химические реагенты должны быть аналитической чистоты. При использовании радиоактивно немеченых тестируемых веществ известного состава рекомендуется использовать образцы не менее 95% чистоты. Когда используют радиоактивно меченые тестируемые вещества, то они не должны быть известного состава и не должны содержать радиоактивных примесей. В случае если вещество радиометки малостабильно, то это должно быть соответствующим образом учтено.
5.2 Перед проведением теста по адсорбции-десорбции необходимо иметь следующую информацию о тестируемом веществе:
- растворимость в воде;
- давление паров или константу Генри;
- функцию зависимости абиотического гидролиза от pH;
- коэффициент распределения n-октанол/вода;
- способность к биодеградации или аэробной и анаэробной трансформации в почве;
- прямой фотолиз в воде (поглощение в УФ и видимой части спектра, квантовый выход) и фотодеградация в почве.
6 Применимость теста
6.1 Данный тест применим для всех веществ, для которых разработаны достаточно точные аналитические методы их определения. Важный параметр, влияющий на достоверность полученных результатов, особенно, если используют непрямой метод, это стойкость вещества во время теста. Поэтому в предварительных исследованиях обязательно должна проверяться стабильность вещества. Если обнаружено его разложение в ходе эксперимента, то рекомендуется анализировать как водную, так и твердую фазу почвы.
6.3 При работе с летучими веществами соблюдайте осторожность, чтобы избежать потерь вещества в процессе теста.
7 Описание теста
7.1 Оборудование и химические реагенты
Стандартное лабораторное оборудование приведено ниже.
Пробирки и колбы для проведения экспериментов. Эти пробирки или колбы должны иметь возможность напрямую устанавливаться в центрифугу во избежание потерь при перенесении вещества и должны быть сделаны из инертного материала, минимально адсорбирующего тестируемое вещество.
Перемешивающее устройство: круговой встряхиватель или аналогичное оборудование, способное создавать почвенную суспензию.
Центрифуга, лучше высокоскоростная с ускорением более 3000g, термостатированная и способная осаждать из водного раствора частицы крупнее 0,2 мкм. В ходе взбалтывания и центрифугирования посуда должна быть закрыта крышками во избежание потерь раствора и улетучивания вещества из суспензии. Чтобы минимизировать адсорбцию, следует использовать крышки из инертных покрытий, таких как тефлон (Teflon®).
Дополнительное оборудование: фильтровальная установка; фильтры с диаметром пор менее 0,2 мкм, одноразовые, стерильные. Чтобы избежать потерь тестируемого вещества на фильтрах, следует обратить особое внимание на материал, из которого они изготовлены. Для малорастворимых тестируемых веществ фильтры из органических материалов не рекомендуются.
Аналитическое оборудование: приборы, способные определить концентрацию тестируемого вещества.
Лабораторный сушильный шкаф должен поддерживать температуру 103°C-110°C.
7.2 Характеристики почв и их выбор
7.2.1 Почвы должны быть охарактеризованы потрем основным параметрам, наиболее сильно влияющим на адсорбционную способность: содержание органического углерода, гранулометрический состав, сложение почвы и pH. Как уже упоминалось в 1.3, другие физико-химические свойства почвы могут влиять на адсорбцию-десорбцию некоторых веществ, и их следует также учитывать в таких случаях.
7.2.3 Инструкция по выбору почв для сорбционно-десорбционных экспериментов приведена в таблице 1. Семь выбранных почв обычно широко распространены в умеренной температурной географической зоне. Для веществ, способных к ионизации, выбранные почвы должны покрывать достаточно широкий интервал pH, чтобы определить адсорбцию данного вещества как в ионизованной, так и в неионизированной форме. Указание, какое количество почв использовать на различных этапах эксперимента, приведено в разделе "Проведение теста".
7.2.4 Иногда, кроме указанных почв, возникает необходимость исследовать почвы холодных, умеренных или тропических поясов стран ОЭСР. Однако, даже если выбираются другие почвенные типы, они должны характеризоваться сходными почвенными параметрами и иметь варьирование этих параметров, подобно почвам, приведенным в таблице 1, даже если их нельзя сопоставить в полной мере.
Таблица 1 - Выбор почв для теста по адсорбции/десорбции
Тип почвы | Диапазон pH (в 0,01M ) | Содержание органического углерода, % | Содержание глины, % | Гранулометрический состав |
1 | 4,5-5,5 | 1,0-2,0 | 65-80 | Глина |
2 | >7,5 | 3,5-5,0 | 20-40 | Глинистый суглинок |
3 | 5,5-7,0 | 1,5-3,0 | 15-25 | Илистый суглинок |
4 | 4,0-5,5 | 3,0-4,0 | 15-30 | Суглинок |
5 | <4,0-6,0 | <0,5-1,5 | <10-15 | Песчаный суглинок |
6 | >7,0 | <0,5-1,0 | 40-65 | Глинистый суглинок/глина |
7 | <4,5 | >10 | <10 | Песок/суглинистый песок |
Классификации FAO и US (85). Лучше, если значение укладывается в приведенный интервал. При трудностях с поиском такого образца используют значение ниже минимального. Для почв с содержанием органического углерода менее 0,3% не всегда наблюдается корреляция этого показателя с адсорбцией. Рекомендуется использовать почвы с содержанием органического углерода более 0,3%. | ||||
7.3 Отбор и хранение почвенных образцов
7.3.1 Пробоотбор
Никаких специфических требований к отбору образцов не предъявляется. Техника отбора проб зависит от целей, поставленных в исследовании [53]-[58].
Должны быть соблюдены следующие правила:
- необходима детальная информация о поле, на котором происходил отбор проб; она должна включать в себя расположение поля, произрастающую на нем культуру, историю внесения удобрений и пестицидов, знание о биологических добавках и техногенных загрязнениях. Для описания места отбора проб рекомендуется использовать соответствующие рекомендации [58];
- отобранные образцы следует транспортировать в контейнерах и при температурных условиях, гарантирующих, что в процессе транспортировки не произойдет существенных изменений почвенных свойств.
7.3.2 Хранение
Для анализа рекомендуется брать свежеотобранные образцы почв. В тех случаях, когда это невозможно, почву хранят при температуре окружающей среды в воздушно-сухом состоянии. Нет максимального срока хранения почвенных образцов, однако для почв, хранящихся более трех лет, необходимо перед тестом заново определить содержание органического углерода, pH и емкость катионного обмена.
7.3.3 Подготовка проб почв для теста
7.3.3.1 Почва должна находиться в воздушно-сухом состоянии. Температура в лаборатории должна быть в пределах 20°C-25°C. Дезагрегацию необходимо проводить с минимальными усилиями, чтобы структура почвы изменилась настолько слабо, насколько это возможно. Почва должна быть просеяна через сито с диаметром отверстий 2 мм в соответствии с рекомендациями [58]. Перемешивание почвы следует проводить тщательно, это повысит воспроизводимость результатов.
7.3.3.2 Влажность почвы определяют в трех повторностях методом высушивания в сушильном шкафу при температуре 105°C до тех пор, пока вес образцов не перестанет меняться. Все расчеты следует производить на абсолютно сухую навеску.
7.3.4 Подготовка тестируемого вещества для внесения в почву
7.3.4.2 Исходный головной раствор должен быть приготовлен непосредственно перед экспериментом и должен храниться в темноте при температуре 4°C. Максимально возможное время хранения зависит от стабильности вещества и его концентрации в растворе.
8 Предварительные условия для проведения адсорбционно-десорбционного теста
8.1 Аналитический метод
8.1.1 Ключевыми параметрами, влияющими на точность сорбционных исследований, являются: точность аналитического метода определения концентрации вещества, как в водной фазе, так и в почве; чистота и стабильность тестируемого вещества; достижение сорбционного равновесия; величина изменения концентрации раствора; соотношение почва - раствор и изменение почвенной структуры в процессе достижения равновесия (8.1.4, 9.2.1.12, 9.2.2, 9.2.3.1). Некоторые примеры, касающиеся вопросов точности результатов, приведены в приложении C.
8.1.2 Возможность использования того или иного аналитического метода необходимо оценивать с учетом тех концентраций, которые необходимо будет определять. Каждый исследователь может выбрать метод, подходящий ему по точности, воспроизводимости, пределу определения и открываемости. Некоторые рекомендации по выбору метода даны ниже.
8.1.4 Один раствор (холостой вариант) анализируют без добавления тестируемого вещества, чтобы определить возможные инструментальные ошибки, связанные с матрицей почвы.
8.1.5 Аналитические методы, которые можно использовать для измерения концентрации веществ, включают в себя газожидкостную хроматографию (ГЖХ), высокоэффективную жидкостную хроматографию (ВЭЖХ), спектрометрию и сцинтилляционные исследования (для радиоактивно меченых веществ). Независимо от выбранного метода определения, он должен давать 90%-110%-ную открываемость для используемых концентраций вещества. Чтобы правильно рассчитать величину сорбции, после того как вещество разделилось между фазами, необходимо, чтобы минимальный предел детектирования был на два порядка ниже его определяемой концентрации.
8.1.6 Знание характеристик и предела детектирования аналитического метода определения необходимо для изучения адсорбции и играет важную роль в экспериментальной части исследования в целом. Далее в этом стандарте речь пойдет об основной части эксперимента и будут даны рекомендации для приготовления альтернативных растворов для тех лабораторий, которые ограничены в использовании аналитических методов и имеют недостаточное оснащение.
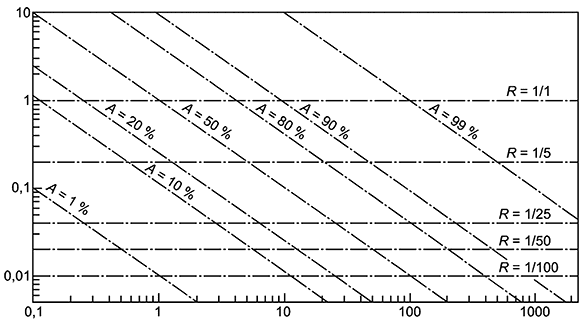
8.2 Выбор оптимального соотношения почва/раствор
 |
9 Проведение теста
9.1 Условия теста
9.1.1 Все эксперименты должны выполняться в лаборатории при температуре окружающей среды. Если возможно, она должна быть постоянной и составлять 20°C-25°C.
9.1.2 Центрифуга должна иметь возможность осаждать из суспензии все почвенные частицы крупнее 0,2 мкм. Такая величина частиц является пограничной между твердой и коллоидной фазой почвы. Указания, как определить параметры центрифугирования, приведены в приложении E.
9.1.3 Если центрифугирование не гарантируют полного удаления из раствора частиц более 0,2 мкм, то оно обязательно должно сочетаться с фильтрованием через фильтры с порами меньше указанной величины. Фильтр должен быть сделан из подходящего инертного материала, исключающего потерю вещества при фильтровании. Однако, в любом случае, отсутствие потерь при фильтровании должно быть проверено.
9.2 Стадия 1. Предварительный эксперимент
Цели проведения предварительного эксперимента указаны в 1.4. Далее будет описано проведение эксперимента.
9.2.1 Выбор оптимального соотношения почва/раствор
9.2.1.1 Для проведения эксперимента необходимы две почвы разных типов и три различных соотношения (итого шесть экспериментов). Почва одного типа должна содержать много органического вещества и небольшое количество глины; почва другого типа, напротив, должна быть с высоким содержанием глины и бедна органическим веществом. Соотношения, которые необходимо получить, приведены ниже. Однако абсолютные масса почвы и объем могут варьироваться с учетом лабораторной необходимости:
50 г почвы и 50 мл водного раствора исследуемого вещества (1/1);
10 г почвы и 50 мл водного раствора исследуемого вещества (1/5);
2 г почвы и 50 мл водного раствора исследуемого вещества (1/25).
9.2.1.2 Минимальное количество почвы, которое может быть использовано, зависит от лабораторных возможностей и возможностей выбранного аналитического метода. Однако для получения реалистичных результатов необходимо использование не менее 1-2 г образца почвы.
9.2.1.5 Все эксперименты, включая контрольные и холостые образцы, необходимо проводить, по крайней мере, в двух повторностях. Общее количество образцов, которые необходимо приготовить, можно рассчитать, используя технику, приведенную в 9.2.1.11.
9.2.1.6 Методы основных предварительного и основного эксперимента обычно одинаковы, кроме тех случаев, когда это нецелесообразно.
9.2.1.8 Приведем пример расчета концентрации головного раствора. Пусть предел обнаружения аналитического метода 0,01 мкг/мл и происходит 90%-ная сорбция. Тогда концентрация вещества в растворе, уравновешенном с почвой, должна быть на два порядка выше (1 мкг/мл). Если решено добавлять к 45 мл раствора максимально рекомендуемую часть (10%), значит, концентрация головного раствора должна быть 10 мкг/мл, что в конечном итоге на три порядка больше предела детектирования.
9.2.1.9 Необходимо измерить рН водной фазы до и после добавления раствора исследуемого вещества, так как этот параметр сильно влияет на сорбцию, особенно ионизированных веществ.
9.2.1.10 Далее проводят взбалтывание суспензии для наступления равновесия. Время его наступления варьирует в широких пределах, но 24 часов обычно заведомо достаточно для его наступления. На предварительном этапе исследования можно провести серию экспериментов с разными временами взбалтывания, например, 4, 8, 24, 48 часов. Однако время анализа может быть гибким в зависимости от графика работы лаборатории.
9.2.1.11 Существует два способа для определения исследуемого вещества в растворе: параллельный и серийный методы. Следует подчеркнуть, что параллельный метод более трудоемкий, но математическая интерпретация результатов проще. Однако конечный выбор остается за исследователем, который должен учитывать возможности и ресурсы своей лаборатории.
(a) Параллельный метод. Образцы с соответствующим соотношением почва/раствор, приготовляют в таком количестве, сколько будет выбрано временных интервалов для изучения кинетики сорбции. После центрифугирования и, если это необходимо, фильтрования, водная фаза из первой пробирки анализируется, скажем, через 4 часа. То же проводят со второй пробиркой через 8 часов, с третьей - через 24 часа и т.д.
(b) Серийный метод. Приготовляют только одну пробирку (в двух повторностях) и через определенные промежутки времени раствор центрифугируют и из жидкой фазы отбирают небольшую аликвоту, которая немедленно анализируется. Дальнейший эксперимент продолжается с исходной суспензией. Если необходима еще и фильтрация, то лаборатория должна располагать соответствующим оборудованием для фильтрации микроколичеств раствора. Рекомендуется, чтобы объем аликвоты не превышал 1% от общего объема раствора, так чтобы изменение соотношения почва/раствор, влияющее на сорбционное равновесие, не было очень значительным.
9.2.2 Определение времени адсорбционного равновесия и количества тестируемого вещества, адсорбированного при равновесии
9.2.2.2 Если для некоторых образцов равновесие так и не наступило, а обнаруживается устойчивый рост, это может быть следствием совокупности факторов, таких как биодеградация или крайне медленная диффузия. Для установления явления биодеградации, необходимо повторить эксперимент со стерильными образцами почвы. В том случае, если и после такой проверки, равновесие не достигается, необходимо изучить данное явление с целью нахождения других возможных влияющих факторов. Это можно попытаться сделать, изменяя температуру, время взбалтывания или соотношение почва/раствор. В конечном итоге решение о продолжении исследования, несмотря на возможные ошибки в достижении равновесия, остается за исследователем.
9.2.3 Адсорбция тестируемого вещества на поверхности посуды и его стабильность
9.2.3.1 Некоторая информация о стабильности вещества и его сорбции на стенках лабораторной посуды может быть получена из анализа контрольных образцов. Если обнаруженная потеря составляет больше стандартной ошибки выбранного аналитического метода измерения концентрации, то абиотическая деградация и/или сорбция на стенках посуды должны быть непременно учтены. Разница между этими двумя явлениями может быть определена тщательным промыванием стенок посуды подходящим растворителем с последующим анализом полученной жидкости. Если сорбция не обнаружена, значит, вещество способно к абиотической деградации. Если сорбция имеет место, необходимо поменять материал, из которого сделана посуда. Однако данные по сорбции на стенках сосудов не могут быть переведены на эксперименты с присутствием почвы, так как ее присутствие обычно значительно снижает такую сорбцию.
9.2.3.2 Дополнительная информация о стабильности вещества может быть получена расчетом массового баланса исходного вещества с течением времени. Это означает, что и водная фаза, и почвенный экстракт, и стенки сосудов должны быть проанализированы. Разница между массами складывается и полученная сумма масс исследуемого вещества в водной фазе, почвенном экстракте и на стенках посуды эквивалентна массе разложившегося, и/или испарившегося, и/или неэкстрагированного вещества. Для определения массового баланса сорбционное равновесие должно быть достигнуто в течение эксперимента.
9.2.3.3 Расчет массового баланса должен проводиться для обеих почв для одного такого соотношения почва/раствор, которое обеспечивает сорбцию более 20%, а в лучшем случае более 50%. Когда эксперимент по определению соотношения почва/раствор завершен, исследование продолжает анализ последнего образца почвенной суспензии (48 часов). Водную фазу отделяют центрифугированием и, если необходимо, фильтруют. После удаления водной фазы, настолько полно, насколько это возможно, к почве добавляют растворитель с высокой экстрагирующей силой (коэффициент экстракции, по крайней мере, 95%). Рекомендуется сделать две последовательные экстракции. Количество исследуемого вещества в почве и на стенках сосуда определяют, и рассчитывают массовый баланс [уравнение (10) в разделе "Данные и отчет"]. Если он получается менее 90%, исследуемое вещество считается нестабильным в течение эксперимента. Однако эксперимент может быть продолжен, принимая при конечном расчете этот установленный факт. В таких случаях рекомендуется анализировать как водную, так и твердую фазу почвы.
9.3 Стадия 2. Кинетика адсорбции при одной концентрации тестируемого вещества
9.3.1 Используют пять разных почв. Критерии отбора приведены в таблице 1. Рекомендуется, чтобы среди этих почв были также некоторые или все почвы, которые исследовали на предварительном этапе. В этом случае для этих почв повторять второй этап исследования нет необходимости.
9.3.2 Время равновесия, соотношение почва/раствор, массу почвенного образца, объем и концентрацию раствора, контактирующего с почвой, выбирают исходя из результатов предварительных исследований. Анализы желательно проводить спустя 2, 4, 6, 8 и, если возможно, 10 и 24 часа. Максимальное время анализа можно довести и до 48 часов, если для вещества характерно долгое установление равновесия. Однако указанные значения временных интервалов можно изменять по своему усмотрению.
9.3.5 Результаты и обсуждение теста по кинетике адсорбции
9.4 Стадия 3. Изотермы адсорбции, кинетика десорбции и изотермы десорбции
9.4.1 Изотермы адсорбции
Выбирают пять значений концентрации тестируемого вещества, желательно покрывающие интервал в два порядка. Концентрации вещества следует выбирать с учетом его растворимости и возможности их определения после наступления равновесия. В течение всего эксперимента должно поддерживаться одинаковое соотношение почва/раствор. Адсорбционный тест проводят согласно 9.2.1.2-9.2.1.11 с той лишь разницей, что анализ проводится только один раз по истечении времени наступления равновесия, определенного ранее на втором этапе исследования. Количество вещества в растворе определяют и по его убыли в растворе рассчитывают количество адсорбированного почвой вещества (можно воспользоваться также и прямым методом определения). Строят график зависимости равновесной концентрации вещества в растворе от количества вещества, сорбированного единицей массы почвы (см. раздел "Данные и отчет").
9.4.2 Результаты построения изотермы адсорбции
Среди всех математических моделей сорбции изотерма Фрейндлиха употребляется наиболее часто. Более подробную информацию о сорбционных моделях можно найти у авторов [41], [45], [80]-[82].
9.4.3 Кинетика десорбции
9.4.3.1 Целью данного эксперимента является определение, сорбируется ли исследуемое вещество почвой необратимо. Данная информация очень важна, так как десорбция играет очень важную роль в поведении веществ в почве. Более того, десорбционные данные часто используют для расчета выщелачивания и плоскостного смыва при помощи математического моделирования. Если десорбционные исследования будут проводиться, то рекомендуется, чтобы эксперимент, описанный ниже, был проведен для каждой системы, для которой возможно точное определение в процессе исследования кинетики сорбции.
9.4.3.2 Так же как и в случае кинетики сорбции, существует два метода исследования: параллельный и серийный методы. Выбор одной из приведенных ниже методик зависит от возможностей экспериментатора, исходя из имеющихся ресурсов и оборудования. Следует иметь в виду замечания, сделанные в 9.2.1.11.
9.4.4 Результаты эксперимента по десорбционной кинетике
Обычно графики зависимости процента адсорбции и процента десорбции вещества от времени показывают характеристику обратимости этого процесса, даже если десорбционное равновесие наступает в два раза позже, чем адсорбционное. Если общая десорбция составляет более 75% от общей адсорбции, адсорбция считается обратимой.
9.4.5 Изотермы десорбции
Изотерму десорбции Фрейндлиха определяют для почв, использованных в изучении адсорбции. Десорбционный эксперимент проводят по схеме, приведенной в разделе "Кинетика десорбции" (9.4.3) с той лишь разницей, что анализ водной фазы проводят только один раз в точке десорбционного равновесия. Рассчитывают количество десорбированного вещества, а содержание тестируемого вещества, оставшегося сорбированным, рассчитывают как функцию от содержания вещества в равновесном растворе (раздел "Данные и отчет" и приложение F).
10 Данные и отчет
Аналитические данные представляют в виде таблиц (приложение G). Также приводят индивидуальные измерения и расчеты средних значений. Изотермы адсорбции представляют в графическом виде. Расчеты проводят, как описано в 10.1.
В данных исследованиях полагается, что 1 мл водной фазы весит 1 г. Поэтому соотношение почва/раствор может быть указано в г/г или в г/мл, что здесь по сути одно и то же.
10.1 Адсорбция
где %oc - содержание в почве органического углерода, %;
Таким образом, этот коэффициент сильно зависит от специфических свойств различных фракций гумуса, значительно отличающихся по сорбционной емкости, а также по строению, происхождению и т.д.
10.2 Изотермы адсорбции
Изотерма адсорбции Фрейндлиха показывает соотношение между количеством адсорбированного вещества и его концентрацией в растворе в точке равновесия [8].
Уравнение изотермы Фрейндлиха (8):
в линейной форме:
n - коэффициент регрессии. Обычно коэффициент 1/n находится в интервале 0,7-1,0, указывая на то, что зависимость часто имеет слегка нелинейный характер.
Рисунок 2 - Нормальный и линеаризованный графики изотерм Фрейндлиха
10.3 Баланс масс
Баланс масс рассчитывают как процент вещества, оставшегося после адсорбционного эксперимента от начального количества вещества, введенного в эксперимент.
Обработка данных несколько отличается в зависимости от свойств растворителя. В случае использования растворителя, свободно смешивающегося с водой, количество экстрагированного вещества может быть рассчитано, как приведено в подразделе "Десорбция". Если растворитель не смешивается с водой, расчет количества извлеченного вещества должен быть произведен.
где MB - баланс масс, %;
10.4 Десорбция
Десорбцию определяют как процент десорбированного вещества от предварительно сорбированного в условиях эксперимента:
10.5 Изотермы десорбции
Изотерма десорбции Фрейндлиха показывает соотношение между количеством вещества, оставшимся адсорбированным почвой, и концентрацией вещества в растворе в точке десорбционного равновесия (12).
Для каждой пробирки содержание тестируемого вещества, оставшегося в почве, рассчитывают как:
Десорбционная изотерма Фрейндлиха:
В линейной форме:
n - коэффициент регрессии;
11 Отчет о тесте
Отчет о проведенном тесте должен содержать следующую информацию:
- полное описание использованных почвенных образцов;
- географическое положение поля (широта, долгота);
- дату отбора проб;
- происхождение образцов (сельскохозяйственные земли, лесные почвы и т.д.);
- глубину отбора проб;
- гранулометрический состав;
- содержание органического углерода;
- содержание органического вещества;
- содержание азота;
- соотношение C/N;
- емкость катионного обмена, ммоль/кг;
- всю информацию о сборе и хранении образцов;
- где необходимо, всю дополнительную информацию, способную помочь интерпретировать результаты сорбционно/десорбционных испытаний;
- методы, использованные для определения каждого из параметров;
- информацию об исследуемом веществе;
- температуру эксперимента;
- условия центрифугирования;
- доказательство необходимости использования растворяющих агентов для приготовления головного раствора исследуемого вещества;
- объяснение всех поправок, внесенных в расчеты;
- данные в виде заполненного бланка из приложения G;
- все данные и наблюдения, помогающие интерпретировать результаты анализа.
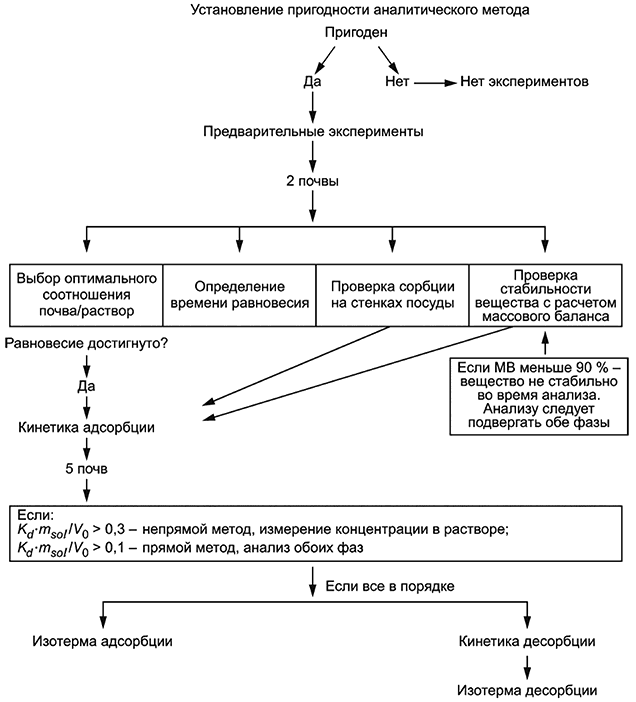
Приложение A
(обязательное)
Схема теста
 |
Приложение B
(обязательное)
Определения и единицы измерения
Таблица B.1
Символ | Определение | Единица измерения |
Процент сорбции во временной точке | % | |
Процент вещества, сорбированного ко времени наступления равновесия | % | |
Масса сорбированного почвой вещества к моменту времени | мкг | |
Масса вещества, сорбированного почвой в течение временного интервала | мкг | |
Масса вещества, сорбированного почвой в точке равновесия | мкг | |
Масса исследуемого вещества в начале анализа | мкг | |
Масса вещества в аликвотном растворе, определенная в точке | мкг | |
Масса вещества в растворе в точке равновесия | мкг | |
Масса почвы в абсолютно сухом состоянии | г | |
Начальная массовая концентрация вещества, контактирующего с почвой | мкг/мл | |
Массовая концентрация головного стандарта | мкг/мл | |
Массовая концентрация вещества в растворе в момент времени | мкг/мл | |
Содержание сорбированного почвой вещества в точке равновесия | мкг/г | |
Массовая концентрация вещества в растворе в точке равновесия | мкг/мл | |
Объем равновесного раствора | мл | |
Объем аликвоты, в которой измеряют содержание исследуемого вещества | мл | |
Коэффициент распределения | мл/г | |
Коэффициент распределения, нормированный по содержанию углерода | мл/г | |
Коэффициент распределения, нормированный по содержанию органического вещества | мл/г | |
Коэффициент адсорбции Фрейндлиха | мкг мл · г | |
1/n | Показатель степени изотермы Фрейндлиха | - |
Процент десорбции во временной точке | % | |
Процент десорбции за время | % | |
Коэффициент десорбции | мл/г | |
Коэффициент десорбции Фрейндлиха | мкг мл · г | |
Масса вещества, десорбированного почвой к моменту времени | мкг | |
Масса вещества, десорбированного почвой, по истечении | мкг | |
Масса вещества, аналитически определяемая в водной фазе в точке десорбционного равновесия | мкг | |
Общая масса вещества, десорбированного почвой к моменту равновесия | мкг | |
Масса вещества, оставшегося сорбированным почвой по истечении временного интервала | мкг | |
Масса исследуемого вещества, оставшаяся в адсорбированном состоянии из-за неполного замещения раствора | мкг | |
Количество вещества, оставшегося сорбированным почвой в точке десорбционного равновесия | мкг/г | |
Массовая концентрация вещества в водной фазе в точке десорбционного равновесия | мкг/мл | |
Полный объем раствора, находящийся в контакте с почвой при проведении эксперимента по кинетике десорбции серийным методом | мл | |
Объем супернатанта, удаленного из пробирки после адсорбционного эксперимента и замененного на аналогичный объем 0,01M | мл | |
Объем анализируемой аликвоты, отбираемой на анализ из пробирки i, при проведении эксперимента по кинетике десорбции серийным методом | мл | |
Объем раствора, взятый из пробирки i, при проведении эксперимента по кинетике десорбции параллельным методом | мл | |
Объем раствора, отбираемого для измерения концентрации исследуемого вещества при десорбционном равновесии | мл | |
MB | Массовый баланс | % |
Общая масса вещества, экстрагированного из почвы и смытого со стенок посуды в два этапа | мкг | |
Объем супернатанта, удаленного из пробирки после адсорбционного равновесия | мл | |
Коэффициент распределения октанол/вода | - | |
pKa | Константа диссоциации | - |
Растворимость | г/л |
Приложение C
(рекомендуемое)
Влияние точности аналитического метода и изменений концентрации на точность результатов эксперимента
Масса почвы 10 г.
Объем раствора 100 мл.
Таблица C.1
, мкг | , мкг/мл | R, % | , мкг | , мкг/г | , % | , % | ||
110 г, | Для A=9% | |||||||
1,100 | 100 | 1,000 | Истинное | 10 | 1,00 | Истинное | 1 | |
мкг/мл | 101 | 1,010 | 1 | 9 | 0,90 | 10 | 0,891 | 10,9 |
105 | 1,050 | 5 | 5 | 0,50 | 50 | 0,476 | 52,4 | |
109 | 1,090 | 9 | 1 | 0,10 | 90 | 0,092 | 90,8 | |
Для A=55% | ||||||||
50,0 | 0,500 | Истинное | 60,0 | 6,00 | Истинное | 12,00 | ||
50,5 | 0,505 | 1 | 59,5 | 5,95 | 0,8 | 11,78 | 1,8 | |
52,5 | 0,525 | 5 | 57,5 | 5,75 | 4,0 | 10,95 | 8,8 | |
55,0 | 0,550 | 10 | 55,0 | 5,50 | 8,3 | 10,00 | 16,7 | |
Для A=99% | ||||||||
1,100 | 0,011 | Истинное | 108,9 | 10,89 | Истинное | 990 | ||
1,111 | 0,01111 | 1 | 108,889 | 10,88 | 0,01 | 980 | 1,0 | |
1,155 | 0,01155 | 5 | 108,845 | 10,8845 | 0,05 | 942 | 4,8 | |
1,21 | 0,0121 | 10 | 108,790 | 10,8790 | 0,10 | 899 | 9,2 | |
R - аналитическая ошибка;
Приложение D
(рекомендуемое)
Вещества | Корреляционные связи | Источник |
Замещенные мочевины | [39] | |
Ароматические хлорсодержащие | [65] | |
Различные пестициды | [66] | |
Ароматические углеводороды | [67] |
Таблица D.2 - Корреляционные уравнения, связывающие сорбционные коэффициенты с растворимостью (дополнительные примеры даны в источниках [68], [69])
Вещества | Корреляционные связи | Источник |
Различные пестициды | [66] | |
Алифатические и ароматические хлорсодержащие | [70] | |
А-нафтолы | [71] | |
Циклические алифатические и ароматические | [72] | |
Различные вещества | [73] |
Приложение E
(справочное)
Расчеты выбора условий центрифугирования
1 Расчет времени центрифугирования проводится по формуле (E.1) для частиц сферической формы:
rpm - количество оборотов в минуту;
Для удобства все единицы измерения даны не в системе СИ.
В повседневной практике полученное таким образом время удваивают, для того чтобы осаждение было гарантированно полным.
2 В данном уравнении также принимается, что вязкость и плотность раствора эквивалентны вязкости и плотности воды при 25°C, соответственно 8,95 г/(с·см) и 1,0 г/мл.
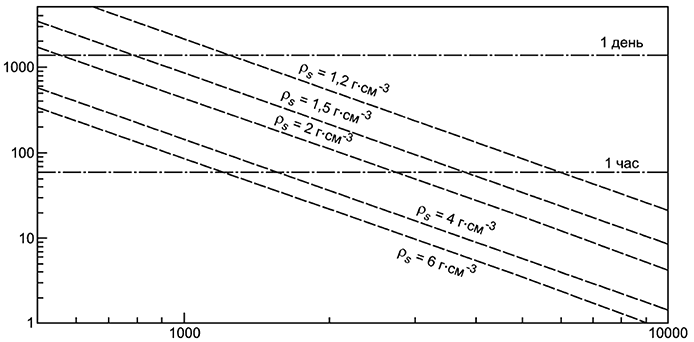
Исходя из этого время центрифугирования будет равно:
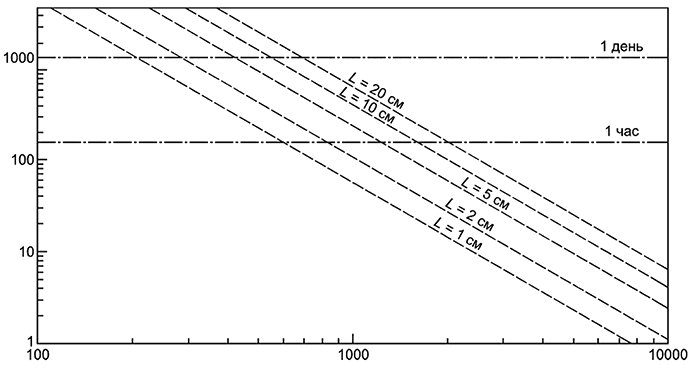
3 Из полученного уравнения (E.2) становится очевидно, что на время центрифугирования влияют два основных параметра: 1) плотность почвы; 2) длина суспензии в центрифужной пробирке (расстояние от поверхности суспензии до дна пробирки). Ясно, что для постоянного объема это расстояние будет зависеть от радиуса пробирки.
5 Кроме того, при подборе условий центрифугирования необходимо также учитывать наличие в почве третьей псевдофазы: почвенных коллоидов. Эти частицы размером менее 0,2 мкм оказывают значительное влияние на адсорбцию веществ почвенной суспензией. Если центрифугирование проводить способом, приведенным выше, то коллоидные частицы остаются в растворе и анализируются совместно с ним. Таким образом, информация об их вкладе в адсорбцию теряется. Если лаборатория располагает приборами для проведения ультрацентрифугирования или ультрафильтрации, то исследования сорбционно-десорбционных процессов можно провести более глубоко, получив информацию об адсорбции на почвенных коллоидах. В этом случае ультрацентрифугирование на скорости 60000 оборотов в минуту или ультрафильтрация через фильтр порозностью в 100000 Дальтон может позволить разделить все три фазы. Итоговый протокол исследования в таком случае должен быть изменен соответствующим образом.
 |
 |
Приложение F
(обязательное)
Расчет адсорбции A (%) и десорбции D (%)
1 Схема эксперимента
2 Во всех расчетах принимается, что вещество стабильно и незначительно сорбируется стенками посуды.
АДСОРБЦИЯ А (%)
a) Параллельный метод
Члены данного уравнения можно рассчитать как:
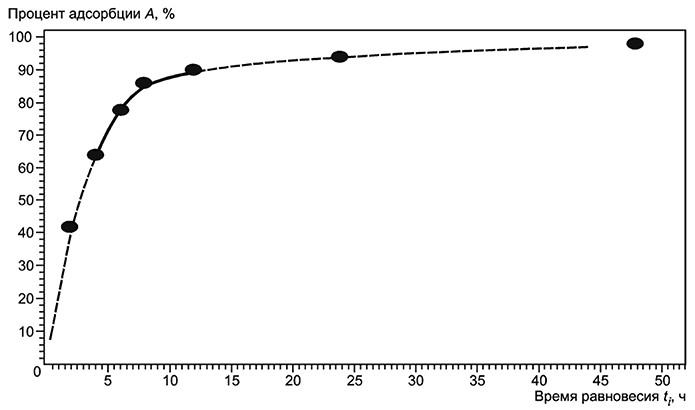 |
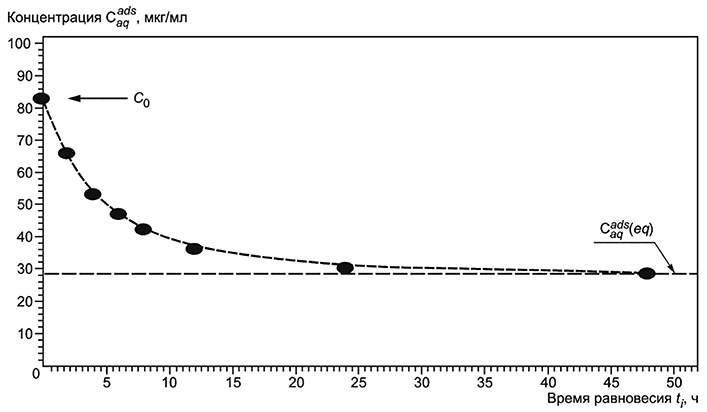 |
b) Серийный метод
4 Следующие уравнения служат для расчета сорбции при проведении эксперимента серийным методом, когда измерение концентрации исследуемого вещества проводится в небольших аликвотах, отбираемых из водной фазы, через определенные временные интервалы.
Количество исследуемого вещества, сорбированного почвой в течение каждого временного интервала, рассчитывают по следующим уравнениям.
в точке равновесия:
масса исследуемого вещества в почве:
масса исследуемого вещества в растворе:
процент адсорбции исследуемого вещества:
Определения использованных выше параметров:
Десорбция D (%)
a) Параллельный метод
b) Серийный метод
Масса вещества в аликвоте связана с массой десорбированного вещества по уравнению:
Количество исследуемого вещества, десорбированного почвой в течение каждого временного интервала, рассчитывают по следующим уравнениям:
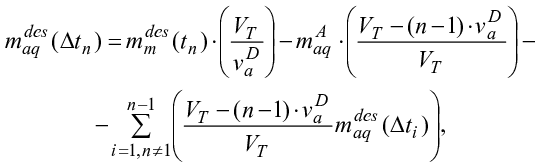
Приложение G
(обязательное)
Сорбция и десорбция в почве. Данные отчета
Исследуемое вещество:
Исследуемые почвы:
Влажность почвы (105°C, 12 часов), %:
Температура, °C:
Применимость аналитического метода
Масса почвы | г | |
Масса абсолютно сухой почвы | г | |
Объем раствора | мл | |
Номинальная концентрация | мкг/мл | |
Определенная концентрация | мкг/мл |
Принцип выбранного аналитического метода: | ||||||||||||
Калибровка аналитического метода: | ||||||||||||
Исследуемое вещество: | ||||||||||||
Исследуемые почвы: | ||||||||||||
Влажность почвы: | % | |||||||||||
Температура: | °C | |||||||||||
Метод анализа: | ||||||||||||
непрямой | параллельный | серийный | прямой | |||||||||
Таблица G.1 - Адсорбционный тест: исследуемые образцы
Символ | Ед. изм. | Время равновесия | Время равновесия | Время равновесия | Время равновесия | |||||
Пробирка N | ||||||||||
Масса влажной почвы | г | |||||||||
Масса сухой почвы | г | |||||||||
Объем воды во влажной почве | мл | |||||||||
Объем раствора , взятый для уравновешивания с почвой | мл | |||||||||
Объем головного раствора | мл | |||||||||
Общий объем водной вазы в контакте с почвой | мл | |||||||||
Начальная концентрация тестового раствора | мкг/мл | |||||||||
Масса исследуемого вещества в начале анализа | мкг | |||||||||
После взбалтывания и центрифугирования | ||||||||||
Непрямой метод | ||||||||||
Параллельный метод | ||||||||||
Концентрация исследуемого вещества с учетом чистого образца | мкг/мл | |||||||||
Серийный метод | ||||||||||
Масса вещества в аликвоте | мкг | |||||||||
Прямой метод | ||||||||||
Масса сорбированного почвой вещества | мкг | |||||||||
Расчет сорбции | ||||||||||
Адсорбция | % | |||||||||
% | ||||||||||
среднее | ||||||||||
Коэффициент | мл/г | |||||||||
среднее | ||||||||||
Коэффициент | мл/г | |||||||||
среднее | ||||||||||
Исследуемое вещество: | ||||
Исследуемые почвы: | ||||
Влажность почвы: | % | |||
Температура: | °C | |||
Таблица G.2 - Адсорбционный тест
Ед. изм. | Чистый | Чистый | Контроль | ||||
Пробирка N | |||||||
Масса влажной почвы | г | 0 | 0 | ||||
Объем воды во влажной почве | мл | - | |||||
Объем раствора , взятый для уравновешивания с почвой | мл | ||||||
Объем головного раствора | мл | 0 | 0 | ||||
Общий объем водной вазы в контакте с почвой | мл | ||||||
Начальная концентрация тестового раствора | мкг/мл | - | - | ||||
После взбалтывания и центрифугирования | |||||||
Концентрация в водной фазе | мкг/мл | ||||||
Исследуемое вещество: | ||||
Исследуемые почвы: | ||||
Влажность почвы: | % | |||
Температура: | °C | |||
Таблица G.3 - Массовый баланс
Символ | Ед. изм. | |||||||||
Пробирка N | ||||||||||
Масса влажной почвы | г | |||||||||
Масса сухой почвы | г | |||||||||
Объем воды во влажной почве | мл | |||||||||
Объем раствора , взятый для уравновешивания с почвой | мл | |||||||||
Объем головного раствора | мл | |||||||||
Общий объем водной вазы в контакте с почвой | мл | |||||||||
Начальная концентрация тестового раствора | мкг/мл | |||||||||
Время равновесия | ч | |||||||||
После взбалтывания и центрифугирования | ||||||||||
Концентрация исследуемого вещества с учетом чистого образца | мкг/мл | |||||||||
Время равновесия | ч | |||||||||
Удаленный объем водной фазы | мл | |||||||||
Добавленный объем раствора | мл | |||||||||
Первая экстракция | ||||||||||
Сигнал прибора, получаемый от растворителя | разн. | |||||||||
Концентрация исследуемого вещества в растворителе | мкг/мл | |||||||||
Масса вещества, экстрагированного из почвы, и смытая со стенок посуды | мкг | |||||||||
Второе разведение с растворителем | ||||||||||
Удаленный объем растворителя | мл | |||||||||
Добавленный объем растворителя | мл | |||||||||
Вторая экстракция | ||||||||||
Сигнал прибора, получаемый от растворителя | разн. | |||||||||
Концентрация исследуемого вещества в растворителе | м кг/мл | |||||||||
Масса вещества, экстрагированного из почвы, и смытая со стенок посуды | мкг | |||||||||
Общая масса вещества, экстрагированная в два этапа | мкг | |||||||||
Массовый баланс | MB | % | ||||||||
Исследуемое вещество: | ||||
Исследуемые почвы: | ||||
Влажность почвы: | % | |||
Температура: | °C | |||
Таблица G.4 - Изотерма адсорбции
Символ | Ед. изм. | |||||||||
Пробирка N | ||||||||||
Масса влажной почвы | г | |||||||||
Масса сухой почвы | г | |||||||||
Объем воды во влажной почве | мл | |||||||||
Объем раствора , взятый для уравновешивания с почвой | мл | |||||||||
Объем головного раствора | мл | |||||||||
Общий объем водной вазы в контакте с почвой | мл | |||||||||
Начальная концентрация тестового раствора | мкг/мл | |||||||||
Время равновесия | - | ч | ||||||||
После взбалтывания и центрифугирования | ||||||||||
Концентрация в водной фазе | мкг/мл | |||||||||
Температура | ||||||||||
Сорбированно ед. массой почвы | м кг/мл | |||||||||
Исследуемое вещество: | ||||||||||
Исследуемые почвы: | ||||||||||
Влажность почвы: | % | |||||||||
Температура: | °C | |||||||||
Метод анализа: непрямой | параллельный | серийный | ||||||||
Таблица G.5 - Десорбционный тест
Символ | Единица измерения | Время | Время | Время | Время | ||
N пробирки, берется из адсорбционного этапа эксперимента | |||||||
Масса вещества, сорбированного почвой в точке равновесия | мкг | ||||||
Объем удаленной из пробирки водной фазы, замененный на 0,01M | мл | ||||||
Полный объем раствора, | PM | мл | |||||
находящийся в контакте с почвой | SM | ||||||
масса исследуемого вещества, оставшаяся в адсорбированном состоянии из-за неполного замещения раствора | мкг | ||||||
Кинетика десорбции | |||||||
Измеренная масса вещества, десорбированного почвой к моменту времени | мкг | ||||||
Объем раствора, отбираемый из | PM | мл | |||||
пробирок на анализ | SM | ||||||
масса вещества, десорбированного почвой к моменту времени (рассчитывается) | мкг | ||||||
масса вещества, десорбированного почвой за время | мкг | ||||||
Процент десорбции | |||||||
процент десорбции во временной точке | % | ||||||
процент десорбции за время | % | ||||||
коэффициент десорбции | мл/г | ||||||
PM - параллельный метод; SM - серийный метод
Библиография
[1] | Kukowski H. and Brummer G. (1987). Investigations on the Adsorption and Desorption of Selected Chemicals in Soils. UBA Report 10602045, Part II | |
[2] | Friinzle O., Kuhnt G. and Vetter L. (1987). Selection of Representative Soils in the EC-Territory. UBA Report 106 02 045, Part 1 | |
[3] | Kuhnt G. and Muntau H. (Eds.). EURO-Soils: Identification, Collection, Treatment, Characterization. Special Publication no. 1.94.60, Joint Research Centre. European Commission, TSPRA, December 1994 | |
[4] | OECD Test Guidelines Programme, Final Report of the OECD Workshop on Selection of Soils/Sediments, Belgirate, Italy, 18-20 January 1995 (June 1995) | |
[5] | US-Environment Protection Agency: Pesticide Assessment Guidelines, Subdivision N, Chemistry: Environmental Fate, Series 163-1, Leaching and Adsorption/Desorption Studies, Addendum 6 on Data Reporting, 540/09-88-026, Date: 1/1988 | |
[6] | US-Environment Protection Agency: Prevention, Pesticides and Toxic Substances, OPPTS Harminized Test Guidelines, Series 835-Fate, Transport and Transformation Test Guidelines, OPPTS No: 835.1220 Sediment and Soil Adsorption/Desorption Isothenn. EPA 0: 712-C-96-048, April 1996 | |
[7] | ASTM Standards, E 1195-87, Standard Test Method for Determining a Sorption Constant (Кос) for an Organic Chemical in Soil and Sediments | |
[8] | Agriculture Canada: Environmental Chemistry and Fate. Guidelines for registration of pesticides in Canada, 15 July 1987 | |
[9] | Netherlands Commission Registration Pesticides (1995): Application for registration of a pesticide. Section G. Behaviour of the product and its metabolites in soil, water and air | |
[10] | Danish National Agency of Environmental Protection (October 1988): Criteria for registration of pesticides as especially dangerous to health or especially harmful to the environment | |
[11] | BBA (1990), Guidelines for the Official Testing of Plant Protection Products, Biological Research Centre for Agriculture and Forestry, Braunschweig, Gennany | |
[12] | Calvet R. (1989). Evaluation of adsorption coefficients and the prediction of the mobilities of pesticides in soils, in Methodological Aspects of the Study of Pesticide Behavior in Soil (ed. P. Jamet), INRA, Paris, (Review) | |
[13] | Calvet R. (1980). Adsorption-Desorption Phenomena, in Interactions between herbicides and the soil. (R.J. Hance ed.), Academic Press, London, pp.83-122 | |
[14] | Hasset J.J. and Banwart W.L. (1989). The sorption of nonpolar organics by soils and sediments, in Reactions and Movement of Organic Chemicals in Soils. Soil Science Society of America (S.S.S.A), Special Publication no. 22, pp.31-44 | |
[15] | van Genuchten M. Th., Davidson J.M., and Wierenga P.J. (1974). An evaluation of kinetic and equilibrium equations for the prediction of pesticide movement through porous media. Soil Sci. Soc. Am. Proc, I8JD, 29-35 | |
[16] | McCall P.I., Laskowski D.A., Swann R.L., and Dishburger H.J. (1981). Measurement of sorption coefficients of organic chemicals and their use, in environmental fate analysis, in Test Protocols for Environmental Fate and Movement of Toxicants. Proceedings of AOAC Symposium, AOAC, Washington DC | |
[17] | Lambert S.M., Porter P.E. and Schieferrstein R.H. (1965). Movement and sorption of chemicals applied to the soil. Weeds, 13, 185-190 | |
[18] | Rhodes R.C., Belasco I.J. and Pease H.L. (1970). Determination of mobility and adsorption of agrochemicals in soils. 1 Agric. Food Chem., 18, 524-528 | |
[19] | Russell M.H. (1995). Recommended approaches to assess pesticide mobility in soil, in Environmental Behavior of Agrochemicals (ed. T.R. Roberts and P.C. Kearney). John Wiley & Sons Ltd | |
[20] | Esser H.O., Hemingway R.J., Klein W., Sharp D.B., Vonk J.W and Holland P.T. (1988). Recommended approach to the evaluation of the environmental behavior of pesticides, IUPAC Reports on Pesticides (24). Pure Appl. Chem., 60, 901-932 | |
[21] | Guth J.A., Burkhard N., and D.O Eberle (1976). Experimental models for studying the persistence of pesticides in soils. Proc. BCPC Symposium: Persistence of Insecticides and Herbicides, pp. 137-157, BCPC, Surrey, UK | |
[22] | Furminge C.G.L. and Osgerby J.M. (1967). Persistence of herbicides in soil. J. Sci. Food Agric., 18, 269-273 | |
[23] | Burkhard N. and Guth J.A. (1981). Chemical hydrolysis of 2-Chloro-4,6-bis(alkylamino)-1,3,5triazine herbicides and their breakdown in soil under the influence of adsorption. Pestic. Sci., 11, 45-52 | |
[24] | Guth J.A., Gerber H.R. and Schlaepfer T. (1977). Effect of adsorption, movement and persistence on the biological availability of soil-applied pesticides. Proc. Br. Crop Prot. Conf., 3, 961-971 | |
[25] | Osgerby IM. (1973). Process affecting herbicide action in soil. Pestic. Sci., 4, 247-258 | |
[26] | Guth J.A. (1972). Adsorptions- und Einwascheverhalten von Pflanzenschutzmitteln in . Schr. Reihe Ver. Wass. - . Berlin-Dahlem, Heft 37,143-154 | |
[27] | Hamaker J.W. (1975). The interpretation of soil leaching experiments, in Environmental Dynamics of Pesticides (eds R. Haque and V.H. Freed), pp.135-172, Plenum Press, N.Y. | |
[28] | Helling C.S. (1971). Pesticide mobility in soils. Soil Sci. Soc. Amer. Proc, 35, 732-210 | |
[29] | Hamaker J.W. (1972). Diffusion and volatilization, in Organic chemicals in the soil environment (C.A.I. Goring and I.W. Hamaker eds), Vol. 1, 49-143 | |
[30] | Burkhard N. and Guth J.A. (1981). Rate of volatilization of pesticides from soil surfaces; Comparison of calculated results with those detennined in a laboratory model system. Pestic. Sci., 12, 37-44 | |
[31] | Cohen S.Z., Creeger S.M., Carse I. R.F. and Enfield C.G. (1984). Potential pesticide contamination of groundwater from agricultural uses, in Treatment and Disposal of Pesticide Wastes, pp. 297-325, ACS Symp. Ser. 259, American Chemical Society, Washington, DC | |
[32] | Gustafson D.I. (1989). Groundwater ubiquity score: a simple method for assessing pesticide leachability 1. Environ. Toxic. Chern., 8(4), 339-357 | |
[33] | Leistra M. and Dekkers W.A. (1976). Computed effects of adsorption kinetics on pesticide movement in soils. 1. Soil Sci., 28, 340-350 | |
[34] | Bromilov R.H. and Leistra M. (1980). Measured and simulated behavior of aldicarb and its oxidation products in fallow soils. Pest. Sci., 11, 389-395 | |
[35] | Green R.E. and Karickoff S.W. (1990). Sorption estimates for modeling, in Pesticides in the Soil Environment: Process, Impacts and Modeling (ed. H.H. Cheng). Soil Sci. Soc. Am., Book Series no. 2, pp. 80-101 | |
[36] | Lambert S.M. (1967). Functional relationship between sorption in soil and chemical structure. J. Agri. Food Chem., 12, 572-576 | |
[37] | Hance R.J. (1969). An empirical relationship between chemical structure and the sorption of some herbicides by soils. 1. Agri. Food Chem., 11, 667-668 | |
[38] | Briggs G.G. (1969). Molecular structure of herbicides and their sorption by soils. Nature, 223, 1288 | |
[39] | Briggs G.G. (1981). Theoretical and experimental relationships between soil adsorption, octanolwater partition coefficients, water solubilities, bioconcentration factors, and the parachor. J. Agric. Food Chem., 29, 1050-1059 | |
[40] | Sabljic A. (1984). Predictions of the nature and strength of soil sorption of organic polutants by molecular topology. J. Agric. Food Chem., 32, 243-246 | |
[41] | Bailey G.W. and White J.L. (1970). Factors influencing the adsorption, desorption, and movement of pesticides in soil. Residue Rev., 32, 29-92 | |
[42] | Bailey G.W., White I.L. and Rothberg Y. (1968). Adsorption of organic herbicides by montomorillonite: Role of pH and chemical character of adsorbate. Soil Sci. Soc. Amer. Proc., 32, 222-234 | |
[43] | Karickhoff S.W. (1981). Semi-empirical estimation of sorption of hydrophobic pollutants on natural sediments and soils. Chemosphere, 10, 833-846 | |
[44] | Paya-Perez A., Riaz M. and Larsen B. (1989). Soil Sorption of 6 Chlorobenzenes and 20 PCB Congeners. Environ. Toxicol. Safety, 21, 1-17 | |
[45] | Hamaker J.W. and Thompson J.M. (1972). Adsorption in organic chemicals, in Organic Chemicals in the Soil Environment (Goring C.A.I. and Hamaker J.W. eds), Vol 1 and, Marcel Dekker, Inc., New York, NY, 1972, pp. 49-143 | |
[46] | Deli J. and Warren G.F. (1971). Adsorption, desorption and leaching of diphenamid in soils. Weed Sci., 19, 67-69 | |
[47] | Chu-Huang Wu, Buehring N., Davinson J.M. and Santelmann (1975). Napropamide Adsorption, desorption and Movement in soils. Weed Science, 23, 454-457 | |
[48] | Haues M.H.B., Stacey M. and Thompson J.M. (1968). Adsorption of s-triazine herbicides by soil organic preparations, in Isotopes and Radiation in Soil Organic Studies, p.75, International. Atomic Energy Agency, Vienna | |
[49] | Pionke H.B. and Deangelis R.J. (1980). Methods for distributing pesticide loss in field run-off between the solution and adsorbed phase, CREAMS, in A Field Scale Model for Chemicals, Runoff and Erosion from Agricultural Management Systems, Chapter 19, Vol. Ill: Supporting Documentation, USDA Conservation Research report | |
[50] | ISO Standard Compendium Environment: Soil Quality - General aspects; chemical and physical methods of analysis; biological methods of analysis. First Edition (1994) | |
[51] | Scheffer F. and Schachtschabcel P. Lehrbuch der Bodenkunde, F. Enke Verlag, Stuttgart (1982), 11-th edition | |
[52] | Black, Evans D.O., White J.L., Ensminger L.E. and Clark F.E., eds. Methods of Soil Analysis, Vol, I and 2, American Society of Agronomy, Madison, Wl, 1982 | |
[53] | ISO/DIS 10381-1 | Soil Quality - Sampling - Part 1: Guidance on the design of sampling programmes |
[54] | ISO/DIS 10381-2 | Soil Quality - Sampling - Part 2: Guidance on sampling techniques |
[55] | ISO/DIS 10381-3 | Soil Quality - Sampling - Part 3: Guidance on safety of sampling |
[56] | ISO/DIS 10381-4 | Soil Quality - Sampling - Part 4: Guidance on the investigation of natural and cultivated soils |
[57] | ISO/DIS 10381-5 | Soil Quality - Sampling - Part 5: Guidance on the investigation of soil contamination of urban and industrial sites |
[58] | ISO 10381-6, 1993 | Soil Quality - Sampling - Part 6: Guidance on the collection, handling and storage of soil for the assessment of aerobic microbial processes in the laboratory |
[59] | Green R.E. and Yamane V.K. (1970). Precision in pesticide adsorption measurements. Soil Sci. Am. Proc., 34, 353-354 | |
[60] | Grover R. and Hance R.J. (1970). Effect of ratio of soil to water on adsorption of linuron and atrazine. Soil Sci., 109-138 | |
[61] | Boesten U.T.I (1990). Influence of soil/liquid ratio on the experimental el1" Or of sorption coefficients in pesticide/soil system. Pest. Sci., 30, 31-41 | |
[62] | Boesten J.J.T.I. Influence of soil/liquid ratio on the experimental error of sorption coefficients in relation to OECD guideline 106. Proceedings of 5th international workshop on environmental behaviour of pesticides and regulatory aspects, Brussels, 26-29 April 1994 | |
[63] | Bastide J., Cantier J.M. and Coste C. (1980). Comportement de substances herbicides dans le sol en fonetion de leur structure chimique. Weed Res., 21,227-231 | |
[64] | Brown D.S. and Flagg E.W. (1981). Empirical prediction of organic pollutants sorption in natural sediments. J. Environ. Qual., 10(3), 382-386 | |
[65] | Chiou C.T., Porter Р.Е. and Schmedding D.W. (1983). Partition equilibria of nonionic organic compounds between soil organic matter and water. Environ. Sci. Technol., 17(4) 227-231 | |
[66] | Gerstl Z. and Mingelgrin U. (1984). Sorption of organic substances by soils and sediments. J. Environm. Sci. Health, 819(3), 297-312 | |
[67] | Vowles P.O. and Mantoura R.F.C. (1987). Sediment-water partition coefficient and HPLC retention factors of aromatic hydrocarbons. Chemosphere, 16(1), 103-116 | |
[68] | Lyman W.J., Reehl W.F. and Rosenblatt D.H. (1990). Handbook of Chemical Property Estimation Methods. Environmental Behaviour of Organic Compounds. American Chemical Society, Washington DC | |
[69] | Keniga E.E. and Goring C.A.I. (1980). Relationship between water solubility, soil sorption, octanol-water partitioning and concentration of chemicals in the biota, in Aquatic Toxicology (eds. J.G. Eaton, et al.), pp.78-115, ASTM STP 707, Philadelphia | |
[70] | Chiou C.T., Peters L.J. and Freed V.H. (1979). A physical concept of soil-water equilibria for nonionic organic compounds. Science, 106, 831-832 | |
[71] | Hassett J.J., Banwart W.I., Wood S.G. and Means J.C. (1981). Sorption of/-Naphtol: implications concerning the limits of hydrophobic sorption. Soil Sci. Soc. Am. J, 45, 38-42 | |
[72] | Karickhoff S.W. (1981). Semi-empirical estimation of sorption of hydrophobic pollutants on natural sediments and soils. Chemosphere, 10(8), 833-846 | |
[73] | Moreale A., van Bladel R. (1981). Adsorption de 13 herbicides et insecticides parl e sol. Relation solubilite- reactivite. Revue de I’Agric., 34(4), 319-322 | |
[74] | M., W. (1996). Comparison of screening methods for the determination/estimation of adsorption coefficients on soil. Chemosphere, 32(12), 2493-2504 | |
[75] | W., Kotthoff G., M. (1995). HPLC - screening method for the detemination of the adsorption coefficient on soil - results of a ring test. Chemosphere 30(7), 1373-1384 | |
[76] | W., Stutte J., Kotthoff G. (1993). HPLC - screening method for the determination of the adsorption coefficient on soil - comparison of different stationary phases. Chemosphere, 27(12), 2341-2352 | |
[77] | Hance R.J. (1967). The speed of Attainment of Sorption Equilibria in Some Systems Involving Herbicides. Weed Research, 7, pp.29-36 | |
[78] | Koskinen W.C. and Harper S.S. (1990). The retention processes: mechanisms, in Pesticides in the Soil Environment: Processes, Impacts and Modelling (ed. H.H. Cheng). Soil Sci. Soc. Am. Book Series, NO.2, Madison, Wisconsin | |
[79] | Cohen S.Z., Creeger S.M., Carsel R.F. and Enfield C.G. (1984). Potential pesticide contamination of groundwater from agricultural uses, in Treatment and Disposal of Pesticide Wastes, pp.297-325, ACS Symp. Ser, 259, American Chemical Society, Washington, DC | |
[80] | Giles C.H. (1970). Interpretation and use of sorption isotherms, in Sorption and Transport Processes in Soils. S.C.I. Monograph No. 37, 14-32 | |
[81] | Giles C.H., McEwan J.H., Nakhwa S.N. and Smith D. (1960). Studies in adsorption: XI. A system of classification of solution adsorption isotherms and its use in the diagnosis of adsorption mechanisms and in measurements of pesticides surface areas of soils. J. Chem. Soc, 3973-93 | |
[82] | Calvet R., Terce M. and Arvien J.C. (1980). Adsorption des pesticides par les sols et leurs constituants: 3. Caracter-istiques generales de I’adsorption. Ann. Agron., 31, 239-251 | |
[83] | Bedbur E. (1996). Anomalies in the Freundlich equation, Proc. COST 66 Workshop, Pesticides in soil and the environment, 13-15 May 1996, Stratford-upon-Avon, UK | |
[84] | Guth J.A. (1985). Adsorption/desorption, in Joint International Symposium, Physicochemical Properties and their Role in Environmental Hazard Assessment, July 1-3, Canterbury, UK | |
[85] | Soil Texture Classification (US and FAO systems): Weed Science, 33, Suppl. 1 (1985) and Soil Sci. Soc. Amer. Proc., 26, 305(1962) | |
УДК 658.382.3:006.354 | МКС 71.040.50 |
Ключевые слова: химическая продукция, окружающая среда, почва, адсорбция, десорбция | |
