ГОСТ 32475-2013
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Оценка биоразлагаемости органических соединений в сброженном осадке сточных вод в анаэробных условиях
Testing of chemicals of environmental hazard. Anaerobic biodegradability of organic compounds in digested sludge
МКС 71.040.50
Дата введения 2014-08-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием "Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ" (ФГУП "ВНИЦСМВ")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 5 ноября 2013 г. N 61)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Киргизия | KG | Кыргызстандарт |
Молдова | MD | Молдова-Стандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 ноября 2013 г. N 810-ст межгосударственный стандарт ГОСТ 32475-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 августа 2014 г.
5 Настоящий стандарт идентичен международному документу OECD Test N 311* "Оценка биоразлагаемости органических соединений в сброженном осадке сточных вод в анаэробных условиях: измерение образования газа" ("Anaerobic Biodegradability of Organic Compounds in Digested Sludge: by Measurement of Gas Production", IDT).
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Наименование настоящего стандарта изменено относительно наименования указанного международного документа для приведения в соответствие с ГОСТ 1.5 (подраздел 3.6)
6 ВВЕДЕН ВПЕРВЫЕ
7 ПЕРЕИЗДАНИЕ. Ноябрь 2019 г.
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
Введение
Поскольку сброженный осадок используется с относительно высокой концентрацией исследуемого вещества и продолжительность испытания обычно больше, чем время его пребывания в анаэробных реакторах, условия теста не всегда соответствуют условиям анаэробных процессов, а также не применимы для оценки анаэробного биоразложения органических химических веществ в других условиях окружающей среды. Осадок подвергается воздействию исследуемого вещества до 60 дней, что превышает обычное время нахождения осадка (от 25 до 30 дней) в анаэробных реакторах, хотя на промышленных объектах время нахождения может быть значительно больше. Прогнозы по результатам данного испытания не могут быть сделаны так убедительно, как в случае аэробного биоразложения, поскольку доказательства, накопленные для описания поведения исследуемых веществ в аэробных испытаниях и при моделировании испытаний также в аэробной среде, являются достаточными для установления связи с разложением; для анаэробной среды существует немного подобных доказательств. Можно предполагать, что полное анаэробное биоразложение происходит, если достигается уровень от 75% до 80% от теоретического выделения газа. Высокое соотношение содержания химического вещества к биомассе, используемое в данном испытании, означает, что химическое вещество, поступающее в анаэробный реактор, вероятно, будет разлагаться в подобных условиях. Кроме того, вещества, которые не могут быть переведены на газ в испытании, необязательно будут устойчивыми при более экологически реалистичных соотношениях вещество - биомасса. Кроме того, происходят другие анаэробные реакции, в которых вещества могут хотя бы частично разлагаться, например, путем дехлорирования, но настоящий тест такие реакции не обнаруживает. Однако, применяя конкретные аналитические методы определения исследуемого вещества, можно контролировать его убывание (см. 2.1.3, 3.12.4, 4.2.2 и 4.8).
1 Область применения
Настоящий стандарт описывает метод для оценки потенциального анаэробного биоразложения органических химических веществ при определенных условиях (например, в анаэробном реакторе в данный момент времени и при определенном диапазоне концентрации микроорганизмов).
2 Основные положения
2.1 Принцип метода
2.1.1 Промытый сброженный осадок с низким (менее 10 мг/л) содержанием неорганического углерода (НУ) десятикратно разбавляют до получения общей концентрации твердых веществ от 1 до 3 г/л и инкубируют в закупоренных сосудах с исследуемым веществом при температуре (35±2)°С в концентрации от 20 до 100 мг содержания углерода на литр в течение не более 60 дней. Активность осадка оценивают с помощью параллельной холостой пробы, содержащей осадок в тестовой среде, но без исследуемого вещества.
________________
Сброженный осадок представляет собой смесь осажденных фаз сточных вод и активного ила, которые были инкубированы в анаэробном реакторе при температуре около 35°С для снижения биомассы и запаха и обезвоживания. Осадок состоит из ассоциации анаэробных ферментативных и метанобразующих бактерий, продуцирующих углекислый газ и метан [11].
2.1.2 Измеряют увеличение давления газовой фазы в сосуде в результате образования углекислого газа и метана. Бльшая часть образовавшегося
будет растворяться в жидкой фазе или переходить в карбонат или гидрокарбонат в условиях испытания. Этот неорганический углерод измеряется в конце испытания.
2.1.3 Количество углерода (неорганического и метана), полученного в результате биоразложения исследуемого вещества, рассчитывают из нетто образования газа и нетто образования НУ в жидкой фазе сверх образованного в пустых контрольных пробах. Степень биоразложения рассчитывают, исходя из общего полученного НУ и углерода в составе метана, как процент от измеренного или рассчитанного количества углерода, добавленного в составе исследуемого вещества. Ход биоразложения можно отследить только путем промежуточных измерений образования газа. Кроме того, основное биоразложение может быть определено путем специальных анализов в начале и конце испытания.
2.2 Информация об исследуемом веществе
Для корректной интерпретации полученных результатов должны быть известны чистота, растворимость в воде, летучесть и адсорбционные характеристики исследуемого вещества. Содержание органического углерода (в процентах по массе) в исследуемом веществе должно быть рассчитано из его химической структуры или определено путем измерения. Для летучих исследуемых веществ необходимо знать измеренные или рассчитанные константы Генри в целях определения возможности использования теста. Для выбора соответствующей концентрации исследуемого вещества и интерпретации результатов, свидетельствующих о низкой способности к биоразложению, необходимы сведения о токсичности вещества для анаэробных бактерий. Рекомендуется также проводить контроль ингибирования, если только не известно, что исследуемое вещество не подавляет активность анаэробных микроорганизмов (см. 3.8 и [12]).
2.3 Применимость метода
Метод может использоваться для растворимых в воде химических веществ; он также может применяться для плохо растворимых и нерастворимых химических веществ, при условии, что используется метод точного дозирования, например по [13]. Как правило, для летучих веществ решение принимается индивидуально. Могут быть созданы специальные условия, например газ в течение испытания не выпускают.
2.4 Референтное (стандартное) вещество
Для проверки процедуры референтное вещество тестируют в параллельной пробе вместе с обычными тестовыми пробами. В качестве стандартных веществ могут использоваться фенол, бензоат натрия и полиэтиленгликоль 400, для которых ожидается биоразлагаемость более 60% от теоретического выделения газа (например, по метану и неорганическому углероду) в течение 60 дней по [3], [14].
2.5 Воспроизводимость результатов испытаний
2.5.1 В международном межлабораторном тесте [14] была показана хорошая воспроизводимость при измерении давления газа в трех параллельных пробах. Относительное стандартное отклонение (коэффициент вариации КВ), как правило, составляло менее 20%, хотя данное значение часто превышало 20% в присутствии токсичных химических веществ или ближе к концу 60-дневного инкубационного периода. Более значительные отклонения были также обнаружены в пробах объемом менее 150 мл. Окончательные значения рН тестовой среды находились в диапазоне от 6,5 до 7,0.
2.5.2 В межлабораторном тесте были получены следующие результаты.
Таблица 1 - Результаты воспроизводимости
Исследуемое вещество | Общие данные, | Среднее разло- | Относи- | Под- | Среднее разло- | Относи- | Данные по >60% разло- |
Пальмитиновая кислота | 36 | 68,7±30,7 | 45 | 27 | 72,2±18,8 | 26 | 19=70%* |
Полиэтиленгликоль 400 | 38 | 79,8±28,0 | 35 | 29 | 77,7±17,8 | 23 | 24=83%* |
* В пропорции от | |||||||
2.5.3 Коэффициенты вариации средних значений для всех величин, полученных для пальмитиновой кислоты и полиэтиленгликоля 400, достигали 45% (=36) и 35% (
=38) соответственно. Когда значения менее 40% и более 100% не учитывались (предполагается, что первое связано с неоптимальными условиями, последнее - по неизвестным причинам), КВ снизились до 26% и 23% соответственно. Соотношения "подтвержденных" величин разложения составляли не менее 60%. Разложения составляли 70% для пальмитиновой кислоты и 83% - для полиэтиленгликоля 400. Соотношения процента биоразложения, полученные из измерений растворенного неорганического углерода (далее - РНУ), были относительно низкими, но непостоянными. Для пальмитиновой кислоты они находились в диапазоне от 0% до 35%, среднее - 12%, КВ - 92%; полиэтиленгликоля 400 - от 0% до 40%, среднее - 24%, с КВ - 54%.
3 Описание метода
3.1 Оборудование
В испытании используют стандартное лабораторное оборудование, а также:
- инкубатор искробезопасный с возможностью поддержания температуры (35±2)°С;
- стеклянные тестовые сосуды, устойчивые к давлению, соответствующего номинального объема, каждый из которых снабжен герметичной газонепроницаемой мембраной, способной выдержать давление около 2 бар. Объем свободного пространства должен составлять от 10% до 30% от общего объема. Если биогаз регулярно выпускается, достаточно использовать 10% общего объема в качестве свободного пространства, но если выпуск газа проводится только в конце испытания, требуются 30%. Стеклянные сосуды номинального объема 125 мл, общего объема около 160 мл, рекомендуется закрывать мембраной
и алюминиевыми скобами, если давление выпускается во время каждого отбора проб;
________________
Рекомендуемый объем составляет от 0,1 до 1 л.
Рекомендуется использовать газонепроницаемые силиконовые мембраны. Кроме того, рекомендуется проверять герметичность крышек, особенно мембран из бутилкаучука, поскольку некоторые коммерчески доступные мембраны не являются достаточно непроницаемыми для метана, и некоторые мембраны теряют герметичность после прокола иглой в условиях испытания.
- прибор для измерения давления, адаптированный для измерения и выпуска в атмосферу образованного газа, например, ручной манометр подключают к подходящей игле шприца; трехканальный газонепроницаемый клапан облегчает высвобождение избыточного давления (приложение А). Необходимо сохранить внутренний объем трубки датчика давления и клапана на максимально низком уровне, чтобы ошибки за счет пренебрежения объемом оборудования были незначительными.
________________
Оборудование должно использоваться и калиброваться регулярно в соответствии с инструкциями производителя. Если используется манометр надлежащего качества, например капсулированный со стальной мембраной, калибровка в лаборатории не нужна. Точность калибровки можно проверить в лаборатории с помощью одноточечного измерения при 1·10
Па по сравнению с манометром с механической индикацией. Когда эта точка измеряется правильно, линейность также будет неизменной. Если используются другие измерительные устройства (без сертифицированной калибровки производителя), калибровку рекомендуется проводить для всего диапазона с регулярными интервалами.
Примечание 1 - Значения давления используют непосредственно для расчета количества образованного в свободном пространстве углерода (см. 4.1-4.3). Кроме того, значения давления могут быть преобразованы в объем (при температуре 35°С, атмосферном давлении) образованного газа с использованием графика перевода (калибровочной кривой). Этот график строят по данным, полученным путем введения известных объемов газообразного азота в серию тестовых сосудов при (35±2)°С и регистрирования полученных давлений (приложение Б).
Примечание 2 - Следует соблюдать осторожность и избегать уколов иглой при использовании микрошприцев;
- анализатор углерода, предназначенный для прямого определения неорганического углерода в диапазоне от 1 до 200 мг/л;
- шприцы высокой точности для отбора газообразных и жидких проб;
- магнитные мешалки (по выбору);
- перчаточная камера (рекомендуется).
3.2 Реагенты
Используют реагенты аналитической чистоты.
3.3 Вода
Используют дистиллированную или деионизированную воду (не содержащую кислород, полученную барботированием азотом, содержащим менее 5 мкл/л кислорода), с содержанием РОУ менее 2 мг/л.
3.4 Тестовая среда
3.4.1 Готовят среду для разбавления, содержащую следующие компоненты в установленном количестве:
- калия дигидрофосфат безводный ![]() : 0,27 г;
: 0,27 г;
- динатрия гидрофосфат додекагидрат ![]() : 1,12 г;
: 1,12 г;
- аммония хлорид ![]() : 0,53 г;
: 0,53 г;
- кальция хлорид дигидрат ![]() : 0,075 г;
: 0,075 г;
- магния хлорид гексагидрат ![]() : 0,10 г;
: 0,10 г;
- железа (II) хлорид тетрагидрата ![]() : 0,02 г;
: 0,02 г;
- резазурин (индикатор кислорода): 0,001 г;
- натрия сульфид наногидрат ![]() : 0,10 г;
: 0,10 г;
- основной раствор микроэлементов (по выбору, см. 3.5): 10 мл;
- довести водой, не содержащей кислород (см. 3.5), до 1 л.
Примечание - Для обеспечения необходимого восстановительного потенциала следует использовать свежеприготовленный сульфид натрия или промывать и высушивать его перед использованием.
Испытания могут проводиться без использования перчаточной камеры (см. 3.11). В этом случае конечная концентрация сернистого натрия в среде должна быть увеличена до 0,20 г ![]() на 1 л. Также через мембрану закрытых тестовых сосудов из соответствующего анаэробного основного раствора можно добавлять сульфид натрия, поскольку данная процедура снизит риск окисления. Сульфид натрия может быть заменен на цитрат титана (III), который добавляют через мембрану закрытых тестовых сосудов в конечной концентрации от 0,8 до 1,0 ммоль/л. Цитрат титана (III) является высокоэффективным и малотоксичным восстановительным агентом, который готовят следующим образом: растворяют 2,94 г дигидрата цитрата тринатрия в 50 мл воды, не содержащей кислород (в результате получают раствор 200 ммоль/л), и добавляют 5 мл 15 об.% раствора хлорида титана (III). Нейтрализуют до рН (7±0,2) раствором минеральной щелочи и переносят в подходящий сосуд в потоке азота. Концентрация цитрата титана (III) в данном основном растворе составляет 164 ммоль/л.
на 1 л. Также через мембрану закрытых тестовых сосудов из соответствующего анаэробного основного раствора можно добавлять сульфид натрия, поскольку данная процедура снизит риск окисления. Сульфид натрия может быть заменен на цитрат титана (III), который добавляют через мембрану закрытых тестовых сосудов в конечной концентрации от 0,8 до 1,0 ммоль/л. Цитрат титана (III) является высокоэффективным и малотоксичным восстановительным агентом, который готовят следующим образом: растворяют 2,94 г дигидрата цитрата тринатрия в 50 мл воды, не содержащей кислород (в результате получают раствор 200 ммоль/л), и добавляют 5 мл 15 об.% раствора хлорида титана (III). Нейтрализуют до рН (7±0,2) раствором минеральной щелочи и переносят в подходящий сосуд в потоке азота. Концентрация цитрата титана (III) в данном основном растворе составляет 164 ммоль/л.
3.4.2 Смешивают компоненты тестовой среды, за исключением восстановительного агента (сульфида натрия/цитрата титана), и барботируют раствор азотом в течение приблизительно 20 мин непосредственно перед использованием для удаления кислорода. Затем добавляют необходимый объем свежеприготовленного раствора восстановительного агента (в деоксидированной воде) непосредственно перед использованием среды. При необходимости приводят рН среды разбавленным раствором минеральной кислоты или щелочи к (7±0,2).
3.5 Основной раствор микроэлементов (по выбору)
Рекомендуется для улучшения процесса анаэробного разложения добавлять в тестовую среду следующие микроэлементы, особенно при использовании низких концентраций (например, 1 г/л) инокулята по [1]:
- марганца хлорид тетрагидрат ![]() : 50 м;
: 50 м;
- борную кислоту ![]() : 5 мг;
: 5 мг;
- цинка хлорид ![]() : 5 мг;
: 5 мг;
- меди (II) хлорид ![]() : 3 мг;
: 3 мг;
- динатрия молибдат дигидрат ![]() : 1 мг;
: 1 мг;
- кобальта хлорид гексагидрат ![]() : 100 мг;
: 100 мг;
- никеля хлорид гексагидрат ![]() : 10 мг;
: 10 мг;
- динатрия селенит ![]() : 5 мг.
: 5 мг.
Довести водой, не содержащей кислород (см. 3.3), до 1 л.
3.6 Исследуемое вещество
Добавляют исследуемое вещество в виде основного раствора, суспензии, эмульсии или непосредственно в твердом или жидком виде или в абсорбированном на фильтре из стекловолокна для обеспечения концентрации органического углерода не более 100 мг/л. Если используют основные растворы, готовят соответствующий водный раствор (см. 3.5) (в деоксидированной воде) такой крепости, чтобы добавленный объем составлял менее 5% от общего объема реакционной смеси. Приводят рН основного раствора к (7±0,2), если это необходимо. Для исследуемых веществ, которые плохо растворимы в воде, см. [13]. Если используется растворитель, готовят дополнительную контрольную пробу с растворителем - в инокулированную среду добавляют только растворитель. Следует избегать использования органических растворителей, которые ингибируют образование метана, таких как хлороформ и тетрахлорид углерода.
Примечание - При работе с токсичными тестируемыми веществами или теми, чьи свойства неизвестны, следует соблюдать осторожность.
3.7 Референтные вещества
Референтные вещества, такие как бензоат натрия, фенол и полиэтиленгликоль 400, успешно применяются для проверки процедуры и демонстрируют более, чем 60% разложения в течение 60 дней. Готовят основной раствор (в деоксидированной воде) выбранного референтного вещества так же, как и для исследуемого вещества, и приводят рН к (7±0,2), если это необходимо.
3.8 Контроль ингибирования (при необходимости)
Для получения информации о токсичности исследуемого вещества для анаэробных микроорганизмов и подбора наиболее подходящей тестовой концентрации добавляют исследуемое и стандартное вещества в сосуды с тестовой средой (см. 3.4.1), каждое в установленной ранее концентрации соответственно (см. 3.6 и 3.7 и [12]).
3.9 Сброженный осадок
3.9.1 Сброженный осадок отбирают из реактора очистных сооружений, предназначенных преимущественно для очистки бытовых сточных вод. Свойства осадка должны быть полностью изучены, справочная информация должна быть представлена (см. 4.9). Если планируется использовать адаптированную посевную культуру, можно использовать сброженный осадок из промышленной установки очистки сточных вод. Для сбора осадка используют сосуды с широким горлом из полиэтилена высокой плотности или подобного материала, который может расширяться. Добавляют осадок примерно на 1 см горлышка и плотно закрывают, желательно с предохранительным клапаном. После транспортирования в лабораторию, собранный осадок может использоваться непосредственно или помещаться в лабораторную установку. Из сосудов с осадком очень аккуратно выпускают биогаз. Кроме того, полученный в лаборатории анаэробный осадок может использоваться в качестве источника посевной культуры, но его спектр активности, возможно, может быть нарушен.
Примечание - Сброженный осадок выделяет горючие газы, которые обладают пожаро- и взрывоопасностью; он также содержит потенциально патогенные организмы, поэтому следует принимать надлежащие меры предосторожности при работе с осадком. Из соображений безопасности для сбора осадка не используют стеклянные сосуды.
3.9.2 Для снижения образования газа и влияния контрольных проб может проводиться предварительное сбраживание осадка. Если предварительное сбраживание необходимо, осадок подвергают брожению без добавления каких-либо питательных веществ или субстрата при температуре (35±2)°С в течение семи дней. Было установлено, что предварительное сбраживание в течение примерно пяти дней, как правило, дает оптимальное снижение образования газа в контрольных пробах без неприемлемого увеличения лаг-фазы или инкубационного периода во время теста или потери активности по отношению к некоторым исследуемым веществам.
3.9.3 Для исследования веществ, которые плохо или предположительно плохо поддаются биологическому разложению, может проводиться предварительное испытание по воздействию осадка на исследуемое вещество для получения наиболее адаптированной посевной культуры. В таком случае добавляют исследуемое вещество в концентрации (в расчете на органический углерод) от 5 до 20 мг/л сброженного осадка и инкубируют в течение двух недель. Перед использованием осадок для предварительного испытания тщательно промывают (см. 3.10). В протоколе испытаний указывают условия предварительного испытания.
3.10 Инокулюм (прививочный материал)
Осадок промывают (см. 3.9) непосредственно перед использованием, чтобы уменьшить концентрацию НУ до значения менее 10 мг/л в конечной суспензии. Затем центрифугируют в герметичных тубах (например, 3000 г в течение 5 мин) и сливают надосадочную жидкость. Суспендируют полученный осадок в деоксидированной среде (см. 3.4), повторно центрифугируют суспензию и сливают супернатант. Если количество НУ не было достаточно снижено, процедура промывки осадка может проводиться еще не более двух раз. Эта процедура не оказывает отрицательного влияния на микроорганизмы. В заключение, суспендируют осадок в необходимом для тестовой среды объеме и определяют общую концентрацию сухого остатка (например, см. [15]). Конечное общее содержание сухого остатка в тестовых сосудах должно быть в диапазоне от 1 до 3 г/л (или около 10% от содержания в неразбавленном осадке). Указанные операции проводят таким образом, чтобы осадок имел минимальный контакт с кислородом (например, использование атмосферы азота).
3.11 Порядок проведения испытания
Выполняют следующие начальные процедуры с использованием техник для сохранения минимального контакта между сброженным осадком и кислородом, например, может быть необходимо использовать для работы перчаточную камеру с атмосферой азота и/или обработку сосудов азотом (см. [4]).
3.12 Подготовка тестовых и контрольных проб
3.12.1 Готовят, как минимум, три экземпляра тестовых сосудов (см. 3.1) для исследуемого вещества, контрольной пробы, референтного вещества, контроля ингибирования (по выбору) и контроля давления в камерах (процедура по выбору) (см. 2.2, 2.6 и 3.7). Могут быть также подготовлены дополнительные сосуды с целью оценки первичной биоразлагаемости с использованием специальных анализов исследуемого вещества. Тот же набор контрольных проб может использоваться для нескольких исследуемых веществ в одном и том же испытании до тех пор, пока объем незаполненного пространства остается постоянным.
3.12.2 Готовят разбавленную посевную культуру, например, с помощью пипетки с широким горлом. Добавляют аликвоты хорошо перемешанной посевной культуры (см. 3.10) так, что общая концентрация взвешенных веществ одинакова во всех сосудах (от 1 до 3 г/л). Добавляют основные растворы исследуемого и стандартного веществ после корректировки рН до (7±0,2), при необходимости. Исследуемое и стандартное вещества должны быть добавлены наиболее подходящим способом (см. 3.6).
3.12.3 Тестовая концентрация органического углерода, как правило, должна составлять от 20 до 100 мг/л (см. 3.1). Если исследуемое вещество является токсичным, тестовая концентрация должна быть снижена до 20 мг углерода на литр или даже меньше, если должна быть оценена только начальная биоразлагаемость с помощью конкретных анализов. Следует отметить, что изменчивость результатов испытаний увеличивается при более низких тестовых концентрациях.
3.12.4 Для холостых проб вместо исходного раствора, суспензии или эмульсии добавляют шприцем эквивалентное количество исследуемого вещества. Если исследуемое вещество вводили с использованием фильтров из стекловолокна или органических растворителей, добавляют в пробы фильтр или эквивалентный объем растворителя, который испаряют. Готовят дополнительную пробу с исследуемым веществом для измерения рН. При необходимости, приводят рН к (7±0,2) небольшим количеством разбавленной минеральной кислоты или щелочи. Такие же количества нейтрализующих агентов необходимо добавить во все тестовые сосуды. Нейтрализующие агенты не добавляют, если рН основных растворов исследуемого и референтного веществ уже были приведены к нужному значению (см. 3.6 и 3.7). При оценке начальной биоразлагаемости соответствующие пробы отбирают из сосудов для контроля рН или из дополнительного тестового сосуда и измеряют концентрацию исследуемого вещества с помощью специальных анализов. Магнитные мешалки могут быть добавлены во все сосуды, если реакционную смесь необходимо перемешивать (не обязательно).
3.12.5 Общий объем жидкости и объем свободного пространства
, которые должны быть одинаковы во всех сосудах, измеряют и регистрируют их значения. Каждый сосуд должен быть закрыт мембраной и перенесен из перчаточной камеры (см. 3.12) в инкубатор (см. 3.1.1).
3.13 Нерастворимые тестируемые вещества
Взвешенные количества плохо растворимых в воде веществ переносят непосредственно в подготовленные сосуды. Когда необходимо использование растворителей (см. 3.6), переносят раствор или суспензию исследуемого вещества в пустые сосуды. Если возможно, растворитель испаряют, пропуская газообразный азот через сосуды, а затем добавляют другие ингредиенты, в том числе, разбавленный осадок (см. 3.10) и деоксидированную воду при необходимости. Также готовят дополнительную контрольную пробу с растворителем (см. 3.6). Для других способов добавления нерастворимых веществ см. [13]. Жидкие исследуемые вещества можно добавлять с помощью шприца в полностью подготовленные закупоренные сосуды, если предполагается, что начальное значение рН не превышает (7±1), в противном случае, вещество дозируют, как описано выше (см. 3.6).
3.14 Инкубация и измерения давления газа
3.14.1 Подготовленные сосуды инкубируют при (35±2)°С в течение одного часа для достижения равновесия и выпускают избыток газа в атмосферу, например, встряхивая по очереди каждый сосуд со вставленной через мембрану иглой манометра (см. 3.1.3) и открывая клапан, пока показания манометра не установятся на нуле. Если на этой стадии или при выполнении промежуточных измерений давление газовой фазы меньше атмосферного, для восстановления атмосферного давления должен быть введен азот. Закрывают клапан (см. 3.1.3) и продолжают инкубировать в темноте, обеспечивая поддержание температуры сбраживания для всех частей сосуда. По прошествии от 24 до 48 ч после инкубации сосуды обследуют. Сосуды исключают, если их содержимое имеет выраженное розовое окрашивание надосадочной жидкости, т.е. если резазурин (см. 3.4.1) изменил цвет, что указывает на присутствие кислорода (см. 4.7). Хотя система может быть толерантна к небольшому количеству кислорода, более высокие концентрации могут серьезно тормозить ход анаэробного биоразложения. Исключение одного случайного сосуда из набора из трех образцов может быть принято, но в случае появления большего количества ошибок необходимо пересмотреть экспериментальные процедуры и повторить эксперимент.
3.14.2 Содержимое каждого сосуда тщательно перемешивают с помощью мешалки или встряхиванием в течение нескольких минут как минимум два или три раза в неделю и незадолго перед каждым измерением давления. Встряхивание повторно суспендирует инокулят и способствует поддержанию газового равновесия. Все измерения давления должны проводиться быстро, поскольку это может привести к снижению температуры тестовых сосудов, что в свою очередь приводит к получению ошибочных результатов. При измерении давления для всего тестового сосуда, включая свободное пространство, необходимо поддерживать температуру сбраживания. Давление газа измеряют, например, путем введения через мембрану иглы шприца (см. 3.1), соединенной с манометром. Необходимо следить, чтобы на иглу шприца не попала вода, если это происходит, мокрые части необходимо высушить и установить новую иглу. Давление измеряется в миллибарах (см. 4.1). Давление газа в сосудах можно измерять периодически, например раз в неделю и при необходимости выпускать избыток газа. В альтернативном случае, давление измеряется только в конце испытания для определения количества образованного биогаза.
3.14.3 Рекомендуется проводить промежуточные измерения давления газа, поскольку повышение давления свидетельствует о возможности окончания испытания и позволяет проследить кинетику процесса (см. 3.1).
3.14.4 В общем случае, испытание заканчивают после инкубационного периода в 60 дней, если кривая биоразложения, полученная на основании измерений давления, не достигает плато-фазы ранее; то есть фазы, в которой максимальное разложение было достигнуто и кривая биоразложения выходит на постоянный уровень. Если значение плато меньше 60%, интерпретация является затруднительной, поскольку это означает, что только часть молекул была минерализована или произошла ошибка. Если по окончании стандартного инкубационного периода, газ образуется, но фаза плато, очевидно, не достигнута, необходимо рассмотреть возможность продления испытания до достижения плато (более 60%).
3.15 Измерение неорганического углерода
3.15.1 По окончании испытания после последнего измерения давления газа осадку дают осесть. Каждый сосуд по очереди открывают и немедленно отбирают пробу для определения концентрации (мг/л) НУ в надосадочной жидкости. Надосадочную жидкость не центрифугируют и не фильтруют, поскольку это приведет к неприемлемой потере растворенного углекислого газа. Если невозможно провести анализ надосадочной жидкости, ее хранят в герметичной емкости без свободного пространства и охлажденной до 4°С не более двух дней. После измерения НУ измеряют и регистрируют значение рН.
3.15.2 В альтернативном случае НУ в надосадочной жидкости может быть определен косвенно путем растворения НУ в углекислый газ, который может быть измерен в свободном пространстве. После последнего измерения давления газа каждый из тестовых сосудов приводят к атмосферному давлению. Подкисляют содержимое каждого сосуда до рН=1 путем через мембрану добавления концентрированной минеральной кислоты (например, ![]() ). Сосуды встряхивают и инкубируют при (35±2)°С в течение примерно 24 ч и измеряют давление полученного углекислого газа с помощью манометра.
). Сосуды встряхивают и инкубируют при (35±2)°С в течение примерно 24 ч и измеряют давление полученного углекислого газа с помощью манометра.
3.15.3 Аналогичные измерения проводят для соответствующих контрольных проб, проб с референтным веществом и, если используются, проб с контролем ингибирования (см. 3.8).
3.15.4 В некоторых случаях, особенно если одни и те же контрольные сосуды используются для нескольких исследуемых веществ, измерения промежуточных концентраций НУ в тестовых и контрольных сосудах должны быть рассмотрены. В этом случае достаточное количество флаконов должно быть подготовлено для всех промежуточных измерений. Такая подготовка более предпочтительна, чем отбор всех проб только из одного сосуда. Последнее может быть сделано только, если необходимый для анализа объем растворенного органического углерода (далее РОУ) не будет слишком большим. Измерения РОУ должны быть сделаны после измерения давления газа без выпуска избытка газа, как описано ниже:
- с помощью шприца через мембрану без открытия сосуда отбирают как можно меньшую пробу поверхностной жидкости и определяют в ней содержание НУ;
- после отбора пробы избыток газа выпускают или не выпускают;
- необходимо принять во внимание, что даже небольшое снижение объема поверхностной жидкости (например, около 1%) может привести к значительному увеличению объема свободного пространства газа ();
- формулы (см. 4.2.2) при необходимости корректируют при увеличении в формуле (3).
3.16 Специальные анализы
Если необходимо измерить первичное анаэробное разложение (см. 3.12), отбирают соответствующий объем пробы для специального анализа в начале и в конце испытания из сосуда, содержащего исследуемое вещество. Если это было сделано, принимают во внимание, что и
изменились, и их учитывают при расчете результатов образования газа. Альтернативные пробы могут быть отобраны для конкретных анализов из дополнительных исследуемых смесей, ранее подготовленных для этой цели (см. 3.12.4).
4. Данные и отчет о проведении испытания
4.1 Обработка результатов
Из практических соображений давление газа измеряют в миллибарах (1 мбар =102 Па; 1 Па =1 Н/м), объем - в литрах, температуру - в градусах по Цельсию.
4.2 Углерод в свободном пространстве
4.2.1 1 моль метана и 1 моль углекислого газа каждый содержат по 12 г углерода, массу углерода в данном объеме образовавшегося газа , мг, вычисляют по формуле:
![]() , (1)
, (1)
где - относительная атомная масса углерода;
- число молей газа в данном объеме.
Если помимо метана или углекислого газа в значительных количествах образуется какой-либо другой газ (например, ), в формуле (1) следует внести поправки для описания возможности влияния образующихся газов.
4.2.2 Из законов идеального газа рассчитывают по следующей формуле:
![]() , (2)
, (2)
где - давление газа, Па;
- объем газа, м
;
- газовая постоянная, равная 8,314 Дж/(моль·К);
- температура инкубации, К.
Из комбинации формул (1) и (2) и оптимизации для образования газа в пустых контрольных пробах массу чистого углерода, образованного в виде газа в свободном пространстве , мг, вычисляют по формуле
![]() , (3)
, (3)
где - средняя разница между начальным и конечным давлениями в тестовых сосудах минус соответствующее среднее значение в контрольных сосудах, мбар;
- объем свободного пространства в сосуде, л;
- коэффициент перевода для Н/м
в мбар и м
в л.
Формула (4) используется для нормальной температуры инкубации, равной 35°С (308 К)
![]() . (4)
. (4)
Примечание - Расчет альтернативного объема: показания манометра преобразуют в мл образованного газа с использованием стандартного графика, полученного путем построения графика зависимости добавляемого объема (мл) от показаний манометра (приложение Б).
Число молей () газа в свободном пространстве каждого сосуда вычисляется путем деления общего объема полученного газа (мл) на 25286 мл/моль - объем, занимаемый одним молем газа при температуре 35°С и стандартном атмосферном давлении. 1 моль
и 1 моль
каждый содержат по 12 г углерода, количество углерода (
, мг) в свободном пространстве (
) вычисляют по формуле
![]() . (5)
. (5)
Преобразование для вычисления образования газа в контрольных сосудах
![]() , (6)
, (6)
где - масса чистого углерода, образованного в виде газа в свободном пространстве, мг;
- средняя разница между объемом газа, образованного в свободном пространстве тестового сосуда и контрольных сосудов;
![]() - объем, занимаемый 1 моль газа при температуре 35°С, 0,1 МПа.
- объем, занимаемый 1 моль газа при температуре 35°С, 0,1 МПа.
4.2.3 Ход биоразложения можно проследить путем построения зависимости зарегистрированных значений повышения давления (мбар) от времени при необходимости. На данной кривой выявляют и регистрируют лаг-фазу (дни). Лаг-фаза - это время от начала испытания до начала значительного разложения (например, приложение В). Если промежуточные пробы поверхностной жидкости были отобраны и проанализированы (см. 4.15, 4.3 и 4.4), то общее количество образованного углерода (в газе и жидкости) может быть построено только в зависимости от совокупного давления.
4.3 Углерод в жидкой фазе
Количество метана в жидкой фазе не учитывается, поскольку его растворимость в воде, как известно, очень мала. Массу неорганического углерода в жидкой фазе тестовых сосудов , мг, вычисляют по формуле (7)
![]() , (7)
, (7)
где - концентрация неорганического углерода в тестовых сосудах минус концентрация неорганического углерода в контрольных сосудах в конце испытания, мг/л;
- объем жидкости в сосуде, л.
4.4 Общий газообразный углерод
Общую массу газообразного углерода в сосуде , мг, вычисляют по формуле
![]() , (8)
, (8)
где и
вычислены по формулам (6) и (7).
4.5 Углерод исследуемого вещества
Массу углерода, образованного из добавленного исследуемого вещества , мг, вычисляют по формуле
![]() , (9)
, (9)
где - концентрация углерода исследуемого вещества в тестовом сосуде, мг/л;
- объем жидкости в тестовом сосуде, л.
4.6 Степень биоразложения
Процент биоразложения , %, и общий процент биоразложения
, %, рассчитывают по формулам (10) и (11) соответственно:
 , (10)
, (10)
 , (11)
, (11)
где ,
и
определены по формулам (5), (6), (9), (7).
Степень основного биоразложения , %, вычисляют (по выбору), исходя из измерений концентрации исследуемого вещества в начале и в конце периода инкубации, по формуле (12)
 , (12)
, (12)
где - начальная концентрация исследуемого вещества, мг/л;
- концентрация исследуемого вещества в конце испытания, мг/л.
Если метод анализа указывает на значительные концентрации исследуемого вещества в неизменной анаэробной посевной культуре, то скорректированное основное разложение исследуемого вещества , %, вычисляют по формуле (13)
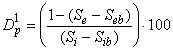 , (13)
, (13)
где - начальная "очевидная" концентрация исследуемого вещества в контрольных пробах, мг/л;
- "очевидная" концентрация исследуемого вещества в контрольных пробах в конце испытания, мг/л.
4.7 Достоверность результатов
4.7.1 Показания давления используют только для сосудов, которые не имеют розовой окраски (см. 4.14). Загрязнение кислородом минимизируется за счет использования соответствующих анаэробных методов обработки.
4.7.2 Следует учитывать, что испытание считается действительным, если стандартное вещество достигает плато, составляющее более 60% биоразложения.
________________
Должно быть пересмотрено, если используются адсорбирующиеся и нерастворимые стандартные вещества.
4.7.3 Если рН в конце испытаний превышает диапазон (7±1) и происходит недостаточное биоразложение, испытание повторяют с повышенной буферной емкостью среды.
4.8 Ингибирование разложения
Образование газа в сосудах, содержащего исследуемое и референтное вещества, должно быть как минимум равно находящемуся в сосудах, содержащих только референтное вещество; в ином случае наблюдается ингибирование образования газа. В некоторых случаях образование газа в сосудах, содержащих исследуемое вещество без референтного вещества, будет ниже, чем в контрольной пробе. Это означает, что исследуемое вещество является ингибитором.
4.9 Отчет о проведении испытания
Отчет о проведении испытания должен включать следующую информацию.
Исследуемое вещество:
- общее наименование, химическое наименование, номер CAS, структурная формула и соответствующие физико-химические свойства;
- чистота (примеси) исследуемого вещества.
Условия испытания:
- объемы разбавленного сброженного осадка () и свободного пространства (
) в сосуде;
- описание тестовых сосудов, основные характеристики измерений биогаза (например, тип манометра), а также анализатора НУ;
- использование исследуемого и стандартного веществ в тестовой системе: используемая концентрация и любое применение растворителей;
- подробная информация об используемой посевной культуре: очистные сооружения, описание источника сточных вод, подвергающихся очистке (например, температура, время удержания осадка, происхождение и др.), концентрация, любая информация, необходимая для обоснования, и информация о любой предварительной обработке посевной культуры (например, предварительное сбраживание, предварительная экспозиция исследуемого вещества);
- температура инкубации;
- количество параллельных проб.
Результаты:
- значения рН и НУ в конце испытания;
- концентрация исследуемого вещества в начале и в конце испытания, если выполнялись конкретные измерения;
- все измеренные данные для тестовых, контрольных проб, проб с референтным веществом и, при необходимости, контролем ингибирования (например, давление в мбар, концентрация неорганического углерода (мг/л)) в табличной форме (данные измерений для газовой и жидкой фаз следует указывать отдельно);
- статистическая обработка данных, продолжительность испытания и ход биоразложения исследуемого вещества, стандартного вещества и контроля токсичности в графической форме;
- процент биоразложения исследуемого и стандартного веществ;
- основания для любого исключения результатов испытаний;
- обсуждение результатов.
Приложение А
(справочное)
Пример оборудования для измерения образования биогаза по давлению газа
|
Рисунок А.1 - Тестовые сосуды при температуре (35±2)°С
Приложение Б
(рекомендуемое)
Преобразование показателей манометра
Показания манометра могут быть переведены в объемы газа с помощью калибровочной кривой, полученной введением известных объемов воздуха при (35±2)°С в сосуды, содержащие объемы воды, равные объемам реакционной смеси , для чего:
- вносят аликвоту воды , мл, выдержанной при (35±2)°С, в пять сосудов. Сосуды закупоривают и помещают в водяную баню при температуре 35°С на 1 ч для достижения равновесия;
- включают манометр, позволяют стабилизироваться и приводят к нулевому значению;
- вставляют иглу шприца через мембрану одного из сосудов, открывают клапан до тех пор, пока манометр не покажет нулевое значение, и закрывают клапан;
- повторяют процедуру с оставшимися сосудами;
- вводят 1 мл воздуха при (35±2)°С в каждый сосуд. Вставляют иглу через мембрану одного из сосудов и позволяют показаниям давления стабилизироваться. Регистрируют давление, открывают клапан, пока давление не придет к нулевому значению, а затем закрывают клапан;
- повторяют процедуру для оставшихся сосудов;
- повторяют всю процедуру с использованием 2, 3, 4, 5, 6, 8, 10, 12, 16, 20 и 50 мл воздуха;
- строят калибровочный график зависимости давления (Па) от добавленного объема газа (мл). Показания прибора линейны в диапазоне от 0 до 70000 Па и от 0 до 50 мл образованного газа.
Приложение В
(справочное)
Пример кривой биоразложения (увеличение общего давления)
|
Рисунок В.1 - Пример кривой биоразложения
Приложение Г
(справочное)
Пример отчета об испытании анаэробного биоразложения - данные для исследуемого вещества
Лаборатория: | Исследуемое вещество: | N испытания: |
Температура испытания, °С: | Объем свободного пространства, | Объем жидкой фазы, |
Содержание углерода в исследуемом веществе |
|
Таблица Г.1
День |
|
|
|
|
|
|
|
|
|
|
|
|
НУ |
|
|
|
|
|
|
|
|
|
|
|
|
рН | ||||||||||||
| ||||||||||||
Приложение Д
(справочное)
Пример отчета об испытании анаэробного биоразложения - данные для стандартного вещества
Лаборатория: | Стандартное вещество: | N испытания: |
Температура испытания, °С: | Объем свободного пространства, | Объем жидкой фазы, |
Содержание углерода в исследуемом веществе, |
|
Таблица Д.1
День |
|
|
|
|
|
|
|
|
|
|
|
|
НУ |
|
|
|
|
|
|
|
|
|
|
|
|
рН | ||||||||||||
| ||||||||||||
Библиография
[1] | OECD Guidelines for the Testing of Chemicals (1981). 302A-C: Inherent Biodegradability and 303A-B: Simulation Test - Aerobic Sewage Treatment Organization for Economic Cooperation Development, Paris |
[2] | OECD Guideline for the Testing of Chemicals (1992). Ready Biodegradability 301 (A-F) and Inherent Biodegradability: Zahn-Wellens/EMPATest 302B, Organization for Economic Cooperation and Development, Paris |
[3] | Birch R. R., Biver C, Campagna R., Gledhill W.E., Pagga U., SteberJ., Reust H. and Bontinck(1989) W.J. Screening of chemicals for anaerobic biodegradation. Chemosphere 19, 1527-1550. (Also published as ECETOC Technical Report No. 28, June 1988) |
[4] | Shelton D.R. and Tiedje J.M. (1984) General method for determining anaerobic biodegradation potential. Appl. Environ. Mircobiology, 47, 850-857 |
[5] | Owen W.F., Stuckey D.C., Healy J.B. Jr., Young L.Y. and McCarty PL. (1979) Bioassay for monitoring biochemical methane potential and anaerobic toxicity. Water Res. 13, 485-492 |
[6] | Healy J.B. Jr. and Young L.Y. (1979) Anaerobic biodegradation of eleven aromatic compounds to methane. Appl. Environ. Microbiol. 38, 84-89 |
[7] | Gledhill W.E. (1979) Proposed standard practice forthe determination of the anaerobic biodegradation of organic chemicals. Working document. Draft 2 no.35.24. American Society for Testing Materials, Philadelphia |
[8] | Battersby N.S. and Wilson V. (1988) Evaluation of a serum bottle technique for assessing the anaerobic biodegradability of organic chemicals under methanogenic conditions. Chemosphere, 17, 2441-2460 |
[9] | E1192-92. Standard Test Method for Determining the Anaerobic Biodegradation Potential of Organic Chemicals. ASTM, Philadelphia |
[10] | US-EPA (1998) Fate, Transport and Transformation Test Guidelines OPPTS 835.3400 Anaerobic Biodegradability of Organic Chemicals |
[11] | International Organization for Standardization (1995) ISO 11 734 Water Quality - Evaluation of the ultimate anaerobic biodegradation of organic compounds in digested sludge - Method by measurement of the biogas production |
[12] | International Organization for Standardization (2003) ISO 13 641-1 Water Quality - Determination of inhibition of gas production of anaerobic bacteria - Part 1: General Test |
[13] | International Organization for Standardization (1995) ISO 10 634 Water Quality - Guidance for the preparation and treatment of poorly water-soluble organic compounds forthe subsequent evaluation of their biodegradability in an aqueous medium |
[14] | Pagga U. and Beimborn D.B. (1993) Anaerobic biodegradation test for organic compounds. Chemosphere, 27, 1499-1509 |
[15] | International Organization for Standardization (1997) ISO 11 923 Water Quality - Determination of suspended solids by filtration through glass-fibre filters |
[16] | NF T 20-043 AFNOR (1985). Chemical products for industrial use - Determination of partition coefficient - Shake flask method 40 CFR, 796.1550, Office of the Federal Register (1989) |
[17] | Jubermann O. (1958) in Houben-Weyl, Methoden der Organischen Chemie, Band I/1, 223-339, Georg Thieme Verlag, Stuttgart |
УДК 658.382.3:006.354 | МКС 71.040.50 | |
Ключевые слова: химическая продукция, окружающая среда, биоразлагаемость, органические соединения, сточные воды, анаэробные условия | ||
Электронный текст документа
и сверен по:
, 2019


