ГОСТ 32432-2013
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Аэробные и анаэробные трансформации в донных отложениях
Test methods for chemicals of environmental hazard. Aerobic and anaerobic transformation in aquatic sediment systems
МКС 71.040.50
Дата введения 2014-08-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием "Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ" (ФГУП "ВНИЦСМВ") на основе собственного перевода на русский язык англоязычной версии документа, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 5 ноября 2013 г. N 61-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Армения | AM | Минэкономики Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Киргизия | KG | Кыргызстандарт |
Молдова | MD | Молдова-Стандарт |
Россия | RU | Росстандарт |
Таджикистан | TJ | Таджикстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 ноября 2013 г. N 788-ст межгосударственный стандарт ГОСТ 32432-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 августа 2014 г.
5 Настоящий стандарт идентичен международному документу OECD Test No 308:2002* "Аэробные и анаэробные трансформации в донных отложениях" ("Aerobic and Anaerobic Transformation in Aquatic Sediment Systems", IDT).
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
Наименование настоящего стандарта изменено относительно наименования указанного международного документа для приведения в соответствие с ГОСТ 1.5 (подраздел 3.6)
6 ВВЕДЕН ВПЕРВЫЕ
7 ПЕРЕИЗДАНИЕ. Май 2019 г.
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
Введение
Химические вещества могут попадать в мелкие или глубокие поверхностные воды многими способами: в результате непосредственного применения веществ в воде, их сноса при опрыскивании, смыва поверхности, слива, ликвидации отходов, сброса промышленных, бытовых и сельскохозяйственных стоков. В данном стандарте описаны методы лабораторных испытаний для оценки аэробной и анаэробной трансформации органических химических веществ в системах водных отложений. Стандарт создан на основе существующих Руководств OECD [1-6]. На заседании рабочей группы ОЕСD по отбору Почвы/Отложений, проведенном в Белжирате, Италия, в 1995 г. [7], было принято решение, в частности, о количестве и типах отложений для испытаний такого вида. Группой также были составлены рекомендации относительно отбора, обращения и хранения образцов отложений, на основе [8]. Такие исследования необходимы для химических веществ, которые непосредственно применяются в воде или которые с большой долей вероятности могут попасть в водную среду вышеуказанными способами. Часто в природных системах "донные отложения - вода" условия в верхней водной фазе являются анаэробными. В поверхностном слое отложений могут быть как аэробные, так и анаэробные условия, при этом в более глубоких слоях отложений среда анаэробная. Для того чтобы учесть все возможные варианты разложения, в настоящем стандарте приводится описание как аэробного, так и анаэробного разложения. Тест на аэробное разложение моделирует аэробную водную колонну и верхний аэробный слой отложений, лежащий на толще, характеризующейся анаэробным градиентом. Анаэробный тест моделирует полностью анаэробную систему. В случае если есть указания на то, что следует использовать отличные условия от рекомендуемых, например применять интактные пробы осадков или отложения, которые могли уже подвергаться воздействию исследуемого вещества, можно использовать другие методики, разработанные для этих целей [9].
1 Область применения
Данный стандарт устанавливает метод лабораторного исследования аэробного и анаэробного разложения органических веществ в системах "вода - донные осадки".
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 время удаления 50% : Время, за которое изначальная концентрация вещества упадет на 50%.
2.2 время удаления 75% : Время, за которое изначальная концентрация вещества упадет на 75%.
2.3 время удаления 90% : Время, за которое изначальная концентрация вещества упадет на 90%.
2.4 анаэробное разложение (восстановление): Реакция, протекающая без молекулярного кислорода.
2.5 аэробное разложение (окисление): Реакция, протекающая в присутствии молекулярного кислорода.
2.6 исследуемое вещество: Любое вещество, исходное или соответствующие продукты разложения.
2.7 минерализация: Полное разложение органических соединений до углекислого газа и воды при аэробных условиях, и до метана, углекислого газа и воды - при анаэробных условиях. При использовании радиоактивно меченного вещества минерализацией является полным разложением молекулы, во время которого меченый атом углерода восстанавливается или окисляется с образованием соответствующего количества ![]() или
или ![]() соответственно.
соответственно.
2.8 отложения: Смесь неорганических и органических химических компонентов, последние обладают высокой молекулярной массой и характеризуются высоким содержанием углерода и азота. Они осаждаются из природных вод и являются границей раздела с водой.
2.9 период полуразложения (): Время, необходимое для разложения 50% исследуемого вещества, в случае, если реакция может быть описана кинетикой первого порядка, т.е. не зависима от концентрации вещества.
2.10 природные воды: Поверхностные воды, полученные из озер, рек и др.
2.11 продукты разложения: Все вещества, образующиеся в результате биотических или абиотических трансформаций исследуемого вещества, включая углекислый газ или связанные остатки.
2.12 связанные остатки: Представляют собой соединения в почвах, животных или растениях, которые удерживаются в матрице после экстракции в форме исходного вещества или его метаболитов. Метод выделения не должен существенно влиять на соединения или структуру матрицы. Характер связи в матрице может быть уточнен, применяя методы извлечения и сложные аналитические методы. На сегодняшний день, например, ионные и ковалентные связи, так же как и захват, были определены таким образом. В общем, образование связанных остатков снижает значительно биодоступность и биоаккумулирование.
3 Общие положения
3.1 Принцип метода
3.1.1 В рамках используемых аэробных и анаэробных систем (приложение A) "донные отложения - вода" с помощью описываемого метода возможно:
- определить скорость разложения исследуемого вещества в системах "донные отложения - вода";
- определить скорость разложения исследуемого вещества в донных отложениях;
- определить скорость минерализации исследуемого вещества и/или разложения его продуктов (при использовании исследуемого вещества, меченного );
- идентифицировать и количественно охарактеризовать продукты разложения в воде и донных отложениях, включая определение баланса масс (если использовалось радиоактивно меченное вещество);
- исследовать распределение исследуемого вещества и продуктов его разложения между двумя фазами (вода - донные отложения) в период инкубации в темноте (во избежание, например, цветения воды) при постоянной температуре.
3.1.2 Периоды полуразложения, значения ,
и
могут быть определены на основании данных, но не должны экстраполироваться далеко в прошлое до проведения эксперимента.
3.1.3 Должны использоваться два различных вида отложений с соответствующими водами, как для аэробных, так для анаэробных исследований. Возможны случаи, когда необходимо использование большего количества видов осадков, например в случаях, когда химическое вещество может присутствовать как в пресных, так и/или в морских экосистемах.
3.2 Применимость метода
3.2.1 Данный метод применим к химическим веществам (радиоактивно меченным или немеченным), для анализа которых был разработан достаточно точный и чувствительный аналитический метод. Он применим к нелетучим, малолетучим веществам, а также к водорастворимым или слаборастворимым в воде веществам. Метод нельзя использовать для анализа веществ с высокой летучестью из водных растворов (например, фумигантов, органических растворителей), т.к. нельзя обеспечить наличие вещества в воде/отложениях при заданных экспериментальных условиях.
3.2.2 Данный метод ранее применялся для изучения разложения веществ в пресной воде и отложениях, но также может использоваться для исследования поведения вещества в эстуарных/морских системах. Он не подходит для моделирования условий в проточной воде (например, реках) или открытом море.
3.3 Информация об исследуемом веществе
3.3.1 При определении скорости разложения вещества может использоваться радиоактивно меченное или немеченное вещество. Предпочтение отдают меченому материалу для исследования каскада реакций разложения и для расчета баланса вещества. Рекомендуется вводить изотопы С, но возможно использование и других изотопов, таких как
,
,
. Насколько это является возможным, метку следует вводить в наиболее стабильную часть(и) молекулы
. Химическая и/или радиохимическая чистота исследуемого вещества должна быть не ниже 95%.
________________
Например, если в структуре вещества содержится одно кольцо, то необходимо ввести метку в это кольцо; если же в структуре вещества два или более колец, должны проводиться отдельные исследования для определения судьбы каждого меченого кольца и получения достаточной информации об образовании продуктов разложения.
3.3.2 До проведения исследования должна быть известна следующая информация:
- растворимость в воде [10];
- растворимость в органических растворителях;
- давление паров [10] и/или константа закона Генри;
- коэффициент разделения н-октанол/вода [10];
- коэффициенты адсорбции (,
и
, где необходимо) (10);
- гидролиз [10];
- константа диссоциации () [10];
- химическая структура вещества и места ввода радиоактивной метки, если применимо.
Примечание - Необходимо указывать температуру, при которой проводились данные исследования.
3.3.3 Другая полезная информация может включать данные о токсичности исследуемого вещества для микроорганизмов, данные о первичной и/или характерной биоразлагаемости, об аэробном и анаэробном разложении в почве.
3.3.4 Должны быть известны аналитические методы для количественного анализа исследуемого вещества и, если применимо, для идентификации и количественного анализа продуктов разложения в воде и осадках.
3.4 Вещества сравнения
При возможности должны быть использованы вещества сравнения для идентификации и количественного анализа продуктов разложения спектроскопическими и хроматографическими методами.
3.5 Критерии качества
3.5.1 Эффективность определения
Необходимо провести извлечение и анализ, по крайней мере, двух идентичных образцов воды и отложений сразу после добавления исследуемого вещества для изначального подтверждения воспроизводимости аналитического метода и применимости метода внесения исследуемого вещества. Эффективность определения на последующих стадиях эксперимента определяется балансом вещества (при использовании радиоактивно меченного материала). Она должна находиться в диапазоне от 90 % до 110 % для меченных [6], и от 70 % до 110 % - для немеченных соединений.
3.5.2 Воспроизводимость и чувствительность аналитического метода
3.5.2.1 Удостовериться в воспроизводимости аналитического метода/методов (исключая эффективность изначальной экстракции) для количественного определения исследуемого вещества и продуктов разложения можно, проведя анализ экстрактов этих же образцов воды и отложений, дважды после того, как они будут инкубироваться достаточное время для образования значительного количества определяемых продуктов разложения.
3.5.2.2 Предел чувствительности аналитического метода анализа исследуемого вещества и продуктов разложения должен составлять 0,001 мг/кг в воде или осадках, или 1% от количества вносимого изначально вещества, в зависимости от того, какое значение ниже. Предел количественного определения также может быть указан.
3.6 Погрешности данных о разложении
Регрессионный анализ зависимости концентрации исследуемого вещества от времени позволяет получить информацию о погрешности кривой разложения и рассчитать границы доверительного интервала для периодов полуразложения (в случае, если применима кинетика псевдо-первого порядка) или значений , а также, если применимо,
и
.
4 Описание метода исследования
4.1 Оборудование и установка
4.1.1 Испытание вещества необходимо проводить в стеклянной таре (например, в колбах, центрифужных пробирках), кроме случаев, когда заранее известная информация (такая, как коэффициент разделения н-октанол/вода, данные о сорбции вещества и т. д.) указывает на то, что вещество может прилипать к стеклу. В таких случаях возможно использование альтернативных материалов (таких, как тефлон). Проблему прикрепления вещества к стеклу также можно решить одним из следующих способов:
- определить массы исследуемого вещества и продуктов разложения, адсорбировавшихся на стекле;
- промыть всю тару раствором растворителя в конце исследования;
- использовать специальные средства (см. 5.2.3);
- использовать увеличенное количество сорастворителя при добавлении исследуемого вещества к тест-системе; при этом необходимо убедиться, что этот сорастворитель не вступает в реакцию обмена с исследуемым веществом
4.1.2 Примеры типичных установокпроточных и биометрических систем приведены соответственно в приложениях B и C [11]. Другие полезные системы инкубации описаны в [12].
4.1.3 Конструкция экспериментальной установки должна позволять воздухообмен или циркуляцию азота, а также улавливать летучие вещества. Размеры испытательной установки должны соответствовать требованиям эксперимента (см. 5.1.1). Вентиляцию можно осуществлять осторожным барботированием или циркуляцией воздуха или азота над поверхностью воды. В последнем случае для лучшего распределения кислорода или азота в воде рекомендуется осуществить осторожное перемешивание воды сверху вниз. Не следует использовать для этих целей воздух без углекислого газа, так как это может привести к увеличению рН воды. В любом случае возмущение осадка нежелательно, и его необходимо избегать насколько это возможно. Исследование малолетучих веществ необходимо проводить в системах биометрического типа при осторожном перемешивании поверхностного слоя воды. Возможно использование закрытых резервуаров, свободное пространство в которых должно быть заполнено атмосферным воздухом или азотом, с внутренними емкостями для улавливания летучих веществ [13]. При аэробном исследовании необходимо периодически обменивать газ в свободном пространстве для компенсации кислорода, потребленного биомассой.
4.1.4 В качестве подходящих уловителей для летучих веществ можно использовать растворы с концентрацией 1 моль/дм гидроксида калия или натрия для диоксида углерода
и этиленгликоль, этаноламин или 2%-ный раствор парафина в ксилоле для улавливания органических веществ. Летучие соединения, образовавшиеся при анаэробных условиях, такие как метан, могут быть задержаны на молекулярных ситах. Такие вещества можно сжечь, например при пропускании
через кварцевую трубку, содержащую
, при 900°С. Образовавшийся углекислый газ можно уловить щелочью [14].
________________
Данные щелочные абсорбирующие растворы также поглощают углекислый газ из вентиляционного воздуха и углекислый газ, образованный в процессе дыхания в аэробных экспериментах. Следует периодически заменять эти растворы во избежание их насыщения и потери абсорбционной способности.
4.1.5 Необходимо использовать лабораторные инструменты для анализа исследуемого вещества и продуктов трансформации (газо-жидкостная хроматография, высокоэффективная жидкостная хроматография (ВЭЖХ), тонкослойная хроматография (ТСХ), масс-спектроскопия (МС), газовая хроматография - масс-спектрометрия (ГХ-МС), ядерный магнитный резонанс (ЯМР) и т. д.), включая соответствующие системы обнаружения радиоактивно меченных и немеченных веществ. В случае применения радиоактивно меченных веществ необходимо использовать жидкостный сцинтилляционный счетчик и окислитель для горения (для сжигания проб отложений перед измерением радиоактивности).
4.1.6 Также необходимо другое соответствующее стандартное лабораторное оборудование для физико-химических и биологических измерений, стеклянная тара, химические вещества и реагенты.
4.2 Выбор мест отбора проб и их количество
В любой ситуации необходимо выбирать места отбора проб в зависимости от целей исследования. При определении мест отбора проб следует учитывать пути формирования водосборного бассейна (сельскохозяйственные, промышленные, бытовые стоки) и воды выше по течению. Нельзя использовать донные отложения, которые в течение четырех предыдущих лет могли быть загрязнены исследуемым веществом или его структурными аналогами.
4.3 Выбор донных отложений
4.3.1 Для проведения аэробных исследований используются два вида донных отложений [7], при этом они должны различаться по содержанию органического углерода и текстуре. Один из видов отложений должен характеризоваться высоким уровнем содержания органического углерода (от 2,5% до 7,5%) и мелкозернистой структурой, другой - низким уровнем содержания органического углерода (от 0,5% до 2,5%) и крупнозернистой структурой.
Обычно разница в содержании органического углерода должна составлять не менее 2%. Мелкозернистая структура определяется как содержание (глина+ил)>50%, крупнозернистая структура: (глина+ил)<50%. Разница в содержании (глина+ил) двух образцов должна составлять не менее 20%. Если химическое вещество может попадать в морскую воду - в качестве одного из видов отложений следует использовать морской осадок.
________________
[глина+ил] - минеральная часть отложений с размером частиц менее 50 мкм.
4.3.2 В случае проведения строго анаэробного исследования два вида отложений (включая соответствующие воды) должны отбираться из анаэробных зон открытых водоемов [7]. Отложения, как и их водные фазы, следует транспортировать с осторожностью, избегая доступа кислорода.
4.3.3 Другие параметры также могут оказаться значительными, и их следует принимать во внимание в зависимости от случая. Например, значения рН отложений могут оказаться важными, если существует зависимость разложения и/или сорбции исследуемого вещества от рН. Зависимость сорбции вещества от рН может отражаться значением вещества.
4.4 Определение характеристик проб донные "отложения - вода"
4.4.1 Основные показатели, которые необходимо определить и привести (с указанием использованного метода) для вод и отложений, а также момент исследования, в котором должны определяться эти параметры, приведены в таблице 1. Для информации: методы для определения этих параметров приводятся в [15-18].
Таблица 1 - Измерение показателей для описания проб "донные отложения - вода"
Показатель | Стадия исследования | |||||
Отбор проб в полевых условиях | Обращение после изначального отбора проб | Начало акклима- | Начало теста | Во время теста | Конец теста | |
Вода | ||||||
Источник | x | |||||
Температура | x | |||||
рН | x | x | x | x | x | |
Общий органический углерод (ТОС) | x | x | x | |||
Содержание | x | x | x | x | x | |
ОВП* | x | x | x | x | ||
Отложения | ||||||
Источник | x | |||||
Глубина слоя | x | |||||
рН | x | x | x | x | x | |
Гранулометрический состав | x | |||||
ТОС | x | x | x | x | ||
Микробная биомасса** | x | x | x | |||
ОВП* | Наблюдение (цвет/запах) | x | x | x | x | |
* Определение содержания кислорода в воде и окислительно-восстановительного потенциала (ОВП) при росте популяций микроорганизмов в поверхностных водах не имеют значения для определения механизма реакции или прогностической ценности [21, 22]. Более полезным для интерпретации и оценки скорости аэробного биоразложения и его путей может оказаться определение значений биохимической потребности в кислороде БПК (BOD), при первичном отборе проб в полевых условиях, в начале и при окончании исследования, концентраций в воде микро/макропитательных веществ - ** Метод интенсивности дыхания микроорганизмов [23], фумигация [24], определение количества микроорганизмов посевом (бактерий, актиномецетов, грибов, колоний всего) при аэробных исследованиях; метаногенез при анаэробных исследованиях. | ||||||
4.4.2 Также в зависимости от ситуации может потребоваться определить другие показатели (например, для пресной воды: содержание частиц, щёлочность, жесткость, проводимость, ![]() (соотношение и индивидуальные значения); для отложений: емкость катионного обмена, водоудерживающая способность, содержание карбонатов, суммарного азота и фосфора; для морских систем: соленость). При исследовании окислительно-восстановительных процессов, особенно в случае анаэробного исследования, может быть полезным определить содержание нитратов, сульфатов, биодоступного железа, а также других возможных акцепторов электронов.
(соотношение и индивидуальные значения); для отложений: емкость катионного обмена, водоудерживающая способность, содержание карбонатов, суммарного азота и фосфора; для морских систем: соленость). При исследовании окислительно-восстановительных процессов, особенно в случае анаэробного исследования, может быть полезным определить содержание нитратов, сульфатов, биодоступного железа, а также других возможных акцепторов электронов.
4.5 Отбор, обращение, хранение
4.5.1 Отбор
Отбор проб следует проводить в соответствии с черновым вариантом отбора проб донных осадков [8]. Образцы отложений должны браться из всего верхнего слоя отложений от 5 до 10 см толщиной. Соответствующие водные фазы должны отбираться из того же места одновременно с отложениями. Для исследования в анаэробных условиях отложения и вода должны забираться и транспортироваться в бескислородных условиях [25], см. также 4.3.2. Некоторые устройства для отбора проб описаны в [8, 20].
4.5.2 Обращение
Отложения отделяют от воды фильтрацией, затем их просеивают сквозь 2 мм сито, используя при этом избыточное количество воды, отобранной в том же месте, что и осадки. Определенные количество осадков и воды смешивают в колбах для последующей инкубации в необходимом соотношении (см. 5.1.1) и готовят для периода акклиматизации (см. 4.5). При проведении анаэробных исследований все операции должны проводиться без доступа кислорода [26-30].
4.5.3 Хранение
Рекомендуется использовать только что отобранные образцы воды и донных отложений. Однако, если стадия хранения необходима, следует отфильтровать воду и просеять отложения методом, описанным выше, и хранить их вместе, под слоем воды (толщиной от 6 до 10 см), в темноте, при температуре (4±2)°С не более четырех недель [7, 8, 20]. Образцы для аэробных исследований должны храниться в сосудах со свободным доступом к кислороду (например, в открытых контейнерах), образцы для анаэробных исследований, наоборот, надлежит хранить, исключая возможность доступа кислорода. Нельзя допускать замораживания отложений или воды, а также высыхание отложений во время транспортировки или хранения.
________________
Последние исследования показали, что хранение при 4°С может приводить к уменьшению содержания органического углерода а осадках, что, возможно, может привести к уменьшению микробной активности.
4.6 Подготовка образцов донных отложений/воды к проведению исследований
Перед проведением исследования вещества необходимо провести акклиматизацию образцов отложений и воды. При этом все образцы воды/отложений должны быть помещены в инкубационные резервуары, которые будут использоваться при дальнейших исследованиях, и выдерживаться при условиях, идентичным тем, что будут при проведении самого исследования (см. 5.1.1 и 5.1.2). Под периодом акклиматизации понимают время, необходимое для достижений системы относительно стабильного состояния по таким параметрам, как рН, концентрация кислорода в воде, окислительно-восстановительный потенциал отложений и воды, а также достижение макроскопического разделения фаз. Обычно период акклиматизации может продолжаться от одной до двух недель и не должен превышать четырех недель. В отчете следует приводить результаты данных измерений.
5 Проведение испытания
5.1 Условия проведения эксперимента
5.1.1 Исследование должно проводиться в инкубаторе (см. 4.1.1-4.1.3), заполненном водой в объемном соотношении от 3:1 до 4:1, толщина слоя осадков должна составлять (2,5±0,5) см. Рекомендуемое минимальное количество осадков на инкубационный резервуар составляет 50 г (сухого веса).
5.1.2 Эксперимент необходимо проводить в темноте при постоянной температуре от 10°С до 30°С. Температура (20±2)°С является приемлемой. По необходимости, в зависимости от конкретного случая возможно проведение дополнительного испытания при более низкой температуре (например, 10°С), в зависимости от задач исследования. Температура инкубации должна контролироваться и фиксироваться.
5.2 Обращение с исследуемым веществом и его применение
5.2.1 Используется одна исследуемая концентрация вещества. Для химических веществ, предназначенных для защиты растений и попадающих непосредственно в водные объекты, максимальная дозировка на этикетке должна соответствовать максимальной дозировке, высчитанной на основании площади водной поверхности использованной при тестировании емкости. Во всех других случаях используемый уровень концентрации должен основываться на прогнозах возможных поступлений из окружающей среды. Необходимо тщательно отследить, чтобы используемый уровень концентрации был соответствующим для целей определения процесса разложения и процессов образования и снижения содержания продуктов разложения. Возможно применение повышенных (например, в 10 раз) доз в случаях, когда концентрация исследуемого вещества близка к пределу обнаружения в начале исследования и/или когда основные продукты преобразования трудно обнаружить при концентрации 10% от концентрации тестируемого вещества при его внесении. В случае применения более высоких концентраций последние не должны оказывать негативного влияния на микробную активность в системе "донные отложения - вода". Для достижения постоянной концентрации исследуемого вещества в емкостях разных объемов может оказаться необходимым скорректировать количество применяемого материала на основании глубины водного столба в емкости относительно глубины воды в полевых условиях (которая принимается за 100 см, однако могут применяться и другие величины). Образцы расчетов приведены в приложении D.
__________________
Тестирование второй концентрации может оказаться полезным для химических веществ, попадающих в поверхностные воды различными путями, достигая при этом значительно отличных друг от друга концентраций, при условии, что более низкая концентрация может быть проанализирована с достаточной точностью.
5.2.2 Идеально, если исследуемое вещество должно вводиться в виде водного раствора в водную фазу тест-системы. Если это неизбежно, допускается добавление смешивающихся с водой растворителей (таких как ацетон, этанол) в малых количествах для внесения и распределения исследуемого вещества, но их содержание не должно превышать 1% об/об и не должно оказывать негативного влияния на микробную активность тестируемой системы. Необходимо внимательно подходить к приготовлению водного раствора тестируемого вещества: для этих целей будет целесообразно использовать генераторные колонны и предварительное смешивание для полной однородности раствора. После добавления водного раствора в исследуемую систему рекомендуется медленно помешивать водную фазу, минимально затрагивая осадок.
5.2.3 Применение специальных средств не является рекомендуемой практикой, так как их компоненты могут негативно воздействовать на распределение исследуемого вещества и/или продуктов разложения между водной и осадочной фазами. Для исследуемых веществ с плохой растворимостью использование специального средства может быть вполне уместной альтернативой.
5.2.4 Количество инкубационных резервуаров зависит от количества отборов проб (см. 5.3.1). В исследовании необходимо использовать достаточное количество тестируемых систем, чтобы иметь возможность использовать по две системы при каждом отборе проб. В случае, если при тестировании используются контрольные установки для каждой системы "вода - осадок", в них не должно добавляться исследуемое вещество. Контрольные установки могут применяться для определения микробной биомассы в осадке и общего органического углерода в воде, и осадке по окончании исследования. Две контрольные установки (т.е. по одной установке для каждой системы "вода - осадок") могут использоваться для отслеживания требуемых параметров осадка и воды в ходе акклиматизации (см. таблицу в 4.4.1). В исследование необходимо включить две дополнительные контрольные установки в случае, если исследуемое вещество применяется с использованием растворителей для установления негативного воздействия на микробную активность в тестируемой системе.
5.3 Продолжительность исследования и отбор проб
5.3.1 Продолжительность эксперимента обычно не должна превышать 100 дней [6], и исследование должно продолжаться до тех пор, пока не будет установлен ход разложения и принцип распределения воды и осадка или пока 90% исследуемого вещества не будет удалено путем разложения и/или испарения. Количество отборов проб должно составлять, по меньшей мере, шесть (включая нулевой отбор). При этом возможно проведение факультативного предварительного исследования для установления соответствующего режима отбора проб и продолжительности тестирования, если только в наличии нет достаточной информации о тестируемом веществе, оставшейся от предыдущих исследований. Для исследуемых веществ с гидрофобными свойствами может оказаться необходимым назначить дополнительные отборы проб на начальном этапе исследования для установления соотношения распределения между фазами воды и осадка.
5.3.2 Во время соответствующих отборов проб на анализ берутся инкубационные сосуды (одинаковые) полностью. Осадок и вода подвергаются анализу отдельно. Поверхностную воду необходимо отделять осторожно, с минимальным возмущением осадка. Выделение и определение характеристик исследуемого вещества и продуктов разложения должны производиться соответствующими аналитическими методами. Необходимо с осторожностью удалять материал, который мог абсорбироваться стенками инкубационного сосуда или соединительными трубками, улавливающими испарения.
________________
В случае когда легко может произойти быстрый процесс повторного окисления продуктов анаэробного разложения, анаэробные условия должны поддерживаться в ходе отбора проб и проведения анализа.
5.4 Факультативное предварительное исследование
Если длительность тестирования и режим отбора проб не могут быть установлены на основании данных похожих исследований изучаемого вещества, может оказаться целесообразным факультативное предварительное исследование, которое следует проводить в тех же условиях, что и окончательное исследование. В случае его проведения должен быть составлен краткий отчет о существенных условиях эксперимента и результатах, полученных в ходе этого предварительного исследования.
5.5 Измерение и анализ
5.5.1 При каждом отборе проб необходимо измерять концентрацию исследуемого вещества в воде и осадке и составлять отчет по результатам (с показателями концентрации и процентного содержания вносимого вещества). В целом, продукты разложения в количестве ?10 % от радиоактивно меченного вещества во всей системе "вода - осадок" в ходе любого отбора проб должны определяться, если только не предоставлено обоснованное объяснение обратного. Также должны выявляться продукты разложения, концентрация которых постоянно растет в ходе исследования, даже если она не превышает вышеупомянутых пределов, так как это может свидетельствовать об устойчивости. Последняя должна учитываться в зависимости от случая, при этом в отчете должны предоставляться соответствующие объяснения.
5.5.2 Продукты, полученные из газо- и пароулавливающих систем ( и прочие, т.е. летучие органические смеси), также должны включаться в отчет при каждом отборе проб. Для них необходимо указывать степень минерализации. Информация о связанных остатках в осадке включается в отчет при каждом отборе проб.
6 Данные и отчетность
6.1 Обработка результатов и расчеты
6.1.1 Общий баланс массы или эффективность (см. 4.5.1) определения добавленного радиоактивно меченного вещества должны высчитываться по время каждого отбора проб. Результаты помещаются в отчет в виде процентного содержания добавленного радиоактивно-меченого вещества. Распределение радиоактивности между водой и осадком включается в отчет в показателях концентрации и процентного содержания в ходе каждого отбора проб.
6.1.2 Период полураспада, показатель и, если возможно,
и
исследуемого вещества должны высчитываться одновременно с их доверительными пределами (см. 4.6). Информация о показателе рассеивания исследуемого вещества в воде и в осадке может быть получена при помощи соответствующих оценочных инструментов. Эти последние могут варьироваться от применения кинетики псевдопервого порядка, вычерчивания эмпирической кривой с применением графических или числовых решений и более сложные системы оценки, применяющие, например, моно- и мультикомпартментальные модели. Дальнейшие подробности описаны в [32-34].
6.1.3 Все подходы имеют свои сильные и слабые стороны и значительно отличаются по сложности. Допущение кинетик первого порядка может оказаться чрезмерным упрощением процессов разложения и распределения, но при возможности дает простой показатель (константу скорости или период полураспада), который легок для понимания и представляет ценность при имитационном моделировании и расчетах прогнозируемых концентраций в окружающей среде. Эмпирические подходы или линейные преобразования могут иметь результатом то, что кривая графика будет в большей степени соответствовать данным и, следовательно, позволят провести более точную оценку периодов полураспада, показателя и, если возможно,
и
. Применение производных констант, тем не менее, ограничено. С помощью составных моделей можно определить ряд полезных констант, применимых для оценки риска, описывающей показатель разложения в разных камерах и распределение химического вещества. Их также следует применять для оценки констант скорости формирования и распада основных продуктов разложения. Выбор метода должен быть обоснован, а исследователь должен графически и/или статистически продемонстрировать его хорошую согласованность.
6.2 Отчет об исследовании
6.2.1 Отчет об исследовании должен включать следующую информацию:
Исследуемое вещество:
- общеизвестное название, химическое название, номер CAS, структурная формула (с указанием местоположения изотопа(ов), если применяется радиоактивно меченное вещество) и значимые физико-химические свойства;
- чистота (примеси) исследуемого вещества;
- радиохимическая чистота меченного вещества и показатель молярной активности (если целесообразно).
Вещества сравнения:
- химическое название и структура веществ сравнения, используемых для определения характеристик и/или идентификации продуктов разложения.
Исследуемые осадок и вода:
- расположение и описание места отбора образцов водного осадка, включая, по возможности, историю загрязнения;
- вся информация по отбору, хранению (если имеет место) и акклиматизации систем "вода - осадок";
- характеристики водно-осадочных образцов (таблица 1).
Условия проведения исследования:
- используемая при исследовании система (проточность, биологический индикатор, способ вентилирования, метод перемешивания, объем воды, масса осадка, толщина слоя воды и слоя осадка, объем резервуаров и т.д.);
- применение исследуемого вещества в тестируемой системе: тестируемая концентрация, количество повторов и режим контроля применения исследуемого вещества (например, использование растворителей, если использовались) и т.д.;
- температура инкубации;
- отборы проб;
- методы экстракции и эффективность, а также аналитические методы и пределы обнаружения;
- методы определения характеристик/идентификации продуктов разложения;
- отклонения от протокола или условий исследования в ходе тестирования.
Результаты:
- необработанные данные типичных анализов (вся необработанная информация должна храниться в GLP-архиве);
- повторяемость и чувствительность применяемых аналитических методов;
- показатели эффективности определения;
- таблицы с результатами, выраженными в процентах от примененной дозы и в мг·кг в воде, осадке и всей системе (только в процентах) для исследуемого вещества и, если возможно, для продуктов разложения и неэкстрагируемого радиоактивно меченного вещества;
- баланс массы вещества в ходе и в конце исследования;
- графическое изображение разложения в водной и осадочной фракциях и во всей системе в целом (включая минерализацию);
- показатели минерализации;
- период полураспада, показатель и, если возможно,
и
исследуемого вещества и, если уместно, для продуктов разложения, включая доверительные пределы в воде, осадке и всей системе в целом;
- оценка кинетик разложения исследуемого вещества и, если целесообразно, продуктов разложения;
- предполагаемый ход разложения, если необходимо;
- обсуждение полученных результатов.
Приложение A
(справочное)
Аэробные и анаэробные тест-системы
А.1 Аэробная тест-система
В настоящем стандарте описывается аэробная система, состоящая из: аэробного слоя водного (типичные значения концентрации кислорода 7-10 мг/л) и слоя отложений, аэробного на поверхности и анаэробного в глубине (в анаэробной зоне отложений типичные значения окислительно-восстановительного потенциала () находятся в диапазоне от минус 80 до минус 90 мВ. Для поддержания постоянной концентрации кислорода в каждой инкубационной установке над водной поверхностью должен циркулировать увлажненный воздух.
А.2 Анаэробная тест-система
Ход анаэробного исследования принципиально не отличается от исследования с помощью аэробных тест-систем за исключением того, что над поверхностью воды в каждой инкубационной установке циркулируется увлажненный азот, для того чтобы свободное пространство было все время заполнено азотом. Осадки и вода могут считаться анаэробными, если значение окислительно-восстановительного потенциала составляет менее - 100 мВ.
При анаэробном исследовании, определение минерализации включает измерение выделенного углекислого газа и метана.
Приложение B
(рекомендуемое)
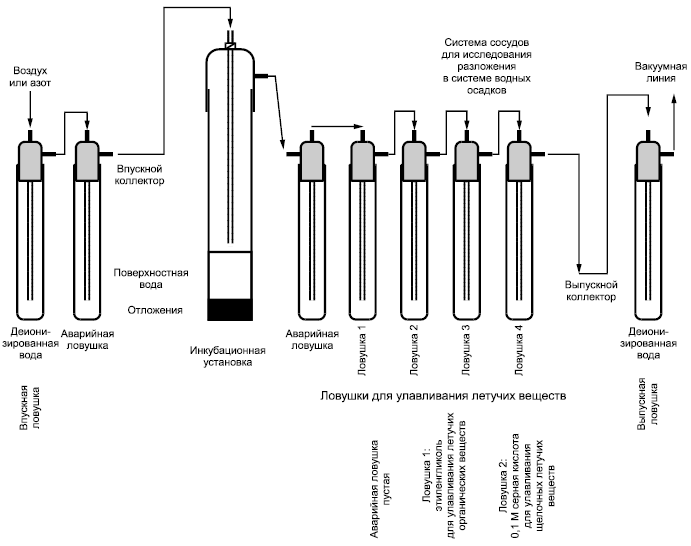
Пример газопроточной установки
|
Рисунок B.1
Приложение C
(рекомендуемое)
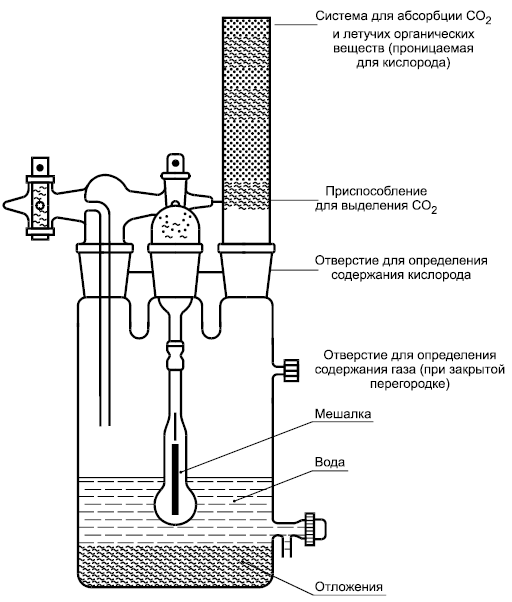
Пример биометрической установки
|
Рисунок C.1
Приложение D
(рекомендуемое)
Пример расчета концентрации, вносимой в испытательную установку
Внутренний диаметр цилиндра | 8 см |
Толщина водной колонны, исключая осадок | 12 см |
Площадь поверхности: 3,142 | 50,3 см |
Дозирование вещества: 500 г исследуемого вещества/га соответствует | 5 мкг/см |
Всего: 5 | 251,5 мкг |
Скорректируйте количество на долю от глубины в 100 см: | 30,18 мкг |
Объем водной колонны: 50,3 | 603 мл |
Концентрация в воде: 30,18 | 0,050 мкг/мл или 50 мкг/л |
Библиография
[1] | BBA-Guidelines for the examination of plant protectors in the registration process. (1990). Part IV, Section 5-1: Degradability and fate of plant protectors in the water/sediment system. Germany. |
[2] | Commission for registration of pesticides: Application for registration of a pesticide. (1991). Part G. Behaviour of the product and its metabolites in soil, water and air, Section G.2.1 (a). The Netherlands. |
[3] | MAFF Pesticides Safety Directorate (1992). Preliminary guideline for the conduct of biodegradability tests on pesticides in natural sediment/water systems. Ref No SC 9046. United-Kingdom. |
[4] | Agriculture Canada: Environmental chemistry and fate (1987). Guidelines for registration of pesticides in Canada. Aquatic (Laboratory) - Anaerobic and aerobic. Canada, pp. 35-37. |
[5] | US-EPA: Pesticide assessment guidelines. Subdivision N. Chemistry: Environmental fate (1982). Section 162-3, Anaerobic aquatic metabolism. |
[6] | SETAC-Europe publication (1995). Procedures for assessing the environmental fate and ecotoxicity of pesticides. Ed. Dr Mark R. Lynch. SETAC-Europe, Brussels. |
[7] | OECD Test Guidelines Programme (1995). Final Report of the OECD Workshop on Selection of Soils/sediments. Belgirate. Italy, 18-20 January 1995. |
[8] | ISO/DIS 5667-12 (1994). Water quality - Sampling - Part 12. Guidance on sampling of bottom sediments. |
[9] | US-EPA (1998a). Sediment/water microcosm biodegradation test. Harmonised Test Guidelines (OPPTS 835.3180). EPA 712-C-98-080. |
[10] | OECD (1993). Guidelines for Testing of Chemicals. Paris. OECD (1994-2000): Addenda 6-11 to Guidelines for the Testing of Chemicals. |
[11] | Scholz. K., Fritz R., Anderson С. and Spiteller M. (1988) Degradation of pesticides in an aquatic model ecosystem. BCPC - Pests and Diseases, 3B-4, 149-158. |
[12] | Guth, J.A. (1981). Experimental approaches to studying the fate of pesticides in soil. In Progress in Pesticide Biochemistry (D.H. Hutson. T.R. Roberts. Eds.). Vol.1, 85-114. J. Wiley & Sons. |
[13] | Madsen, Т., Kristensen, P. (1997). Effects of bacterial inoculation and non-ionic surfactants on degradation of polycyclic aromatic hydrocarbons in soil. Environ. Toxicol. Chem. 16, 631-637. |
[14] | Steber, J., Wierich, P. (1987). The anaerobic degradation of detergent range fatty alcohol ethoxylates. Studies with 14C-labelled model surfactants. Water Research 21, 661-667. |
[15] | Black, C.A (1965). Methods of Soil Analysis. Agronomy Monograph No.9. American Society of Agronomy, Madison. |
[16] | APHA (1989). Standard Methods for Examination of Water and Wastewater (17th edition). American Public Health Association, American Water Works Association and Water Pollution Control Federation, Washington D.C. |
[17] | Rowell, D.L. (1994). Soil Science Methods and Applications. Longman. |
[18] | Light, T.S. (1972). Standard solution for redox potential measurements. Anal. Chemistry 44, 1038-1039. |
[19] | SETAC-Europe publication (1991). Guidance document on testing procedures for pesticides in freshwater mesocosms. From the Workshop "A Meeting of Experts on Guidelines for Static Field Mesocosms Tests", 3-4 July 1991. |
[20] | SETAC-Europe publication (1993). Guidance document on sediment toxicity tests and bioassays for freshwater and marine environments. From the Workshop On Sediment Toxicity Assessment (WOSTA), 8-10 November 1993. Eds.: I.R. Hill, P. Matthiessen and F. Heimbach. |
[21] | Vink, J.P.M., van der Zee, S.E.A.T.M. (1997). Pesticide biotransformation in surface waters: multivariate analyses of environmental factors at field sites. Water Research 31, 2858-2868. |
[22] | Vink, J.P.M., Schraa, G., van der Zee, S.E.A.T.M. (1999). Nutrient effects on microbial transformation of pesticides in nitrifying waters. Environ. Toxicol., 329-338. |
[23] | Anderson, Т.Н., Domsch, K.H. (1985). Maintenance carbon requirements of activelymetabolising microbial populations under in-situ conditions. Soil Biol. Biochem. 17, 197-203. |
[24] | ISO-14240-2. (1997). Soil quality - Determination of soil microbial biomass - Part 2: Fumigation-extraction method. |
[25] | Beelen, P. van and F. van Keulen. (1990). The Kinetics of the Degradation of Chloroform and Benzene in Anaerobic Sediment from the River Rhine. Hydrobiol. Bull. 24(1), 13-21. |
[26] | Shelton, D.R. and Tiedje, J.M. (1984). General method for determining anaerobic biodegradation potential. App. Environ. Microbiol. 47, 850-857. |
[27] | Birch, R.R., Biver, C., Campagna, R., Gledhill, W.E., Pagga, U., Steber, J., Reust, H. and Bontinck, W.J. (1989). Screening of chemicals for anaerobic biodegradation. Chemosphere 19, 1527-1550. |
[28] | Pagga, U. and Beimborn, D.B. (1993). Anaerobic biodegradation tests for organic compounds. Chemoshpere 27, 1499-1509. |
[29] | Nuck, B.A. and Federle, T.W. (1986). A batch test for assessing the mineralisation of 14C radiolabelled compounds under realistic anaerobic conditions. Environ. Sci. Technol. 30, 3597-3603. |
[30] | US-ЕРА (1998b). Anaerobic biodegradability of organic chemicals. Harmonised Test Guidelines (OPPTS 835.3400). EPA 712-C-98-090. |
[31] | Sijm, Haller and Schrap (1997). Influence of storage on sediment characteristics and drying sediment on sorption coefficients of organic contaminants. Bulletin Environ. Contam. Toxicol. 58, 961-968. |
[32] | Timme, G., Frehse H. and Laska V. (1986) Statistical interpretation and graphic representation of the degradational behaviour of pesticide residues II. Pflanzenschutz - Nachrichten Bayer, 39, 187-203. |
[33] | Timme, G., Frehse. H. (1980) Statistical interpretation and graphic representation of the degradational behaviour of pesticide residues I. Pflanzenschutz - Nachrichten Bayer, 33, 47-60. |
[34] | Carlton, R.R. and Allen, R. (1994). The use of a compartment model for evaluating the fate of pesticides in sediment/water systems. Brighton Crop Protection Conference - Pest and Diseases, pp. 1349-1354. |
УДК 658.382.3:006.354 | МКС 71.040.50 |
Ключевые слова: химическая продукция, воздействие на окружающую среду, окружающая среда, острая токсичность, рыбы | |
Электронный текст документа
и сверен по:
, 2019