ГОСТ ISO 10993-15-2023
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
Изделия медицинские
ОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 15
Идентификация и количественное определение продуктов деградации изделий из металлов и сплавов
Medical devices. Biological evaluation of medical devices. Part 15. Identification and quantification of degradation products from metals and alloys
МКС 11.100.20
Дата введения 2024-06-01
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией "Институт медико-биологических исследований и технологий" (АНО "ИМБИИТ") на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 31 мая 2023 г. N 162-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
Армения | AM | ЗАО "Национальный орган по стандартизации и метрологии" Республики Армения |
Беларусь | BY | Госстандарт Республики Беларусь |
Киргизия | KG | Кыргызстандарт |
Россия | RU | Росстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 14 июля 2023 г. N 536-ст межгосударственный стандарт ГОСТ ISO 10993-15-2023 введен в действие в качестве национального стандарта Российской Федерации с 1 июня 2024 г.
5 Настоящий стандарт идентичен международному стандарту ISO 10993-15:2019* "Оценка биологического действия медицинских изделий. Часть 15. Идентификация и количественное определение продуктов деградации изделий из металлов и сплавов" ("Biological evaluation of medical devices - Part 15: Identification and quantification of degradation products from metals and alloys", IDT).
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ 1.5-2001 (подраздел 3.6).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА
6 ВЗАМЕН ГОСТ ISO 10993-15-2011
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге "Межгосударственные стандарты"
Введение
ISO (Международная организация по стандартизации) является федерацией национальных органов по стандартизации (органов - членов ISO). Работу по подготовке международных стандартов проводят через технические комитеты ISO. Каждая организация-член, заинтересованная в области деятельности, для которой создан технический комитет, имеет право быть представленной в данном комитете. Международные правительственные и неправительственные организации также принимают участие в работе ISO. ISO тесно сотрудничает с Международной Электротехнической Комиссией (IEC) по вопросам стандартизации электротехнической продукции.
Процедуры, примененные при разработке настоящего стандарта, а также процедуры, предназначенные для его дальнейшей поддержки, приведены в Директивах ISO/IEC, часть 1. В частности, следует отметить наличие различных критериев утверждения для различных типов документов ISO. Настоящий стандарт подготовлен в соответствии с редакционными правилами Директив ISO/IEC, часть 2 (см. www.iso.org/directives).
Некоторые элементы настоящего стандарта могут быть объектом патентных прав. ISO не несет ответственности за обозначение каких-либо патентных прав. Сведения о патентных правах, обозначенных при разработке настоящего стандарта, будут указаны во введении и/или в перечне полученных патентных деклараций ISO (см. www.iso.org/patents).
Любая торговая марка продукции, приведенная в настоящем стандарте, является информацией, указанной для удобства пользователей, и не является рекламой.
Для разъяснения добровольного характера применения стандартов, значений конкретных терминов ISO и выражений, относящихся к оценке соответствия, а также информации о соблюдении ISO принципов Всемирной торговой организации (ВТО) по техническим барьерам в торговле (ТВТ) см. следующий URL: www.iso.org/iso/foreword.html.
Настоящий стандарт разработан Техническим комитетом ISO/TC 194 "Биологическая и клиническая оценка медицинских изделий".
Настоящий стандарт представляет собой второе пересмотренное издание, которое отменяет и заменяет первое издание ISO 10993-15:2000, и содержит следующие изменения:
a) настоящий стандарт распространяется на материалы, предназначенные и непредназначенные для деградации в организме человека;
b) в методах исследований учтены требования к наноматериалам и соответствующих стандартов на конкретные материалы;
c) более подробно указан состав испытательного раствора (электролита);
d) конкретизированы требования к форме образцов;
e) иммерсионный метод исследования изложен более подробно;
f) приложение С предыдущего издания изменено и в настоящем стандарте приведено как приложение А.
Перечень всех стандартов серии ISO 10993 приведен на официальном сайте ISO.
Все отзывы и вопросы по настоящему стандарту следует направлять в национальный орган по стандартизации пользователя. Полный перечень национальных органов по стандартизации приведен по адресу www.iso.org/members.html.
Одна из потенциальных опасностей для здоровья человека, возникающих в результате использования медицинского изделия, может быть связана с взаимодействием продуктов его электрохимического разложения с биологической средой. Таким образом, идентификация и количественное определение потенциальных продуктов деградации металлов и сплавов методами, подходящими для оценки их электрохимических свойств, является необходимым этапом в исследовании биологических характеристик материалов, предназначенных для изготовления медицинских изделий.
В биологических средах металлические материалы могут подвергаться деградации в различной степени, и продукты деградации могут по-разному взаимодействовать с биологической средой. Следовательно, идентификация и количественное определение продуктов деградации металлов и сплавов является важным этапом в оценке биологического действия медицинских изделий.
1 Область применения
Настоящий стандарт распространяется на медицинские изделия (далее - МИ), их компоненты и материалы, изготовленные из металлов и сплавов, и устанавливает методы исследований, применяемые для идентификации и количественного определения продуктов деградации.
Настоящий стандарт распространяется на готовые МИ, продукты деградации которых высвобождаются в процессе изменения химического состава материалов МИ при исследовании методами in vitro. Вследствие особых условий проведения исследований методами in vitro их результаты приблизительно соответствуют результатам исследования имплантата или материала МИ методами in vivo. Методы in vitro, установленные в настоящем стандарте, применяют для получения продуктов деградации с целью их дальнейший оценки.
Настоящий стандарт распространяется на материалы, предназначенные и непредназначенные для деградации в организме человека.
Настоящий стандарт не распространяется на МИ, продукты деградации которых высвобождаются только в результате механических процессов. Методы исследований этого типа МИ и продуктов их деградации установлены в стандартах на конкретные МИ/материалы (при наличии).
Примечание - Как правило, при деградации МИ, вызванной механическими процессами, происходит высвобождение из МИ твердых частиц. Настоящий стандарт не устанавливает методы исследований МИ/материалов и продуктов их деградации, высвобождаемых при механических процессах и вызывающих ответную биологическую реакцию организма. Такие методы установлены в других стандартах серии ISO 10993.
Настоящий стандарт не устанавливает методы исследований биологической активности продуктов деградации (см. ISO 10993-1 и ISO 10993-17).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты [для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных - последнее издание (включая все изменения)]:
ISO 3585, Borosilicate glass 3.3 - Properties (Стекло боросиликатное 3.3. Свойства)
ISO 3696, Water for analytical laboratory use - Specification and test methods (Вода для лабораторного анализа. Технические требования и методы испытаний)
ISO 8044, Corrosion of metals and alloys - Basic terms and definitions (Коррозия металлов и сплавов. Основные термины и определения)
ISO 10993-1, Biological evaluation of medical devices - Part 1: Evaluation and testing within a risk management process (Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования в процессе менеджмента риска)
ISO 10993-9, Biological evaluation of medical devices - Part 9: Framework for identification and quantification of potential degradation products (Оценка биологического действия медицинских изделий. Часть 9. Основные принципы идентификации и количественного определения потенциальных продуктов деградации)
ISO 10993-12, Biological evaluation of medical devices - Part 12: Sample preparation and reference materials (Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы)
ISO 10993-13, Biological evaluation of medical devices - Part 13: Identification and quantification of degradation products from polymeric medical devices (Оценка биологического действия медицинских изделий. Часть 13. Идентификация и количественное определение продуктов деградации полимерных медицинских изделий)
ISO 10993-14, Biological evaluation of medical devices - Part 14: Identification and quantification of degradation products from ceramics (Оценка биологического действия медицинских изделий. Часть 14. Идентификация и количественное определение продуктов деградации изделий из керамики)
ISO 10993-16, Biological evaluation of medical devices - Part 16: Toxicokinetic study design for degradation products and leachables (Оценка биологического действия медицинских изделий. Часть 16. Концепция токсикокинетических исследований продуктов деградации и выщелачиваемых веществ)
3 Термины и определения
В настоящем стандарте применены термины по ISO 8044, ISO 10993-1, ISO 10993-9, ISO 10993-12, а также следующие термины с соответствующими определениями.
ISO и IEC ведут терминологические базы данных для использования в стандартизации по следующим адресам:
- электропедия IEC: доступна по адресу http://www.electropedia.org/;
- платформа онлайн-просмотра ISO: доступна по адресу http://www.iso.org/obp.
3.1 сплав (alloy): Материал, состоящий из металлического элемента с одной или более добавками других металлических и/или неметаллических элементов.
3.2 электролит (electrolyte): Раствор, содержащий ионы и способный проводить электрический ток.
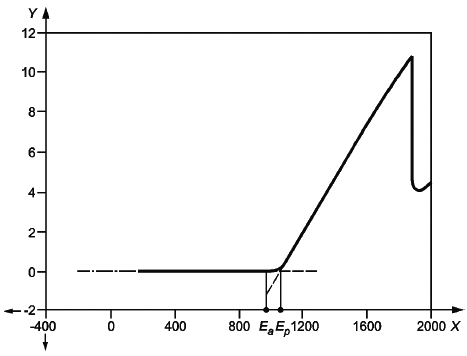
3.3 потенциал электрода при разомкнутой цепи (open-circuit potential): Потенциал электрода, измеренный по отношению к электроду сравнения или другому электроду при отсутствии тока между ними.
Примечание - См. рисунок 1.
Примечание - См. рисунок 1.
3.6 абсорбция (absorb): Проникновение в организм неэндогенного (чужеродного) материала или вещества через клетки и/или ткани или ассимиляция их с течением времени.
3.7 потенциодинамический метод (potentiodynamic test): Метод измерений, в котором потенциал электрода изменяется с заданной скоростью, при этом регистрируют соотношение между плотностью электрического тока и потенциалом электрода.
3.8 потенциостатический метод (potentiostatic test): Метод измерений, в котором изменение тока регистрируют при постоянном потенциале электрода.
4 Общие требования к методам исследований
4.1 Общие положения
Для идентификации и количественной оценки продуктов деградации в материале МИ, изготовленном из металла и/или сплава, применяют два метода исследований. Метод исследования выбирают в зависимости от функционального назначения МИ.
Первый метод - одновременное применении двух электрохимических методов измерений: потенциодинамического и потенциостатического, второй - иммерсионный метод.
Потенциостатический метод измерений применяют с целью получения продуктов деградации материала МИ путем его электрохимического разложения при постоянном потенциале электрода для выполнения их последующего анализа.
Иммерсионный метод исследования применяют для получения продуктов деградации материала МИ путем его химического разложения для проведения их последующего анализа.
При исследовании материала МИ с покрытием, следует учитывать не только продукты деградации самого материала, но и продукты деградации покрытия. Если исследования проводят на материалах МИ с неметаллическим покрытием, то для идентификации и количественного определения потенциальных продуктов деградации такого покрытия следует применять ISO 10993-13 и/или ISO 10993-14.
По результатам идентификации и количественного определения продуктов деградации материалов проводят оценку биологического действия МИ, а при необходимости, и токсикокинетические исследования в соответствии с ISO 10993-16.
Если МИ изготовлены с применением наноматериалов, или размеры продуктов деградации металлических материалов МИ находятся в нанодиапазоне (приблизительно от 1 до 100 нм), то при разработке документов по оценке риска МИ следует учитывать требования ISO/TR 10993-22.
Если МИ изготовлено из металла или сплава, предназначенного для абсорбции организмом, то следует применять соответствующие стандарты, распространяющиеся на конкретные материалы (см. библиографию), устанавливающие методы и условия проведения исследований (например, требования к электролиту, условия окружающей среды и т.д.), специфические для данного типа материала.
4.2 Условия проведения исследований и требования к оборудованию
Скорость реакции электрохимического разложения материала зависит от условий проведения исследований, применяемых измерительных приборов, свойств образца и способов его подготовки. Исследования электрохимической деградации материала МИ должны проводить квалифицированные специалисты в лаборатории, оборудованной соответствующим образом. Техническое обслуживание и калибровку оборудования необходимо осуществлять в соответствии с эксплуатационной документацией, утвержденной в установленном порядке. Методы и условия эксплуатации оборудования должны быть валидированы.
Допускается применять условия проведения исследований на стабильность, время прогрева и т.д., приведенные в [1].
5 Растворы для исследований и подготовка образцов
5.1 Сведения об образцах
Сведения о составе исследуемого(ых) материала(ов) регистрируют в отчете.
5.2 Испытательный раствор (электролит)
При выборе электролита следует учитывать условия клинического применения МИ. Для исследований используют химические вещества степенью чистоты - ч.д.а., воду - степенью чистоты 2 по ISO 3696, при этом все химические вещества должны быть растворимыми в воде.
В качестве электролита рекомендуется применять изотонический 0,9%-ный водный раствор хлорида натрия.
В зависимости от состава исследуемого металла или сплава и механизма коррозии в качестве электролита допускается применять другие растворы, например, искусственную слюну или искусственную плазму. Электролиты для электрохимических методов исследований приведены в приложении А. Допускается использовать другие растворы, состав и физиологические свойства которых более соответствуют предполагаемому клиническому применению МИ. При выборе раствора следует учитывать возможный эффект, обусловленный взаимодействием белков с поверхностью имплантата.
Примечание - Для исследований в качестве электролитов применяют искусственный пот, жидкости желудочно-кишечного тракта и легочную жидкость (см. библиографию).
В отчете об исследовании приводят обоснование выбора электролита. Если в качестве электролита не применяют изотонический 0,9%-ный водный раствор хлорида натрия, то в отчете об исследовании указывают значение pH применяемого электролита.
5.3 Подготовка образов
5.3.1 Требования к образцам
Чувствительность методов, применяемых для исследований электрохимической деградации металлов и сплавов, зависит от характеристик материала, технологии его обработки и свойств поверхности. Процесс отбора образца, его форма и подготовка поверхности имеют существенное значение. Следует учитывать, что ограниченные пространства внутри или вокруг исследуемого образца могут привести к возникновению щелевой коррозии, дефекты покрытий - к питтинговой коррозии. Характеристики образца должны соответствовать характеристикам материала, который используют в готовом МИ.
5.3.2 Отбор образцов
Для каждого метода исследований химической деградации материала МИ отбирают несколько образцов в соответствии с ISO 10993-12. При значительных различиях результатов исследований необходимо определить причины этих различий и провести исследования на дополнительных образцах. Число образцов, отобранных для исследований, должно быть обосновано и задокументировано в отчете.
Если в связи с условиями изготовления материал МИ обладает анизотропными свойствами, то для исследований только свойств его поверхности следует применять образцы, разрезанные в продольном и поперечном направлениях.
5.3.3 Форма образцов
Для исследований используют стандартные образцы (например, прямоугольные или круглые стержни, пластины или изделие с одной свободной поверхностью), изготовленные способом, аналогичным изготовлению готового МИ. Допускается использовать образцы, которые представляют собой часть конкретного МИ, любой формы и любого состояния, при этом исследования необходимо проводить в тщательно контролируемых условиях, которые фиксируют в отчете.
Площадь поверхности образца, контактирующая с электролитом, должна быть определена с точностью до ±10% от общей площади поверхности образца для того, чтобы обеспечить достоверность и воспроизводимость результатов определения скорости деградации.
Если используют репрезентативные образцы, то следует учитывать возможность влияния различий между репрезентативным образцом и готовым МИ или его компонентом на результаты исследований. При исследовании репрезентативного образца вместо готового МИ в отчете приводят описание любых различий между репрезентативным образцом и готовым МИ. Отчет должен содержать подробное обоснование того, почему предполагается, что каждое из различий не повлияет на биосовместимость готового МИ.
5.3.4 Характеристики поверхности образца
Поскольку характеристики поверхности материала могут повлиять на его электрохимические свойства, то характеристики поверхности исследуемого образца должны быть идентичны характеристикам поверхности материала в готовом МИ. Характеристики поверхности исследуемого образца должны быть задокументированы в отчете.
6 Электрохимические методы измерений
6.1 Оборудование
6.1.1 Электролитическая ячейка из боросиликатного стекла по ISO 3585 соответствующих размеров, термостатируемая и контролем температуры с точностью ±1°C.
6.1.5 Рабочий электрод (исследуемый образец).
6.1.6 Измерительный электрод, изготовленный, например, из платины (сетка, пластинка или проволока) или графита, площадь которого в 10 раз превышает площадь рабочего электрода.
6.1.7 Электрод сравнения, являющийся стабильным, с известным потенциалом.
6.1.8 pH-метр с точностью измерений ±0,1.
Принципиальная схема измерительной цепи представлена в приложении B, рисунок B1.
Схема электролитической ячейки приведена в приложении C.
6.2 Подготовка образцов
Рабочий электрод (исследуемый образец) устанавливают в водонепроницаемый держатель таким образом, чтобы только исследуемая поверхность контактировала с электролитом. Следует предпринять меры предосторожности для того, чтобы между держателем и рабочим электродом не было зазора, так как в этом случае возможно возникновение щелевой коррозии образца. Перед исследованием рабочий электрод очищают в этиловом спирте с помощью ультразвука в течение 10-15 мин, затем тщательно промывают водой со степенью чистоты 2 по ISO 3696 и сразу же помещают в электролитическую ячейку.
6.3 Условия проведения измерений
При использовании магнитных мешалок необходимо учитывать возможное их воздействие на электролитическую ячейку. Данный фактор учитывают при валидации измерительного оборудования (см. 4.2).
6.4 Проведение измерений потенциодинамическим методом
Некоторые регулирующие организации могут требовать проведения исследований в соответствии со стандартами, устанавливающими потенциодинамические методы измерений, поэтому при проведении исследований методами, установленными в настоящем стандарте, рекомендуется убедиться в надлежащем использовании соответствующих методов и параметров исследований.
Примечание - Данный метод не обязателен для применения при исследовании абсорбируемых металлов.
 |
 |
6.5 Проведение измерений потенциостатическим методом
Данный метод применяют для качественного и количественного определения продуктов деградации образца, растворенных в электролите.
Примечание - Данный метод не обязателен для применения при исследовании абсорбируемых металлов.
7 Иммерсионный метод исследований
7.1 Оборудование
7.1.1 Измерительная ячейка (далее - ячейка) из боросиликатного стекла по ISO 3585 соответствующих размеров, термостатируемая и контролем температуры с точностью ±1°C.
7.1.2 pH-метр с точностью измерения ±0,1.
7.2 Подготовка образцов
При проведении долгосрочных измерений из-за биологической (например, бактериальной, грибковой) контаминации возможен риск получения недостоверных результатов. Для снижения риска контаминации следует использовать стерильные ячейки и электролит, приготовленный в асептических условиях.
Площадь поверхности образца и объем электролита должны быть достаточными для проведения последующего анализа результатов (см. раздел 8).
Не следует допускать касания образца поверхностей ячейки за исключением, минимальной линии или точки, необходимой для опоры образца. Если исследуемый образец небольших размеров, то требуемое соотношение объема электролита к площади поверхности образца может быть не достигнуто. В этом случае используют два или более образцов исследуемого материала, при этом образцы в ячейке не должны касаться друг друга.
При подготовке образцов с неровной поверхностью или неправильной формы и, следовательно, площадь поверхности которых сложно определить, необходимо руководствоваться ISO 10993-12 и ISO/TR 10993-22 для учета особенностей оценки риска таких материалов МИ.
7.3 Проведение исследований
До начала исследования измеряют рН электролита в ячейке с образцом. Затем ячейку плотно закрывают для предотвращения испарения электролита и термостатируют при температуре (37±1)°C в течение (7,0±0,1) сут. После окончания процедуры образец вынимают из ячейки и снова измеряют рН электролита. Для исследования некоторых материалов в качестве электролита применяют фосфатно-буферный физиологический раствор (т.е. стерилизация которого выполнена фильтрованием), используемый для исследований тканевых культур.
Исследования иммерсионным методом проводят в течение более длительного периода времени, если:
a) сплав используют для изготовления имплантата, применяемого постоянно;
b) сплав содержит компоненты, растворимые в биологической среде при клиническом применении МИ;
c) содержание потенциально опасных растворимых компонентов МИ приблизительно соответствует значениям предельно допустимых концентраций;
d) отсутствует дополнительная информация, подтверждающая стабильность компонентов МИ (например, о сохраняемости характеристик поверхности и допустимой коррозионной стойкости).
Для МИ, соответствующих вышеуказанным критериям, определяют характеристики процесса высвобождения потенциально опасных компонентов и их количества, чтобы установить краткосрочное и долгосрочное воздействие сплава на организм человека, которое необходимо учитывать при анализе риска МИ. Для получения количественных результатов зависимости скорости высвобождения продуктов деградации от времени воздействия электролита исследования иммерсионным методом проводят многократно на одном и том же образце. После окончания каждого предыдущего исследования его повторяют снова. Для этого образец извлекают из ячейки, отбирают электролит для измерения pH, затем образец снова помещают в ячейку с новым электролитом. Значения pH электролита измеряют в начале и в конце каждого интервала отбора проб электролита. Интервалы отбора проб электролита должны быть достаточно частыми, чтобы можно было зафиксировать основные характеристики процесса высвобождения из образца продуктов деградации (например, более частый отбор проб в более ранние моменты времени для фиксирования начала процесса выброса компонентов - начальная стадия высвобождения). Например, интервалы отбора проб электролита при исследовании нитинола, применяемого для изготовления имплантатов, могут составлять не менее нескольких дней 1, 2, 4, 7, 14, 21 и 28 в течение первого месяца суммарного времени термостатирования образцов в электролите, а затем, по крайней мере, - раз в две недели. Аналогичные результаты регистрируют при исследовании образцов из титана, т.е. зависимость кинетики высвобождения ионов из образца от времени воздействия электролита. Исследования завершают, исходя из скорости высвобождения из образца продуктов деградации, которая становится постоянной, достигая установленных значений и/или снижаясь относительно них, что свидетельствует о токсикологической опасности материала. В отчете приводят обоснование необходимости завершения исследований. Следует учитывать, что при исследовании материалов различных партий и различных производственных партий могут быть получены разные результаты исследований. В дополнение к аналитическому оборудованию также проводят валидацию применяемых методов измерений в течение всего периода исследований.
8 Анализ полученных результатов
После каждого измерения выполняют качественный и количественный анализ электролита, используя метод с чувствительностью, соответствующей цели исследования (например, атомно-абсорбционную микроскопию, масс-спектрометрию или масс-спектрометрию с индуктивно связанной плазмой). В отчете регистрируют данные о веществах, содержание которых в электролите выше предела количественного определения. Если в электролите выявлены и идентифицированы потенциально опасные биологические вещества, но не определены их количества, то дополнительно применяют другие соответствующие аналитические методы. Также в отчете регистрируют данные о всех веществах, осажденных на измерительном электроде.
9 Отчет об исследованиях
Отчет об исследованиях должен содержать следующие сведения:
a) полные идентификационные данные исследуемого образца, включая химический состав;
b) отношение площади поверхности образца, контактирующей с электролитом, к объему электролита;
c) состав и pH (с погрешностью ±0,1) электролита и описание электрода сравнения, применяемого в электрохимических методах;
d) состав, начальное и конечное значение pH электролита, применяемого в иммерсионном методе;
e) температуру электролита;
f) график зависимости потенциала от плотности тока, при необходимости сравнения - график зависимости потенциала от логарифма плотности тока (при проведении исследований потенциодинамическим методом измерений);
g) потенциал электрода при разомкнутой цепи;
i) скорость развертки (изменения) потенциала;
j) графики зависимости плотности тока от времени, общее время исследования;
k) краткий анализ кривых (например, гистерезис, пики);
I) описание любых существенных изменений поверхности образца и/или электролита;
n) метод химического анализа электролита;
o) тип электрода сравнения [значения потенциалов должны быть соотнесены со значением нормального водородного электрода (NHE)];
p) результаты анализа продуктов деградации, высвобождаемых из МИ, включая их общую кумулятивную массу (например, выраженную в мкг), скорость высвобождения (например, выраженную в мкг/сут); результаты, приведенные к единообразию по площади поверхности МИ или образца, для сравнения МИ или образцов с разными геометрическими параметрами (при проведении исследований иммерсионным методом);
q) Ф.И.О. специалиста, проводившего исследования;
r) дату(ы) исследования;
s) подпись специалиста, проводившего исследования.
Приложение A
(справочное)
Электролиты для электрохимических методов измерений
A.1 Общие положения
Для исследований используют химические вещества степенью чистоты - ч.д.а., воду - степенью чистоты 2 по ISO 3696, при этом все химические вещества должны быть растворимыми в воде. В приготовленном электролите не должно быть осадка.
A.2 Изотонический 0,9%-ный водный раствор хлорида натрия
A.3 Искусственная слюна (см. [2])
NaCI - 0,700 г/л
KSCN - 0,330 г/л
KCI - 1,200 г/л
A.4 Искусственная плазма (см. [2])
NaCI - 6,800 г/л
KCI - 0,400 г/л
A.5 Фосфатно-буферный физиологический раствор (PBS), стерилизованный фильтрованием и пригодный для клеточных культур
NaCI - 8,000 г/л
KCI - 0,200 г/л
Приложение B
(справочное)
Принципиальная схема измерительной цепи
 |
1 - потенциостат; 2 - вольтметр; 3 - амперметр; 4 - рабочий электрод; 5 - измерительный электрод; 6 - электрод сравнения
Рисунок B.1 - Принципиальная схема измерительной цепи
Приложение C
(справочное)
Схема электролитической ячейки
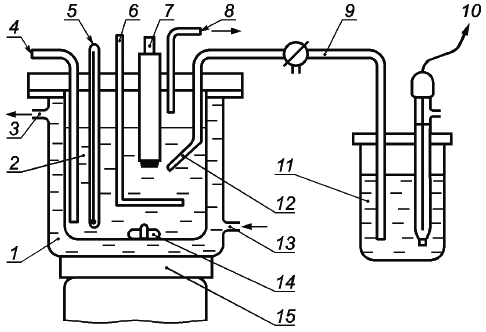 |
1 - ячейка с постоянной температурой; 2 - электролит; 3 - выходное отверстие для воды; 4 - входное отверстие для газа; 5 - термометр; 6 - измерительный электрод; 7 - рабочий электрод; 8 - выходное отверстие для газа; 9 - электролитический мостик; 10 - электрод сравнения; 11 - насыщенный раствор хлорида калия (KCI); 12 - капиллярная трубка; 13 - входное отверстие для воды с постоянной температурой; 14 - стержень магнитной мешалки; 15 - магнитная мешалка
Рисунок C.1 - Схема электролитической ячейки
Приложение ДА
(справочное)
Сведения о соответствии ссылочных международных стандартов межгосударственным стандартам
Таблица ДА.1
Обозначение ссылочного международного стандарта | Степень соответствия | Обозначение и наименование соответствующего межгосударственного стандарта |
ISO 3585 | - | * |
ISO 3696 | IDT | ГОСТ ISO 3696-2013 "Вода для лабораторного анализа. Технические требования и методы контроля" |
ISO 8044 | NEQ | ГОСТ 9.104-2018 "Единая система защиты от коррозии и старения. Покрытия лакокрасочные. Группы условий эксплуатации" |
ISO 10993-1 | IDT | ГОСТ ISO 10993-1-2021 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования в процессе менеджмента риска" |
ISO 10993-9 | IDT | ГОСТ ISO 10993-9-2022 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 9. Основные принципы идентификации и количественного определения потенциальных продуктов деградации" |
ISO 10993-12 | IDT | ГОСТ ISO 10993-12-2023 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Отбор и подготовка образцов для проведения исследований" |
ISO 10993-13 | IDT | ГОСТ ISO 10993-13-2016 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 13. Идентификация и количественное определение продуктов деградации полимерных медицинских изделий" |
ISO 10993-14 | IDT | ГОСТ ISO 10993-14-2011 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 14. Идентификация и количественное определение продуктов деградации изделий из керамики" |
ISO 10993-16 | IDT | ГОСТ ISO 10993-16-2021 "Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 16. Концепция токсикокинетических исследований продуктов деградации и выщелачиваемых веществ" |
* Соответствующий межгосударственный стандарт отсутствует. До его принятия рекомендуется использовать перевод на русский язык данного международного стандарта. Примечание - В настоящей таблице использованы следующие условные обозначения степени соответствия стандартов: - IDT - идентичные стандарты; - NEQ - неэквивалентный стандарт. | ||
_______________
Библиография
[1] | ASTM G 5-14 | Standard Reference Test Method for Making Potentiodynamic Anodic Polarization Measurements |
[2] | NF S91-141 | Biodegradability of dental metal alloys - Standardization of electrochemical tests (Сплавы металлические для стоматологических целей. Стандартные методы испытаний на электрохимическое разложение) |
[3] | ISO 10993-17 | Biological evaluation of medical devices - Part 17: Establishment of allowable limits for leachable substances (Оценка биологическая медицинских изделий. Часть 17. Установление допустимых пределов выщелачиваемых веществ) |
[4] | ISO 10271 | Dentistry - Corrosion test methods for metallic materials (Стоматология. Методы испытаний на коррозионную стойкость металлических материалов) |
[5] | Midander K., Julander A., Kettelarij J., C., Testing in artificial sweat - Is less more? Comparison of metal release in two different artificial sweat solutions. Regul Toxicol Pharmacol. 2016 Nov; 81:381-386 | |
[6] | Simulated Biological Fluids with Possible Application in Dissolution Testing, Margareth R.C. Marques, Raimar Loebenberg, and May Almukainzi | |
[7] | Walczak A.P., Fokkink R., Peters R., Tromp P., Herrera Rivera Z.E., Rietjens I.M. et al., Behaviour of silver nanoparticles and silver ions in an in vitro human gastrointestinal digestion model. Nanotoxicology. 2013, 7 pp.1198-1210 | |
[8] | ASTM WK52640 | New Guide for In-Vitro Degradation Testing of Absorbable Metals |
[9] | ISO/TR 10993-22 | Biological evaluation of medical devices - Part 22: Guidance on nanomaterials (Оценка биологического действия медицинских изделий. Часть 22. Руководство по наноматериалам) |
УДК 615.46:002:006.354 | МКС 11.100.20 |
Ключевые слова: медицинские изделия, оценка биологического действия, идентификация и количественное определение продуктов деградации изделий из металлов и сплавов | |
