ГОСТ Р 52842-2007
(ИСО 18330:2003)
Группа Н09
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
МОЛОКО И МОЛОЧНЫЕ ПРОДУКТЫ
Методы иммунологического или бактериально-рецепторного анализа для определения остатков антибактериальных веществ
Milk and milk products. Methods of immunoassays or receptor assays for the detection of antimicrobial residues
ОКС 67.100.01
Дата введения 2009-01-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 ПОДГОТОВЛЕН ОАО "Всероссийский научно-исследовательский институт сертификации" совместно с ГУ Ярославской области "Ярославский государственный институт качества сырья и пищевых продуктов" на основе аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 335 "Методы испытаний агропромышленной продукции на безопасность"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 27 декабря 2007 г. N 471-ст
4 Настоящий стандарт является модифицированным по отношению к международному стандарту ИСО 18330:2003* "Молоко и молочные продукты. Руководство по стандартизованному описанию методов иммунологического или бактериально-рецепторного анализа для определения остатков антибактериальных веществ" (ISO 18330:2003 "Milk and milk products - Guidelines for the standardized description of immunoassays or receptor assays for the detection of antimicrobial residues"). При этом в него не включен раздел "Нормативные ссылки", а дополнительные слова, фразы, абзацы, показатели и значения показателей, включенные в текст стандарта для учета потребностей национальной экономики Российской Федерации и особенностей российской национальной стандартизации, выделены курсивом.
_______________
* Доступ к международным и зарубежным документам, упомянутым здесь и далее по тексту, можно получить перейдя по ссылке на сайт .- .
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5-2004 (подраздел 3.5).
5 ВВЕДЕН ВПЕРВЫЕ
6 ПЕРЕИЗДАНИЕ. Август 2009 г.
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
1 Область применения
1 Область применения
Настоящий стандарт устанавливает общие требования к проведению и оценке результатов иммунологического или бактериально-рецепторного анализа количественного и качественного методов определения остатков антибактериальных веществ в молоке и молочных продуктах.
Иммунологический (иммуноферментный - ИФА и радиоиммунный - РИА) метод анализа основан на связывании антибактериального вещества со специфическим антителом или специфически связывающейся молекулой другого типа и позволяет количественно оценить пределы обнаружения остатков антибактериальных веществ в молоке и молочных продуктах.
К иммунологическому методу анализа относятся: иммуноферментный (ИФА) и радиоиммунный (РИА).
Бактериально-рецепторный (ферментативный и белково-рецепторный) метод анализа, как разновидность иммунологического анализа основан на связывании антибактериальных веществ с бактериальными рецепторами или рецепторными белками и применяется как для идентификации (качественное определение), так и для количественной оценки остатков антибактериальных веществ в молоке и молочных продуктах.
Бактериально-рецепторный, ферментативный и белково-рецепторный методы анализа относят к рецепторным методам.
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 ложноположительные результаты: Процент положительных результатов при исследовании отрицательных образцов.
2.2 ложноотрицательные результаты: Процент отрицательных результатов при исследовании положительных образцов.
2.3 специфичность: Возможности положительного результата в присутствии веществ с химической структурой, подобной целевому аналиту (перекрестная реакция).
2.4 предел обнаружения для качественных методов: Уровень концентрации, при которой определенный процент образцов дает положительный результат, т.е. 95% с соответствующим доверительным интервалом.
2.5 предел обнаружения для количественных методов: Уровень концентрации, при котором количественный результат анализа статистически достоверно отличается от результата отрицательного образца молока.
3 Информация, требуемая от разработчика/производителя
3.1 Порядок аттестации
Разработчик или производитель тестового набора должен представить информацию о методологии, включающую в себя следующие данные:
- описание метода (например, пробоподготовка и осуществление анализа);
- принцип метода (например, прямой конкурентный иммуноферментный анализ);
- оценку результатов анализа (например, визуальная или количественная оценка, критерии положительного или отрицательного результата);
- пропускную способность (например, количество образцов за единицу времени);
- особые требования к отбору проб, сохранению и анализу;
- процедуры контроля качества, включая применение положительных/отрицательных контрольных образцов;
- область применения, включая:
а) предназначение метода (например, скрининг для выплаты премий или пеней за качество молока, скрининг запрещенных веществ);
б) предназначение по разновидности субстрата (матрицы) (например, для анализа сырого молока из цистерны или термически обработанного молока);
в) ограничения по использованию в зависимости от состава и качества молока (например, количества соматических клеток или бактериологического качества).
3.2 Реактивы в составе тестового набора
Должна быть представлена следующая информация о реактивах в составе тестового набора:
а) при проведении иммунологического анализа:
- тип антител (например, моноклональные или поликлональные, бараньи, кроличьи или прочие);
- тип антигена, если он используется в методе (например, конъюгат антигена с ферментом, антиген, адсорбированный на твердой фазе);
- тип маркера, продуцирующего сигнал (например, фермент: пероксидаза, щелочная фосфатаза; радиоизотоп: ,
,
; инертные частицы: окрашенный латекс, коллоидное золото);
- тип субстрата ферментативной реакции или тип вещества, трансформирующего активность фермента в считываемый сигнал (например, перекись водорода/тетраметилбензидин), если применяется;
б) при проведении бактериально-рецепторного анализа:
- тип метки (например, радиоизотоп);
- уровень радиоактивности и требования безопасности и
- тип рецептора (например, инактивированные бактериальные клетки, нативные или с адсорбированными антителами);
в) при проведении белково-рецепторного анализа:
- тип используемого рецепторного белка (например, конъюгат рецептора с ферментом);
- тип вещества, конкурирующего за сайт связывания рецепторного белка (например, конъюгат фермента с аналитом, аналит, адсорбированный на твердой фазе);
- ферментативная реакция, применяемая для визуализации сигнала.
3.3 Информация о дополнительных химических реактивах, не входящих в тестовый набор
Должна быть представлена следующая информация о дополнительных химических реактивах, не входящих в тестовый набор:
- необходимая чистота и качество химических реактивов;
- состав и приготовление растворов;
- условия хранения и стабильность растворов;
- требуемое качество воды.
3.4 Требования к проведению анализа
Должна быть представлена следующая информация о требованиях к проведению анализа:
а) требования к опыту и уровню подготовки оператора;
б) требования к лабораторному оборудованию:
- микропланшетному ридеру;
- флюориметру, счетчику сцинцилляций, компьютерному оборудованию и программному обеспечению;
- инкубатору и точности автоматических пипеток;
в) требования безопасности (например, к обращению и утилизации радиоактивных отходов);
г) требования к контролю качества разработчиком/производителем и/или оператором.
3.5 Спецификация тестового набора
Должна быть представлена следующая информация о характеристиках тестового набора:
- процент ложноположительных результатов (см. 2.1);
- процент ложноотрицательных результатов (см. 2.2);
- специфичность (см. 2.3);
- предел обнаружения (см. 2.4 и 2.5) соответственно;
- точность: данные повторяемости и воспроизводимости, полученные по результатам сравнительных исследований, если проводились.
3.6 Документация
Должна быть представлена следующая документация:
- руководство пользователя, включая инструкцию по устранению ошибок и неисправностей;
- список поставщиков оборудования, реактивов, стандартов, служб технической поддержки;
- официальный статус метода в конкретной стране (если имеется);
- наличие справочного материала;
- наличие международно признаваемой апробации и/или валидации в рамках ИСО, ММФ, АОАС Интернэшнл или других организаций;
- наличие, к примеру, информационных данных и данных практических исследований.
4 Оценка показателей иммунологического (иммуноферментативного) или рецепторного (ферментативного, бактериально- и белково-рецепторного) метода
_______________
* В бумажном оригинале слова, помеченные знаком (*), выделены курсивом. - .
4.1 Обязательные требования [1]
4.1.1 Молоко, заведомо свободное от антибактериальных веществ ("отрицательное молоко")
Коровы, чье молоко надаивается для контроля в качестве "отрицательного молока", должны соответствовать следующим требованиям:
а) Животное должно быть здоровым, без клинических и субклинических признаков заболевания. Особое внимание обращают на состояние вымени (количество соматических клеток должно быть менее 150000 клеток в см);
б) Обработка кормов антибактериальными веществами должна быть запрещена не менее чем за 8 нед. до получения "отрицательного молока". Молоко не должно отбираться раньше, чем 60 дней после отела, что должно обеспечивать сухостойный период не менее 4 нед.;
в) Отбор молока следует проводить в середине лактации, от 60 до 200 дней после отела, от коров, дающих не менее 5 л молока в день;
г) Отбор молока следует проводить не менее чем от 5-7 коров, чтобы избежать влияния индивидуальных отклонений в составе молока;
д) Общая бактериальная обсемененность молока до процесса консервации (лиофилизации) должна быть менее 10 колониеобразующих единиц (КОЕ) в см
. В случае анализа на
-лактамные антибиотики необходимо иметь в виду возможность продуцирования (
-лактамазы некоторыми микроорганизмами.
При применении метода для анализа молока животных других видов требования должны быть уточнены соответственно данному виду животных.
4.1.2 Вещества, используемые при анализе
Вещества, используемые при анализе, должны быть получены от надежного разработчика/производителя и должны иметь сертификат качества с гарантированной спецификацией. Необходимую концентрацию следует рассчитывать исходя из свободной основной или кислотной формы вещества с учетом его чистоты. Особое внимание следует обращать на вещества с проблемными стабильностью и активностью.
Если не оговорено особо, то предпочтительно использовать при оценке предела обнаружения метода (см. 4.2.2) те антибактериальные вещества и/или их концентрации, которые соответствуют представленным данным разработчика/производителя.
4.1.3 Растворители
Если требуются специальные растворители или иные химикаты для растворения реактивов, то должно быть гарантировано, что данные специальные растворители или иные химические вещества не оказывают влияния на результаты анализа.
4.1.4 Подготовка образцов
4.1.4.1 Общие положения
Для расширенной оценки (например, обобщение полученных данных) все необходимые разведения делают в одной партии, чтобы избежать расхождений в точности взвешивания, разведения и различий в состоянии "отрицательного молока".
Подготовка образцов для исследования - чрезвычайно трудоемкая задача для лаборатории, проводящей оценку метода. Целесообразно использовать централизованную лабораторию, осуществляющую подготовку образцов и предоставляющую заинтересованным лабораториям образцы в стабилизированной форме (например, в глубокой заморозке или лиофилизированными).
4.1.4.2 Выбор концентраций
Процедура выбора концентраций для определения предела обнаружения приведена в 4.2.2. Ориентировочно, если не оговорено особо, концентрация, предполагаемая как предел обнаружения, должна быть проанализирована в сравнении с концентрацией на уровень больше ее и с двумя или тремя уровнями концентраций меньшими, чем предполагаемый предел обнаружения, а также с соответствующим "отрицательным молоком". Полученные данные допускается использовать для установления концентраций, дающих 25%, 50%, 75% и 95% положительных результатов. Рекомендуется разделять ранги концентраций, дающих от 50% до 100% положительных результатов на три или четыре равных отрезка уровней (с линейной и логарифмической шкалой соответственно), как показано на рисунке 1.
Рисунок 1 - Модель кривой содержание/сигнал для определения предела обнаружения
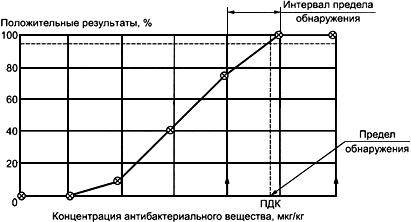
Рисунок 1 - Модель кривой содержание/сигнал для определения предела обнаружения
4.1.4.3 Разведение
Необходимо соблюдать следующие предосторожности при приготовлении серии разведений анализируемых веществ:
а) Приготовление серии разведений следует проводить таким образом, чтобы только в последнем разведении применялось молоко. Это необходимо для предотвращения связывания вещества с белком;
б) Концентрация стандартного водного раствора антибактериального вещества в последнем разведении молоком должна быть одинакова для всех образцов и составлять менее 1%.
4.1.4.4 Консервация
Консервацию образцов предпочтительнее осуществлять лиофилизацией, если это согласовано с разработчиком/производителем исходя из данных исследований или принципа метода. Рекомендуется следующая процедура консервации:
а) Сразу после подготовки различных проб молока все разведения в необходимом объеме разливают в пробирки и замораживают в наклонном положении при минус (18±2) °С;
б) Лиофилизация должна быть проведена максимально быстро, но не позднее недели после замораживания. В процессе лиофилизации температура не должна превышать 25 °С;
в) Сразу после лиофилизации пробирки герметично запаивают и хранят в темноте при температуре не выше 6 °С;
г) Образцы восстанавливают дистиллированной водой. Добавляемый объем воды должен быть на 10% меньше объема лиофилизированного молока, компенсируемого сухим остатком молока;
д) Восстановленные образцы используют в день восстановления. Используемые восстановленные образцы хранят в холодильнике и уничтожают в конце рабочего дня;
е) Допускается консервировать образцы путем глубокой заморозки или с использованием некоторых химических консервантов (см. 4.2.5.3).
4.1.5 План эксперимента
4.1.5.1 Число повторностей
Желательно, чтобы эксперимент представлял собой "слепое" исследование и максимально соответствовал рекомендациям разработчика/производителя о числе повторностей и условиях опыта. Для качественного метода процент положительных результатов от общего количества анализируемых образцов не зависит от общего числа повторностей для каждой концентрации аналита. Процентный расчет в общем случае требует не менее 10-20 повторностей для каждой выбранной концентрации. Если требуется определенная статистическая достоверность, то рассчитывают необходимое число повторностей. Например, с целью подтверждения должно быть проанализировано не менее 60 образцов для определения показателя 90% отрицательных результатов с вероятностью 95% (т.е. один или два положительных результата из 60 проанализированных образцов).
Результаты оценивают с использованием стандартных статистических методов расчета повторяемости. При применении стандартных коммерческих наборов на основе микропланшет для стандартов и образцов используют, как минимум, двойные повторности (дубли).
4.1.5.2 Оценка экспериментальных данных
Под пределом обнаружения обычно понимается концентрация, при которой показатель результата анализа образца достоверно отличается от показателя результата отрицательного контрольного образца. Для статистической оценки исключительно важно иметь установленный приемлемый доверительный интервал метода в ходе исследования. Общепринятым минимальным доверительным интервалом является уровень достоверности 95%. Тем не менее, для достижения даже этого минимального уровня достоверности необходимо провести тщательный анализ достаточно большого числа повторностей для каждой концентрации. В зависимости от предполагаемой цели анализа допускается использовать и более практичный подход.
В качественном методе показатель результата обычно сравнивают с точкой скрининга, полученной при испытаниях отрицательных или положительных контрольных образцов. Точки скрининга (например, пороговая величина или контрольный стандарт/отметка) могут быть даны изготовителем тестового набора или представлены как внутренний контрольный тест или внешний контрольный калибратор. Они или рассчитываются, или выполнены таким образом, чтобы отрицательный результат отличался от положительного не менее чем на два или три стандартных отклонения. С этой целью производители тестовых наборов иногда предоставляют для испытаний отрицательные или положительные контрольные образцы, содержащие определенное количество аналита(ов), определяемого(ых) данным методом. Как правило, выбирают концентрацию, соответствующую регламентируемой величине (например, ПДК). Используя контрольные образцы, показатель результата образца сравнивают с пороговой величиной или контрольным значением и определяют, содержит ли анализируемый образец концентрацию, аналогичную или превышающую содержащуюся в положительном контрольном образце.
Для анализа данных качественного метода рекомендуется представление результатов в виде графика, где на оси X нанесены концентрации определяемого вещества, а по оси Y - процент положительных результатов (кривая концентрация/показатель). Выбор линейной или логарифмической размерности шкалы X зависит от интервала исследуемых концентраций. Логарифмическая шкала более предпочтительна, если кратность интервала более 100.
Для количественного метода выстраивается стандартная кривая, с помощью которой определяют концентрацию аналита в образце, где ось X представляет собой шкалу концентрации определяемого вещества, ось Y - шкалу соответствующих данных, например, оптической плотности, флюоресценции или радиоактивности. Выбор линейной или логарифмической размерности шкалы X зависит от интервала исследуемых концентраций. Логарифмическая шкала более предпочтительна, если кратность интервала более 100. В этом случае строится полулогарифмическая кривая. Полулогарифмическая кривая иммунологического метода имеет, как правило, сигмовидную форму и не может быть описана линейным уравнением. Несмотря на существование множества математических методов, пригодных для описания калибровочных кривых иммунологических методов, для иммуноферментного метода, например, общепринятым является использование четырехкомпонентной логистической модели и метода наименьших квадратов. Оба метода дают сравнительно близкие результаты и по меньшей мере один из них включен в большинство программ обработки данных иммунологических методов.
В количественном методе точность оценки в значительной мере определяется расположением обнаруженной величины оптической плотности (флюоресценции или радиоактивности) на калибровочной кривой. Интервал измерения калибровочного графика соответствует максимально приближенной к линии части сигмовидной кривой (если концентрация выстроена по логарифмической шкале).
4.2 Экспериментальные параметры
4.2.1 Процент ложноположительных и ложноотрицательных результатов
В зависимости от области применения исследуемого качественного метода может быть достаточно определения вероятности ложноположительных и ложноотрицательных результатов. Исследование вероятности ложноположительных результатов включает -кратное исследование "отрицательного молока" (см. 4.1.1) или других отрицательных образцов, соответствующих предполагаемой области применения метода. Число исследований также зависит от предполагаемой области применения метода. Например, для определения показателя 90% отрицательных результатов с вероятностью 95% необходимо проанализировать не менее 60 образцов.
Вероятность ложноотрицательных результатов может быть получена с помощью кривой содержание/сигнал для ряда исследуемых концентраций. Если требуется определить достоверность, оценку проводят согласно процедуре, приведенной для оценки ложноположительных результатов при определенной концентрации (например, предел обнаружения или ПДК).
4.2.2 Предел обнаружения
Выбор антибактериального препарата для оценки предела обнаружения определяют на основе данных, заявленных разработчиком/производителем тестового набора. Принцип подготовки проб описан в 4.1.4.
Выбор оцениваемых концентраций препарата проводят следующим образом:
а) Кроме отрицательных и положительных контролей берут не менее четырех концентраций препарата, которые по предварительной оценке могут дать, соответственно, 25%, 50%, 75% и 95% положительных результатов.
б) Кроме того, в один образец добавляют антибактериальный препарат до концентрации, не менее чем на 50% превышающей концентрацию, дающую по предварительной оценке 100% положительных результатов.
в) Выбранные концентрации должны включать в себя заявленный разработчиком/производителем предел обнаружения и, если необходимо, концентрацию, соответствующую законодательно оговоренному уровню (например, ПДК).
Для качественного теста, как указано в 4.1.5.1, необходимо от 10 до 20 повторностей для каждой выбранной концентрации, чтобы рассчитать процент положительных результатов. Если нет определенных требований к статистической достоверности данных, допускается использовать более упрощенные подходы к определению предела обнаружения. Таким подходом, например, может быть принятие в качестве предела обнаружения концентрации, дающей 95% результатов, интерпретируемых как положительные.
Следуя этому подходу, предел обнаружения может быть выражен двумя способами (см. рисунок 1):
- указанием двух концентраций, между которыми находится величина, дающая 95% положительных результатов;
- определением концентрации по точке пересечения кривой содержание/сигнал с линией уровня "95% положительных результатов".
Важными практическими параметрами метода являются также процент положительных результатов на уровне концентрации, заявленной разработчиком/производителем как предел обнаружения или соответствующей законодательно установленному уровню (например, ПДК) (см. 4.2.1). Если необходима определенная статистическая достоверность, рассчитывают необходимое число повторностей для каждой концентрации.
Для количественного метода пределом обнаружения, как правило, считают уровень концентрации аналита, дающий статистически достоверное различие в результатах от отрицательных образцов; т.е. обычно это концентрация, соответствующая среднему результату отрицательных образцов с вычетом трех среднеквадратичных отклонений.
4.2.3 Специфичность
Специфичность метода характеризует возможности связывания с рецептором, и, таким образом, положительного результата для веществ с химической структурой или структурной частью, подобной оригинальному аналиту (перекрестная реакция).
Например, метаболиты оригинального аналита могут реагировать с антителом, направленным против оригинального вещества. Специфичность метода следует определять результатом специфического связывания антигеном с антителом или аналита с рецептором и отличать ее от неспецифической интерференции (см. 4.2.5). Для определения перекрестной реактивности определенного вещества определяют возможность положительной реакции для его концентрации, приблизительно в 100 раз превышающей предел обнаружения целевого вещества.
Для количественных методов специфичность рассчитывают после определения концентраций целевого вещества и концентрации перекрестно-реагирующего вещества
, дающих 50%-ное снижение сигнала результата по сравнению с отрицательным контролем. Относительную перекрестную реактивность вещества
, %, рассчитывают по формуле
![]() , (1)
, (1)
где - значение концентраций целевого вещества, дающее 50%-ное снижение сигнала результата по сравнению с отрицательным контролем;
- значение концентраций перекрестно-реагирующего вещества, дающее 50%-ное снижение сигнала результата по сравнению с отрицательным контролем.
Указывают все значительные (1%) перекрестные реактивности. В сомнительных случаях вещества перепроверяют при концентрациях, соответствующих максимальным значениям калибровочной кривой. Методы со значительной перекрестной реактивностью не могут быть использованы для количественного определения.
4.2.4 Срок годности тестового набора
Для определения изменений сигнала результата в период заявленного срока годности следуют процедуре выбора аналита, числа повторностей и оценке результатов, описанной в 4.1. Поверку проводят по меньшей мере три раза [в начале, по истечении половины срока годности (или каждые 6 мес от даты производства) и в конце срока годности]. Условия хранения (например, температура, длительность и пр.) должны соответствовать указанным разработчиком/производителем тестового набора.
4.2.5 Восприимчивость к помехам (интерференции) (устойчивость метода)
4.2.5.1 Процедура определения
Для исследования влияния возможных интерферирующих факторов (помех) в ходе анализа (например, отклонения в реактивах, условиях инкубации, объеме образца) подготавливают пробы с рядом комбинаций вещество/его концентрация в соответствии с 4.1. Протокол эксперимента включает определенные отклонения от правильной процедуры анализа.
4.2.5.2 Состав/свойства образца
На результаты иммунологических и бактериально-рецепторных методов может оказывать влияние целый ряд факторов, связанных с составом и свойствами образца. К таким факторам относятся, в первую очередь, бактериологическое качество молока, количество соматических клеток, содержание и состав жиров, рН молока, вид животного и фаза лактации (например, поздняя лактация).
В ходе оценки, беря во внимание ограничения, оговариваемые разработчиком/производителем, получают ответы на следующие вопросы:
а) Могут ли подобные факторы вести к ложноположительным результатам (например, из-за повышенного количества соматических клеток)?
б) Могут ли подобные факторы вести к ложноотрицательным результатам (например, маскирующий эффект бактериальной -лактамазы)?
в) Могут ли подобные факторы вести к ложноположительным/ложноотрицательным результатам (например, любой эффект из-за изменений в содержании и составе жира молока)?
4.2.5.3 Консервация образцов
Образцы для определения остатков антибактериальных веществ могут консервироваться или добавлением консервантов (например, борной кислоты), или глубокой заморозкой.
Если использование консервантов не запрещено разработчиком/производителем, влияние химических консервантов на результаты анализов оценивают на уровне рекомендуемой концентрации консерванта, а также на уровне более низкой и более высокой от уровня рекомендуемой. Образцы анализируют до консервации, после консервации и после хранения. Так как добавление консервантов может влиять на уровень результатов, то калибровочные образцы также консервируют соответствующим образом.
4.2.6 Обнаружение нежелательных примесей
При возможности используют контрольные материалы из проверенных источников (например, BCR).
____________ BCR - сокращенное название бюро стандартов Еврокомиссии (Bureau Communitaire de Reference). Стандарты предоставляются также Институтом стандартных материалов и измерений (IRMM), Отделом управления стандартными материалами (MRM), Retiesweg, В 2440 Geel, Belgium.
Из образцов молока, содержащих оцениваемые вещества, требуемым разведением отрицательного молока готовят пробы с концентрациями согласно 4.1.4.2. Более практичным подходом является использование молока от коров, подвергшихся лечению распространенными ветеринарными препаратами. Для сравнительных целей необходимо определение количества ветеринарных препаратов в пробах аттестованными физико-химическими методами.
4.2.7 Извлекаемость
Если экстракция образца и очистка экстракта являются частью метода, то указывают эффективность данной процедуры (извлекаемость).
4.2.8 Сравнительные испытания
Для сравнительных испытаний пробы готовят в одной лаборатории согласно 4.1.4. Пробы в требуемых условиях рассылают вместе с тестовыми наборами не менее чем в восемь участвующих лабораторий для оценки количественного метода и не менее чем в 15 лабораторий для оценки качественного метода.
При выборе подходящих веществ или их концентрации следуют процедуре согласно 4.1. Пробы кодируют и каждое вещество или концентрацию вещества в каждой участвующей лаборатории анализируют не менее 10-20 раз (при визуальном учете результатов) или 3-5 раз при использовании измерительной шкалы. Протокол эксперимента должен строго соблюдаться.
5 Оценка измеренных параметров
5.1 Возможность применения для заявленных целей
Экспертное заключение о возможности применения для заявленных целей включает в себя следующее:
- измеренные параметры иммунологического или бактериально-рецепторного метода, полученные, возможно, из различных исследований, проведенных с разными целями, в максимально возможной степени должны быть представлены в форме таблиц;
- информация, представленная в этой части заключения (таблицы), формирует основу второй его части, представляющей из себя экспертную оценку данной информации, с особым акцентом на заявленную/предполагаемую область применения метода;
- учитывая, что детальное изучение различных показателей занимает разное количество времени, особенно исследование продолжительности хранения (например, определение срока годности), заключение с оценкой исследуемых показателей приводят в разделах с указанием конкретного времени.
Эксперты должны постоянно изучать новую информацию по данному вопросу.
5.2 Рекомендации по оформлению заключения
Экспертное заключение должно включать следующий порядок разделов:
а) раздел 1:
- извлекаемость (см. 4.2.7);
- предел обнаружения (см. 4.2.2);
- вероятность ложноположительных/ложноотрицательных результатов (см. 4.2.1);
- специфичность (см. 4.2.3);
б) раздел 2:
- восприимчивость к помехам (устойчивость) (см. 4.2.5);
- обнаружение нежелательных примесей (см. 4.2.6).
в) раздел 3:
- срок годности тестового набора (см. 4.2.4);
- сравнительные испытания и точность (см. 4.2.8).
Библиография
[1] ИСО 13969:2003 | Молоко и молочные продукты. Руководство по стандартизированному описанию тестов торможения бактериального роста |
____________________________________________________________________________________
УДК 637.544:006.354 ОКС 67.100.01 Н09
Ключевые слова: молоко, молочные продукты, методы иммунологического или бактериально-рецепторного анализа, антибактериальные вещества, специфичность, предел обнаружения для качественных методов, ложноположительные и ложноотрицательные результаты
____________________________________________________________________________________
Электронный текст документа
и сверен по:
официальное издание
Молоко и молочные продукты.
Общие методы анализа: Сб. ГОСТов. -
М.: Стандартинформ, 2009
