ГОСТ 25057-81
(СТ СЭВ 2714-80)
Группа Ф14
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
КРИПТОН-85 ГАЗООБРАЗНЫЙ
Технические условия
Krypton-85 (gas). Specifications
ОКП 70 1394 1001 07
Дата введения 1984-01-01
Постановлением Государственного комитета СССР по стандартам от 22 декабря 1981 г. N 5572 срок действия установлен с 01.01.1984 г. до 01.01.1989 г.*
______________
* Ограничение срока действия снято по протоколу N 3-93 Межгосударственного Совета по стандартизации, метрологии и сертификации (ИУС N 5/6, 1993 год). - .
Настоящий стандарт распространяется на газообразную смесь изотопов криптона (далее - препарат), содержащую в своем составе радионуклид криптон-85 и выделяемую из газообразных продуктов деления при переработке облученного урана.
Стандарт полностью соответствует СТ СЭВ 2714-80.
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1. Препарат должен изготовляться в соответствии с требованиями настоящего стандарта, по рецептурам на радиоактивные препараты, утвержденным в установленном порядке.
1.2. Нижняя граница доверительного интервала измеренного значения удельной активности радионуклида криптон-85 в препарате при доверительной вероятности 0,95 не должна быть ниже 0,58 ГБк·г
.
1.3. Верхняя граница доверительного интервала измеренного значения суммарной объемной доли химических примесей - водорода, гелия, азота, кислорода, аргона и ксенона - при доверительной вероятности 0,95 не должна превышать 2%.
1.4. Активность радионуклида ксенона-133 на день паспортизации препарата не должна превышать 0,5% активности радионуклида криптон-85. Суммарная погрешность измерения не должна превышать 50% при доверительной вероятности 0,68.
1.5. Препарат должен поставляться в запаянных ампулах из термостойкого стекла. Размеры ампулы приведены на черт.1.
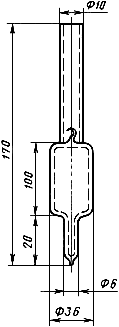
Черт.1
1.6. Номинальные значения активности препарата в ампуле должны составлять: 0,5; 1,0; 2,0; 5,0; 10,0; 20,0; 50,0; ГБк.
Отклонение активности препарата в ампуле от указанных выше номинальных значений не должно превышать 20% с доверительной вероятностью 0,95.
1.7. Поток бета-частиц, вызванный радиоактивным загрязнением поверхности ампулы с препаратом, не должен превышать 100 с. Суммарная погрешность результатов измерения не должна превышать 100% при доверительной вероятности
0,68.
2. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
2.1. При работе с препаратом должны соблюдаться: "Основные санитарные правила работы с радиоактивными веществами и другими источниками ионизирующих излучений" ОСП-72*, утвержденные Министерством здравоохранения СССР и "Нормы радиационной безопасности" НРБ-76**, утвержденные Министерством здравоохранения СССР.
__________________
* На территории Российской Федерации действуют СП 2.6.1.799-99;
** На территории Российской Федерации действуют СП 2.6.1.758-99. - .
2.2. При работе с большим количеством препарата должны быть приняты меры по интенсивному обмену воздуха в рабочих помещениях, по защите персонала от жесткого гамма-излучения криптона-85 и возможного интенсивного тормозного и характеристического излучений при бомбардировке бета-частицами атомов тяжелых элементов.
2.3. При вскрытии ампулы с препаратом необходимо учитывать, что давление газа в ней не превышает 90 кПа.
2.4. Во избежание разрушения ампулы в результате длительного воздействия бета-излучения на стекло неиспользованный препарат по истечении 12 мес срока хранения должен быть переведен в другую стеклянную ампулу или металлический баллон.
3. ПРАВИЛА ПРИЕМКИ
3.1. Препарат, подготовленный для расфасовки в ампулы, предъявляется партиями. В партию включают продукт, однородный по своим качественным показателям и сопровождаемый одним документом о качестве.
3.2. Каждую партию препарата подвергают проверке на соответствие требованиям разд.1. Для проверки от партии препарата отбирают три пробы массой от 10 до 15 мг каждая для анализа на содержание контролируемых примесей и одну пробу массой от 100 до 150 мг для определения удельной активности радионуклида криптон-85 в препарате. Последняя проба сохраняется после анализа в течение 6 мес после паспортизации препарата в качестве арбитражной пробы.
3.3. Последовательность проведения анализа должна соответствовать указанной в таблице.
Контролируемый показатель | Пункт требований | Пункт метода анализа |
Удельная активность радионуклида криптон-85 | 1.2 | 4.1 |
Содержание химических примесей | 1.3 | 4.6 |
Активность радионуклида ксенон-133 | 1.4 | 4.7 |
Уровень радиоактивного загрязнения поверхности ампулы с препаратом | 1.7 | 4.8 |
3.4. Партию продукции считают пригодной, если в результате анализа все требования, предъявляемые к ней, соответствуют настоящему стандарту.
3.5. При получении неудовлетворительных результатов анализа хотя бы по одному из показателей партию передают на переработку.
После переработки партию вторично предъявляют на анализ. Результаты повторного анализа являются окончательными и распространяются на всю партию.
4. МЕТОДЫ АНАЛИЗА
4.1. Определение удельной активности радионуклида криптон-85
Удельную активность радионуклида криптон-85 в препарате определяют путем измерения активности и массы пробы, отобранной от партии продукта и помещенной в калиброванную по объему и массе ампулу.
Массу препарата определяют путем взвешивания и вычисления разности величин, полученных при измерении массы калиброванной ампулы с препаратом и без него.
Активность радионуклида криптон-85 в ампуле определяют относительным методом, путем сличения показаний спектрометрической установки при регистрации гамма-излучения с энергией 82,35 фДж, испускаемого препаратом образцового источника радионуклида криптон-85.
Допускаются другие методы определения активности радионуклида криптон-85 в ампуле, обеспечивающие погрешность измерения, не превышающую 13% с доверительной вероятностью 0,95.
4.2. Аппаратура и материалы
Аналитические весы с пределом взвешивания до 200 г и вариацией показаний не более 0,2 мг (при пяти измерениях).
Калиброванная ампула объемом от 30 до 35 см и массой не более 50 г.
Спектрометрическая установка, в состав которой входят:
полупроводниковый детектор гамма-излучения;
блок усиления спектрометрической установки;
многоканальный амплитудный анализатор с числом каналов не менее 256.
Набор образцовых источников радионуклида криптон-85, состоящий из образцовых источников всех номинальных значений активности по п.1.4. Суммарная погрешность измерения активности радионуклида криптон-85 в образцовом источнике не должна превышать ±10% при доверительной вероятности 0,99. Ампулы для образцовых и контролируемых источников должны быть идентичными.
4.3. Подготовка к анализу
Для определения массы препарата калиброванную ампулу, предварительно откачанную до давления100 Па, помещают на чашу весов и производят пятикратное взвешивание.
Наполняют калиброванную ампулу препаратом до давления не менее 90 кПа и производят ее пятикратное взвешивание.
Для подготовки спектрометрической установки к измерениям устанавливают образцовый источник с препаратом на таком расстоянии от детектора, чтобы полная загрузка усилительного тракта спектрометрической установки не превышала 10 импульсов
с
. Измеряют спектр гамма-излучения криптона-85. Определяют сумму импульсов, зарегистрированных за время измерения
в каналах анализатора, соответствующих пику полного поглощения гамма-излучения с энергией 82,35 фДж.
Стабильность работы спектрометрической установки характеризуют выборочной величиной относительного среднего квадратического отклонения результата наблюдения и проверяют путем определения площади пика полного поглощения при 20 наблюдениях спектра одного и того же источника для выбранного режима работы, набирая при каждом наблюдении сумму импульсов
не менее 10
. Время измерения
для каждого наблюдения одинаково. Оценку относительного среднего квадратического отклонения (
) в процентах вычисляют по формуле
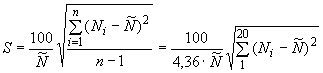 , (1)
, (1)
где - 1-й - результаты наблюдения;
- результат измерений, равный среднему арифметическому результатов наблюдений;
- число наблюдений, равное 20.
Значение не должно превышать 2%.
Измерения проводят периодически не реже одного раза в месяц.
Проверяют гипотезу о принадлежности результатов наблюдений нормальному распределению. Проверку проводят по выполнению -критерия следующим образом:
вычисляют отношение
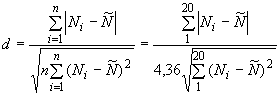 . (2)
. (2)
Результаты наблюдений считают распределенными нормально, если 0,730,88.
Если не удовлетворяет этому условию, то увеличивают число наблюдений.
Погрешность определения относительного среднего квадратического отклонения наблюдения () вычисляют по формуле
![]() . (3)
. (3)
Верхнюю границу относительного среднего квадратического отклонения нормального распределения вычисляют по формуле
![]() . (4)
. (4)
Наблюдают показания спектрометрической установки, обусловленные внешним фоном. Наблюдения проводят два раза: до и после измерений. Время наблюдения фона - . Определяют сумму импульсов, зарегистрированных в каналах, соответствующих пику полного поглощения гамма-излучения с энергией 82,35 фДж и вычисляют среднее значение результата измерения фона (
) по формуле
![]() , (5)
, (5)
где и
- средние значения результатов наблюдений фона перед и после измерений.
При выборе условий измерения должно выполняться неравенство
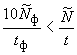 ,
,
где - результат наблюдения при измерении источника криптона-85 любого номинального значения активности.
4.4. Проведение анализа
Сначала устанавливают контролируемый источник и проводят три определения суммы импульсов в пике полного поглощения гамма-излучения с энергией 82,35 фДж - . Время наблюдения
выбирают таким, чтобы
было не менее 10
импульсов. Определяют среднее значение результатов наблюдения
. Заменяют контролируемый источник на соответствующий образцовый источник криптона-85. Проводят не менее трех наблюдений и определяют среднее значение
.
4.5. Обработка результатов
Среднее значение результатов наблюдений () в миллиграммах при взвешивании калиброванной ампулы с препаратом определяют по формуле
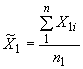 . (6)
. (6)
5.
Среднее значение результатов наблюдений () в миллиграммах при взвешивании вакуумированной калиброванной ампулы определяют по формуле
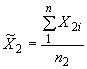 . (7)
. (7)
5.
Среднее значение массы пробы () вычисляют по формуле
![]() . (8)
. (8)
Оценку средних квадратических отклонений ![]() и
и результатов каждой из серий взвешивания вычисляют по формулам:
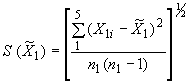 , (9)
, (9)
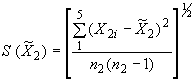 . (10)
. (10)
Оценку среднего квадратического отклонения ![]() результатов измерения массы пробы препарата определяют по формуле
результатов измерения массы пробы препарата определяют по формуле
![]() . (11)
. (11)
Доверительную границу случайной погрешности результата измерений массы пробы препарата вычисляют по формуле
![]() . (12)
. (12)
где ![]() - квантиль распределения Стьюдента при доверительной вероятности
- квантиль распределения Стьюдента при доверительной вероятности и степенях свободы
![]() ;
;
- число параллельных взвешиваний.
При 0,95,
5 и
4;
![]() и
и ![]() .
.
Границу суммарной погрешности ![]() результата измерения массы пробы препарата вычисляют по формуле
результата измерения массы пробы препарата вычисляют по формуле
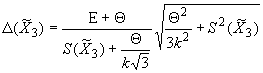 , (13)
, (13)
где ![]() - граница неисключенной систематической погрешности результата взвешивания;
- граница неисключенной систематической погрешности результата взвешивания;
- граница
-й неисключенной систематической погрешности, включающей следующие составляющие: неравноплечность коромысла весов (
2 мг); неточность навешивания встроенных гирь (
0,12 мг); неточность массы разновесов (
0,1 мг).
Суммарная погрешность результата измерения массы пробы препарата не должна превышать 2% при доверительной вероятности 0,95.
Форма записи результатов измерения массы пробы:
![]() ,
, 0,95.
Активность радионуклида криптон-85 () в контролируемом источнике с препаратом вычисляют по формуле
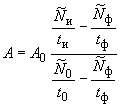 . (14)
. (14)
Относительное среднее квадратическое отклонение результата измерений и
определяют по формуле
![]() . (15)
. (15)
Значение определено по формуле (4). При измерениях фона значение
![]() вычисляют по формуле
вычисляют по формуле
![]() , (16)
, (16)
где принимают равной
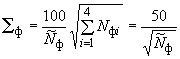 . (17)
. (17)
Доверительную границу относительной случайной погрешности результата измерений вычисляют по формуле
![]() , (18)
, (18)
где - квантиль нормального распределения для доверительной вероятности
0,95.
1,960.
Доверительную границу неисключенной относительной систематической погрешности результата измерений активности
вычисляют по формуле
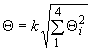 . (19)
. (19)
К компонентам относительной систематической погрешности - относятся:
погрешность аттестации образцового источника по активности радионуклида криптон-85 (10%;
0,99);
неидентичность ампул образцового и контролируемого источников (4%; равномерное распределение);
зависимость разрешающего времени спектрометрической установки от загрузки усилительного тракта - . При сличении контролируемого и образцового источников, имеющих значение активности радионуклида криптона-85 одного номинала,
2% (равномерное распределение);
погрешность определения времени измерения 0,1% (равномерное распределение);
1,1 для доверительной вероятности
0,95.
Доверительную границу относительной суммарной погрешности результата измерения активности радионуклида криптон-85 в контролируемом источнике вычисляют по формуле
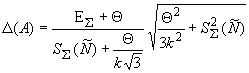 , (20)
, (20)
где - доверительная граница относительной случайной составляющей погрешности результата измерения активности
.
![]() . (21)
. (21)
![]() ; (22)
; (22)
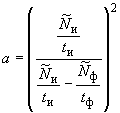 ; (23)
; (23)
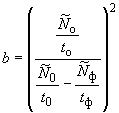 ; (23а)
; (23а)
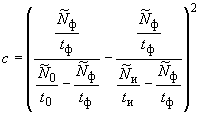 , (24)
, (24)
,
и
- доверительные границы относительной случайной погрешности результатов измерений величин
,
и
, определенные по формуле (18);
![]() ,
, ![]() ,
, ![]() - относительные средние квадратические отклонения результата измерения
- относительные средние квадратические отклонения результата измерения ,
и
, определенные по формулам (15) и (16).
Суммарная погрешность результатов измерения активности не должна превышать 13% при доверительной вероятности
0,95.
Форма записи результатов измерения активности радионуклида криптон-85: ![]() Бк,
Бк, 0,95.
Удельную активность () в Бк·г
радионуклида криптон-85 в препарате вычисляют по формуле
![]() , (25)
, (25)
где - измеренная активность радионуклида криптон-85 в пробе, Бк;
- измеренная масса пробы, г.
Суммарную погрешность результата измерения удельной активности радионуклида криптон-85 в препарате при доверительной вероятности
0,95 вычисляют по формуле
![]() , (26)
, (26)
где и
![]() - суммарные погрешности результатов измерения активности препарата в пробе и ее массы, вычисленные по формулам (20) и (13).
- суммарные погрешности результатов измерения активности препарата в пробе и ее массы, вычисленные по формулам (20) и (13).
Форма записи результатов измерения удельной активности препарата в пробе:
![]() ,
, 0,95.
4.6. Определение массовых долей контролируемых химических примесей в криптоне-85
4.6.1. Аппаратура и материалы
Хроматографическая установка, приведенная на черт.2 и включающая следующие основные узлы:
газовый хроматограф, оснащенный детекторами с порогом чувствительности определения объемной доли газов-примесей не ниже 0,001%. При этом погрешность измерения не должна быть более 10% при доверительной вероятности 0,95;
газо-вакуумный стенд для приготовления образцовых смесей и разбавления контролируемой пробы, снабженный системой вакуумных вентилей и игольчатых натекателей, образцовым пружинным вакуумметром класса 0,16 с диапазоном измерения от 0,2 до 100 кПа, образцовым манометром класса не ниже 0,2 с диапазоном измерения от 0,1 до 0,4 кПа, термопарным вакуумметром, калиброванными по объему баллонами, вакуумными насосами, обеспечивающими достижение в установке давления не выше 0,5 Па;
калиброванный дозатор вместимостью (2,0±0,02) см;
калиброванные емкости вместимостью 10; 200 и 1000 см;
термостат для регулирования и поддержания температуры газа в калиброванных емкостях и дозаторе. Погрешность определения и поддержания температуры в термостате не должна превышать ±0,5% в диапазоне температур от 0 до +50 °С;
циркуляционный насос для перемешивания газовых смесей;
цеолитовая ловушка для адсорбции ксенона с устройством для охлаждения жидким азотом и печью для нагрева до температуры от +150 до +200 °С;
баллоны высокого давления для хранения сжатых газов-носителей (гелий, аргон) и газов для приготовления образцовых смесей (водород, кислород, азот, ксенон, гелий, аргон).
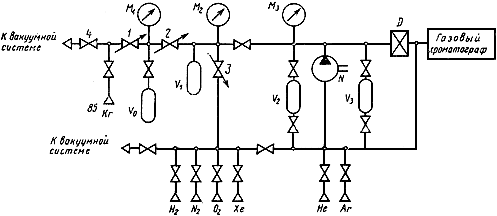
1, 2, 3 - игольчатые натекатели; 4 - вентиль; ,
,
,
- калиброванные емкости;
- циркуляционный насос;
- калиброванный дозатор;
- манометр с пределом измерения от 100 до 600 кПа;
,
- манометр с пределом измерения от 0 до 100 кПа
Черт.2
Газы-носители аргон, гелий, в которых объемная доля каждой из контролируемых химических примесей не превышает 0,005%;
газы для составления образцовых смесей (при отсутствии готовых образцовых смесей) высокой чистоты - водород, кислород, азот, аргон, гелий, ксенон или образцовые смеси, в объемных долях:
гелий 99,9% - азот 0,1%;
гелий 99,9% - кислород 0,1%;
гелий 99,9% - аргон 0,1%;
гелий 99,9% - ксенон 0,1%;
аргон 99,9% - водород 0,1%;
аргон 99,9% - гелий 0,1%.
Погрешности определения в образцовых смесях содержания газов-примесей не должны превышать 5% при доверительной вероятности 0,99.
Молекулярное сито 50 нм (фракция от 0,25 до 0,5 мм).
Активированный уголь марки СКТ (фракция от 0,25 до 0,5 нм) или уголь, соответствующий ему по характеристикам.
4.6.2. Подготовка к анализу
Для приготовления образцовой смеси проводят следующие операции:
откачивают систему до давления 0,5 Па;
промывают систему газом-носителем и вновь откачивают до давления 0,5 Па;
наполняют калиброванную емкость (
10 см
) газом-примесью до давления
10 кПа через игольчатый натекатель;
откачивают газ-примесь из трубопровода, соединяющего баллон с баллоном высокого давления;
дополняют калиброванную емкость другим газом-примесью до давления от 18 до 20 кПа через игольчатый вентиль.
Повторяя две последние операции, вводят в смесь все газы-примеси, увеличивая каждый раз давление в калиброванной емкости на 10 кПа.
Проводя операции заполнения, фиксируют показания манометра с максимальной точностью.
Выдерживают приготовленную смесь газов-примесей в баллоне для гомогенизации смеси в течение 60 мин.
Отбирают из баллона с помощью калиброванного дозатора
пробу (объемом 2 см
) и впускают газовую смесь в предварительно откачанный до остаточного давления
0,5 Па баллон
(200 см
). Проводя эту операцию, фиксируют показания термометра с максимальной точностью.
Разбавляют пробу в баллоне газом-носителем, доводя давление газа до 98 кПа.
Выдерживают смесь в баллоне в течение 60 мин, перемешивая ее циркуляционным насосом. Допускается гомогенизация смеси выдержкой от 2 до 3 сут. По истечении этого времени образцовая смесь готова для проведения градуировки хроматографической установки. Вычисляют концентрацию каждого из газов-примесей в смеси.
Приготовление образцовых смесей более низких концентраций производят аналогичным образом, регулируя давление газа в баллоне и используя для разбавления калиброванную емкость
(1000 см
).
Номинальные значения объемных долей контролируемых примесей в смеси должны составлять следующий ряд: 0,02; 0,03; 0,04; 0,06; 0,08; 0,09; 0,10%.
Фактическое содержание контролируемых примесей в образцовых смесях не должно отличаться более, чем на 10% от указанных номинальных значений.
Конструкция газо-вакуумного стенда и калиброванного дозатора, организация и качество проведения операции приготовления образцовых смесей должны обеспечить определение содержания контролируемых примесей в них с погрешностью не более 5% при доверительной вероятности 0,99.
Градуируют хроматографическую установку по каждой -той; контролируемой примеси, используя приготовленные (или готовые) образцовые смеси.
Градуировка осуществляется по пробам каждого из семи номинальных содержаний при числе параллельных наблюдений 3.
По данным измерений, используя метод наименьших квадратов, вычисляют коэффициенты линейной регрессии, определяющей связь содержания примеси в контролируемой пробе с результатами измерения площади пика на хроматограмме.
Процесс градуировки должен быть проведен таким образом, чтобы погрешность определения коэффициентов линейной регрессии не превышала 10% при доверительной вероятности 0,99.
При градуировке по ксенону пробу, прошедшую через адсорбционную колонну хроматографа (через 7 мин после введения пробы в поток газа-носителя), конденсируют в ловушке, охлаждаемой жидким азотом. Процесс вымораживания ксенона длится от 35 до 40 мин. После этого ловушку интенсивно нагревают и десорбирующийся при нагревании ксенон направляют потоком газа-носителя в катарометр д
ля регистрации пика.
4.6.3. Проведение анализа
Содержание в препарате примесей водорода, гелия, азота, ксенона и смеси кислорода с аргоном определяют хроматографическим методом путем измерения и сличения хроматографических пиков, полученных при анализе контролируемой пробы и проб образцовых газовых смесей.
Вводят в предварительно вакуумированный объем пробу препарата под давлением от 120 до 130 кПа.
Через игольчатый натекатель вводят пробу в калиброванную емкость до давления от 90 до 95 кПа.
Отбирают калиброванным дозатором пробу объемом 2 см
к вводят в поток газа-носителя, фиксируя с максимальной точностью значение давления и температуру газа в объеме
.
Анализ на содержание примеси водорода и гелия проводят, используя в качестве газа-носителя аргон. Остальные примеси - азот, кислород, аргон и ксенон - анализируются при введении пробы в газоноситель гелий.
Анализ содержания ксенона проводят с использованием процесса его адсорбции - десорбции на сорбционной ловушке.
Количественный анализ содержания примесей в препарате должен быть проведен так, чтобы погрешность измерений не превышала 13% при доверительной вероятности 0,95.
4.6.4. Обработка результатов
Содержание - объемную долю в процентах - -ой контролируемой примеси в образцовой смеси (
) вычисляют по формуле
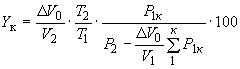 , (27)
, (27)
где ,
и
- объемы калиброванного дозатора и емкости
и
соответственно, см
;
,
- температура газа в емкости
и
в моменты отбора пробы дозатором, К;
- парциальное давление газа
-ой примеси в емкости
;
- общее давление образцовой смеси в емкости
.
По данным, полученным при градуировке хроматографической установки, определяют коэффициенты регрессий в молях
для каждой
-ой примеси
![]() , (28)
, (28)
где - площадь пика на хроматограмме для
-ой примеси, см
;
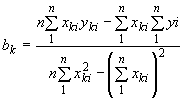 , (29)
, (29)
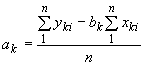 , (29а)
, (29а)
где ![]() ;
;
- число экспериментальных точек на линии регрессии с разным содержанием
-ой примеси при градуировке;
- число параллельных определений контролируемой примеси в каждой из
точек.
Оценку дисперсии измеренных значений содержания
-ой примеси
относительно вычисленных
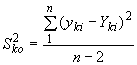 (30)
(30)
со степенями свободы ![]() .
.
Выражение (30) может быть представлено в другой форме:
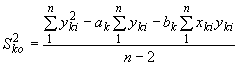 . (31)
. (31)
Находят оценки дисперсий для констант и
.
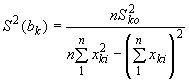 , (32)
, (32)
![]() . (33)
. (33)
Доверительные границы погрешности результатов определения и
при доверительной вероятности
0,95 вычисляют по формулам:
![]() , (34)
, (34)
![]() , (35)
, (35)
где ![]() - квантиль распределения Стьюдента при доверительной вероятности
- квантиль распределения Стьюдента при доверительной вероятности и степенях свободы
![]() .
.
При 0,95 и
![]() .
.
(0,95:19)=2,09.
Среднее значение объемной доли -ой примеси (
) в процентах в параллельных пробах определяют по формуле
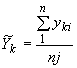 . (36)
. (36)
При расчете пользуются уравнением регрессии (28).
Оценку среднего квадратического отклонения результатов измерения содержания -ой примеси в пробе по трем параллельным пробам
![]() вычисляют по формуле
вычисляют по формуле
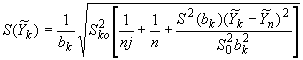 , (37)
, (37)
где - среднее значение из
измерений содержания
-ой примеси при градуировке хроматографа по образцовым смесям.
Доверительную границу случайной погрешности результата измерения содержания -ой примеси в пробе (
) вычисляют по формуле
![]() , (38)
, (38)
где ![]() - квантиль распределения Стьюдента при доверительной вероятности
- квантиль распределения Стьюдента при доверительной вероятности и степенях свободы
![]() .
.
Границу суммарной погрешности результата измерения содержания -ой примеси в пробе (
) вычисляют по формуле
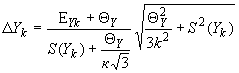 , (39)
, (39)
где 1,1 при доверительной вероятности
0,95,
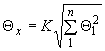 - граница неисключенной систематической погрешности результата измерения
- граница неисключенной систематической погрешности результата измерения -ой примеси в пробе, включающей следующие компоненты:
погрешность определения объема калиброванного дозатора (1%,
0,95);
погрешность показаний образцового вакуумметра (1,6%,
0,95);
погрешность определения калиброванной емкости (0,5%,
0,95);
погрешность определения температуры газа (1%,
0,95);
погрешность, связанная с дрейфом нуля электронного потенциометрического самописца (0,5%,
0,95);
погрешность показаний образцового манометра (0,3%,
0,95).
Форма записи результатов измерения объемной доли в процентах -ой примеси в препарате
![]() ,
, 0,95.
Суммарная погрешность результатов определения -ой примеси в препарате не должна превышать 15% при доверительной вер
оятности 0,95.
4.7. Определение активности примесного радионуклида ксенон-133 в препарате
Определение основано на измерении числа гамма-квантов радионуклида ксенон-133 с энергией 13,0 фДж в спектре гамма-излучения, испускаемого пробой с препаратом.
4.7.1. Аппаратура
Спектрометрическая установка в соответствии с п.4.2.
4.7.2. Подготовка к анализу - по п.4.3.
4.7.3. Проведение анализа
После подготовки спектрометрической установки к анализу определяют сумму импульсов, соответствующих пику полного поглощения гамма-излучения с энергией 13,0 фДж, зарегистрированных за время
.
Определяют сумму импульсов, зарегистрированных за то же время в каналах, соответствующих пику полного поглощения гамма-излучения с энергией 82,35 фДж.
Эти операции проводят трижды на одной пробе.
4.7.4. Обработка результатов
Среднее значение результатов измерения и
определяют по формулам
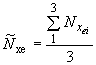 , (40)
, (40)
 . (41)
. (41)
Активность радионуклида ксенон-133 вычисляют по формуле
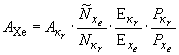 , (42)
, (42)
где - активность радионуклида криптон-85 в пробе продукта, определенная по п.4.1 настоящего стандарта;
,
- эффективности регистрации пиков полного поглощения гамма-излучения с энергией 82,35 и 13,0 фДж соответственно;
0,43%;
37% - выход гамма-квантов с энергией 82,35 и 13 фДж на акт распада радионуклидов криптон-85 и ксенон-133, соответственно.
Суммарная погрешность определения активности радионуклида ксенон-133 не должна превышать 50% при доверительной вероятности 0,68.
4.8. Определение уровня радиоактивного загрязнения наружных поверхностей ампул
Уровень радиоактивного загрязнения определяют методом "влажных мазков". Определение основано на измерении потока бета-частиц, испускаемого тампоном из марли или ваты после протирания им наружной поверхности ампулы с препаратом. Поток бета-частиц, испускаемый тампоном, измеряют относительным методом путем сличения показаний радиометрической установки при измерении тампона и образцового источника.
4.8.1. Аппаратура и материалы
Радиометрическая установка, в состав которой входят:
торцовый счетчик;
счетное устройство.
Образцовый источник бета-излучения на основе радионуклидов стронция-90+иттрий-90 с активностью нуклидов в источнике от 100 до 300 Бк.
Тампоны из марли или ваты, размеры которых должны быть близкими к размеру рабочей поверхности используемого образцового источника.
4.8.2. Проведение анализа
Эффективность регистрации бета-излучения установкой вычисляют по формуле
![]() , (43)
, (43)
где - скорость счета (импульс с
) при измерении образцового источника;
- скорость счета импульсов, обусловленных внешним фоном;
- поток бета-частиц, испускаемый образцовым источником (с
) рассчитывают по формуле
![]() . (44)
. (44)
Коэффициент учитывает число бета-частиц, испускаемых на один акт распада радионуклидов стронций-90 и иттрий-90, поглощение бета-частиц в слое, обратное рассеяние частиц от подложки. В настоящем методе коэффициент
2.
Измеряют скорость счета импульсов фона радиометрической установки. Для определения радиоактивного загрязнения используют установку, скорость счета импульсов фона которой не превышает значения
![]() ,
,
где ![]() 200 с
200 с (
- площадь поверхности ампулы с препаратом, см
).
Определяют скорость счета импульсов при измерении потока бета-частиц, испускаемого тампоном.
4.8.3. Обработка результатов
Поток бета-частиц, вызванный радиоактивным загрязнением поверхности ампулы, определяемый потоком бета-частиц, испускаемым тампоном, вычисляют по формуле
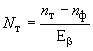 . (45)
. (45)
Значение не должно превышать 100 с
.
Суммарную относительную погрешность измерения () для доверительной вероятности
0,68 вычисляют по формуле
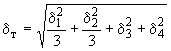 , (46)
, (46)
где - относительная систематическая составляющая погрешности, обусловленная погрешностью определений потока бета-частиц, испускаемого образцовым источником;
50%, (
0,99);
- относительная систематическая составляющая погрешности, определяемая различием в технологии изготовления образцового источника и измеряемого тампона, а также зависимостью
от спектрального состава бета-излучения образцового источника и тампона;
60% (равномерное распределение);
и
- относительные случайные составляющие погрешности измерения скорости счета при измерении потока бета-частиц, испускаемого образцовым источником и тампоном;
![]() 15% (
15% (0,68);
50% (
0,68).
5. УПАКОВКА, МАРКИРОВКА, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
5.1. Упаковка
Препарат должен поставляться в запаянных ампулах из термостойкого стекла. Размеры ампулы приведены на черт.2.
Ампула с препаратом устанавливается в герметичный пенал (черт.3) и упаковывается в защитный транспортный контейнер завода-изготовителя.
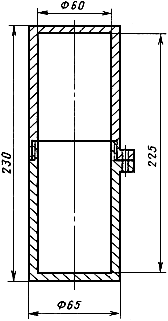
Черт.3
В наружную упаковку транспортного контейнера вкладывается инструкция по его эксплуатации и паспорт на препарат.
5.2. Маркировка
Маркировка ампулы и герметичного пенала должна отвечать требованиям ГОСТ 25058-81.
5.3. Транспортирование
Ампулы с препаратом, упакованные в соответствии с требованиями п.5.1, должны транспортироваться в соответствии с "Правилами безопасности при транспортировании радиоактивных веществ" (ПБТРВ-73), утвержденными Министерством здравоохранения СССР любым видом транспорта, без ограничения расстояния.
5.4. Хранение
Ампулы с препаратом должны храниться в складских помещениях при температуре окружающей среды от минус 70 до плюс 50 °С.
Допустимый срок хранения препарата в ампулах - четыре месяца с момента паспортизации.
6. ГАРАНТИИ ИЗГОТОВИТЕЛЯ
6.1. Изготовитель должен гарантировать соответствие криптона-85 газообразного требованиям настоящего стандарта при соблюдении условий транспортирования и хранения, установленных настоящим стандартом.
6.2. Гарантийный срок хранения препарата в ампулах составляет четыре месяца с момента паспортизации препарата техническим контролем изготовителя.
Электронный текст документа
и сверен по:
М.: Издательство стандартов, 1982
